碳钢因其硬度高、强度好且成本低而被广泛应用于海洋和水利工程金属结构,如海上钻井平台、跨海大桥、水坝闸门、输水管道等设施[1,2]。然而,在自然环境中长期暴露使用的过程中,由于温度差异引发的露水凝结等环境因素,金属表面往往会形成液滴或液膜等液态介质[3,4]。这种表面液态介质的存在显著改变了金属原有的电化学状态,在金属表面形成腐蚀微电池,进而诱发大气腐蚀问题[5,6]。在实际工程应用中,大气腐蚀已然成为影响海工和水工金属结构的安全性和使用寿命的主要问题之一[7]。腐蚀所导致的碳钢损伤不仅会显著降低金属结构的强度和稳定性,缩短其使用寿命,还可能引发一系列安全隐患,对相关工程设施的正常运行以及人类的生命财产安全构成严重威胁[8~10]。
目前,国内外学者围绕液滴下金属大气腐蚀的研究已经取得了一定成果。EL-Mahdy等[11]通过液滴形状分析仪系统研究了液滴形态对碳钢腐蚀速率的影响,实验结果表明,随着腐蚀时间的延长,液滴接触角和高度逐渐减小,腐蚀速率呈现显著增加趋势。值得注意的是,由于液滴尺寸的特殊性,传统电化学手段难以有效测量液滴下的腐蚀行为。这一定程度上限制了深入的研究。针对这一问题,Rahimi等[12]采用微型三电极技术,对单液滴下纯铁的早期电化学行为进行了深入研究,研究表明,在0.01 mol/L NaCl浓度下,腐蚀主要以氧扩散为主导,且呈现均匀腐蚀特征;而在0.1和0.2 mol/L NaCl浓度下,Cl-的富集加速了阳极溶解过程,导致局部腐蚀的发生。这些研究表明液滴电导率变化对腐蚀损伤的发展过程具有显著影响。在此基础上,Wang和Shui[13]采用扫描Kelvin探针参比电极技术,系统研究了液层厚度对氧还原速度的影响机制,实验结果表明,液层厚度的减薄会显著提升氧还原速度,但当液层厚度达到一定程度时,氧还原速度反而迅速下降。
尽管上述研究均从宏观上说明液滴条件变化对金属腐蚀的影响,但均未开展局部腐蚀信息的监测,导致液滴下金属表面局部腐蚀机理尚不明确。由于液滴下的金属腐蚀具有显著的局部腐蚀特征,为了深入研究液滴下金属的腐蚀机理,需要获取其局部电化学数据,尤其是与金属腐蚀密切相关的局部电流和电位分布信息。近年来,丝束电极技术(WBE)已被广泛应用于解决局部腐蚀问题的研究中。Tan[14~16]利用该技术研究了液滴下碳钢腐蚀的非均匀相电化学过程。Wang等[17]使用WBE研究了304不锈钢在1 mol/L NaCl液滴下的腐蚀电位/电流分布,发现局部腐蚀速率和非均匀性随时间先增大后减小。Muster等[18]研究液滴特性对Zn大气腐蚀的影响,认为金属锌在不同尺寸(1~10 μL) 0.6 mol/L NaCl液滴下电流密度基本一致,但NaCl浓度的变化对小液滴(1 μL)下的腐蚀行为影响最小,对大液滴(10 μL)下的腐蚀行为影响较为显著。Wang等[19]结合丝束电极技术分析了液滴下局部腐蚀动力学,并对液滴环境下管道顶部金属腐蚀机理进行探究。Tang等[20~22]研究了纯铁在3.5% (质量分数) NaCl液滴下的局部电化学腐蚀过程,表明当液滴扩展时,新覆盖电极表面作阴极使阳极电偶电流密度增加;当液滴变薄时,局部腐蚀倾向降低。Wang等[23]研究了碳钢在0.001 mol/L NaCl液滴下的腐蚀电位/电流分布,表明阳极位置随时间从中心向三相边界(TPB)区域边缘移动。
综上所述,大量研究表明液滴电导率的差异会显著影响金属腐蚀的发展过程。事实上,在实际工程环境中,由于服役环境的差异,近海区与远海区金属结构表面的腐蚀性介质存在显著不同电导率特征[24]。因此,深入探究液滴电导率变化对金属腐蚀机理的影响具有重要的工程意义。因此,本研究通过实验室模拟大气中的不同液滴环境并结合电化学测试与WBE技术,利用不同浓度NaCl模拟不同电导率开展了液滴电导率梯度变化对金属表面局部腐蚀发展行为的影响研究。首先采用动电位扫描法系统测量了碳钢在不同电导率溶液中的极化曲线,提取了相关电化学动力学参数。随后,利用WBE技术对不同电导率液滴下碳钢表面电流和电位分布进行了系统表征,并基于耦合电位理论深入探讨了不同电导率液滴下碳钢的腐蚀损伤机理。
1 实验方法
1.1 极化曲线测试
本实验采用尺寸为10 mm × 10 mm × 3 mm Q355b钢试样开展不同电导率溶液中金属材料的电化学信息测试,其工作面积为1 cm2。Q355b钢化学成分(质量分数,%)为:C 0.24,Si 0.55,Mn 1.60,S 0.035,P 0.035,Cr 0.30,Ni 0.30,Cu 0.30,Fe余量。使用环氧树脂将Q355b钢进行封装处理,封装后依次用400#、800#、1000#和2000#水磨砂纸逐级打磨,然后用乙醇清洗表面并用冷风吹干。最后将试样置于通风条件良好且干燥的环境中晾干24 h。
将制备好的碳钢试样分别置于1 L浓度为0.001、0.003、0.2和0.5 mol/L的NaCl溶液中,分别对应由低到高不同导电率NaCl溶液环境,实验温度控制在20 ℃,待开路电位稳定后,采用CS350型电化学工作站首先进行阻抗谱测试,以便对后续极化曲线测试进行溶液电阻补偿,随后对试样进行极化曲线测试。需要注意的是,由于极化曲线测试会使溶液中离子浓度增大,对溶液的电导率产生影响,导致测量结果与真实值存在偏差。因此,本文的极化曲线测试中采用的扫描电位范围为相对开路电位±70 mV,扫描速率为0.334 mV/s,以缩短测量时间。测试结束后,采用四参数方程分别拟合出其阳极和阴极Tafel斜率,即βa 和βc。
1.2 局部电化学测试
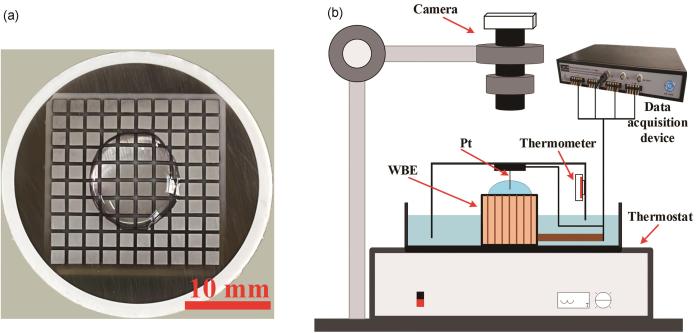
本实验选用由Q355b钢材料制成的丝束电极开展研究。实验所用的每个电极面积均为2 mm × 2 mm,将这些电极均匀排列成10 × 10的矩阵,并通过环氧树脂进行密封工艺处理制成,电极之间彼此绝缘,间距为0.2 mm,如图1a。实验前分别用400#、800#、1000#和2000#的水磨砂纸对丝束电极表面逐级打磨,然后用乙醇清洗表面,用冷风吹干,备用。
图1
图1
丝束电极实物图及局部电化学测试实验装置示意图
Fig.1
Physical image of the wire beam electrode (a) and schematic diagram of the local electrochemical test experimental setup (b)
将丝束电极置于人工气候箱中,通过在箱底放置与液滴相同浓度的NaCl溶液来控制实验箱中的相对湿度,保持环境相对湿度RH为85%,温度为(20±1) ℃。如图1a所示,使用微量注射器在丝束电极表面依次滴加300 μL浓度为0.001、0.003、0.2和0.5 mol/L的NaCl液滴,随后对其进行电位和电偶电流分布测试。图1b为测试装置示意图。测量电偶电流时,依次断开100根丝束电极,测量每根丝与其余短接电极之间的电偶电流,测量时间间隔为1 min。测量电位时,使用铂丝作为参比电极,测量时间间隔为1 h,实验共进行5 h,测量结果与饱和甘汞电极(SCE)进行校准。测试结束后,将丝束电极表面液滴擦去。实验过程中通过摄像头拍照记录实验初期、末期液滴形状及实验结束除锈后的腐蚀形貌。
2 实验结果
2.1 不同浓度溶液下碳钢极化曲线
图2
图2
在不同浓度的NaCl溶液中Q355b碳钢的极化曲线
Fig.2
Polarization curves of Q355b carbon steel in NaCl solutions with different concentration
式中,I表示腐蚀金属电极的外侧电流密度,mA/cm2;∆E表示极化曲线测量时极化电位的绝对值,mV。Icorr表示金属的腐蚀电流密度,mA/cm2;βa 表示阳极反应的Tafel斜率,mV/dec;βc表示阴极反应的Tafel斜率,mV/dec;IL表示极限扩散电流密度的绝对值,mA/cm2。四参数分别为Icorr、βa 、βc和IL,均满足不小于零,且IL始终不小于Icorr。通过四参数方程式拟合得到碳钢在不同电导率溶液中极化曲线的电化学参数如表1所示。
表1 Q355b碳钢在不同浓度的NaCl溶液中极化曲线的拟合电化学参数
Table 1
| Concentration | Icorr / mA·cm-2 | βa / mV·dec-1 | βc / mV·dec-1 | IL / mA·cm-2 |
|---|---|---|---|---|
| 0.001 mol/L | 0.0124 | 76.96 | 22.58 | 0.0233 |
| 0.003 mol/L | 0.0152 | 67.47 | 26.77 | 0.0232 |
| 0.2 mol/L | 0.0191 | 43.77 | 178.84 | 1.27 × 1015 |
| 0.5 mol/L | 0.0038 | 24.93 | 85.47 | 1.17 × 1017 |
2.2 不同浓度液滴下碳钢表面电流分布
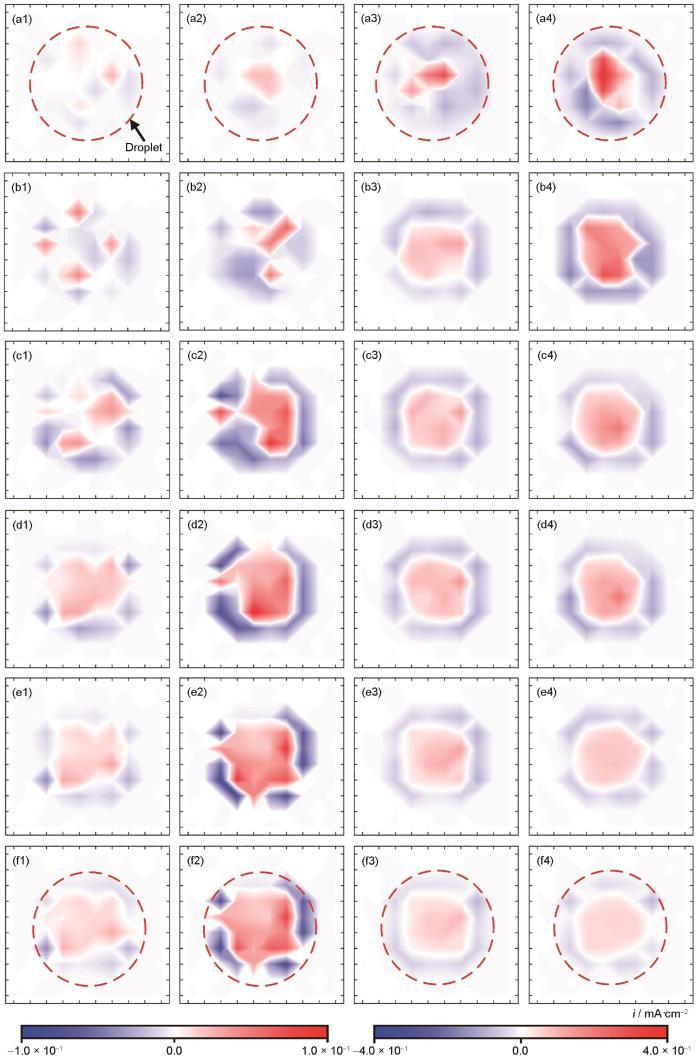
图3展示了不同浓度液滴下碳钢表面的电偶电流分布情况。结果表明,在不同腐蚀阶段,碳钢在不同浓度液滴下的电流分布表现出显著差异。在腐蚀1 min时,0.001 mol/L液滴下碳钢表面的阴阳极电流密度较低,液滴中心区域存在阴极电流分布,而边缘区域则同时存在阳极和阴极电流,且分布较为随机,阴极区与阳极区紧密相邻。随着液滴浓度提升至0.003 mol/L时,阴阳极电流分布发生明显转变:液滴中心区域转变为阳极区,边缘区域则成为阴极区,呈现出典型的Evans环现象[26]。当浓度进一步增加到0.2 mol/L时,液滴中心区域出现明显的主阳极峰,同时阴阳极电流密度均有所提升。浓度为0.5 mol/L时,液滴下的阴阳极分布与0.2 mol/L时相似,中心区域为阳极区,边缘区域为阴极区,且中心区域阳极峰的电流密度值接近0.4 mA/cm2。这些现象表明,在低浓度液滴下,碳钢阴阳极的分布主要受电荷转移速率的控制,阳极倾向于靠近阴极分布。当浓度达到0.003 mol/L时,氧浓差电池成为主导因素,控制着碳钢表面阴阳极电流的分布。具体而言,由于液滴覆盖在碳钢表面,中心区域液滴厚度较大,导致氧气扩散速度较慢,从而引发阳极溶解反应;而边缘区域液滴较薄,氧气扩散速度较快,促进了阴极氧还原反应的发生,形成了明显的氧浓差腐蚀现象。
图3
图3
不同浓度液滴下腐蚀不同时间后Q355b碳钢表面电流分布云图
Fig.3
Cloud maps of current distribution on Q355b carbon steel after corrosion for 1 min (a), 10 min (b), 30 min (c), 60 min (d), 180 min (e) and 300 min (f) under droplets with 0.001 mol/L (a1-f1), 0.003 mol/L (a2-f2), 0.2 mol/L (a3-f3) and 0.5 mol/L (a4-f4) concentration
腐蚀30 min时,0.001 mol/L液滴的中心区域阴极电流密度有所减弱,而边缘区域的阴极电流密度持续增加,同时阳极电流开始向中心区域扩展。对于0.003 mol/L浓度的液滴,其中心阳极区进一步扩展,边缘区域的最大阴极峰靠近中心区的主阳极峰,且阴阳极电流密度均有所增大。在浓度为0.2 mol/L的液滴下,其阴阳极电流分布与电流密度变化趋势与10 min时基本一致。而在浓度为0.5 mol/L的液滴下,阴阳极电流密度继续呈下降趋势。
腐蚀60 min时,0.001 mol/L的液滴开始呈现中心为阳极,边缘为阴极的Evans模型分布特征,主阳极峰靠近主阴极区分布,且阴阳极电流密度无明显变化。当浓度为0.003 mol/L时,液滴中心阳极区的面积增大,但中心阳极区电流密度有所减小,主阳极峰电流密度持续增加,最大电流密度值接近0.1 mA/cm2,且靠近TPB区分布,同时TPB区的阴极电流密度也逐渐上升。浓度为0.2 mol/L时,主阳极峰开始在临近阴极区的位置出现。浓度为0.5 mol/L时,主阳极峰开始向液滴中心转移。由此可见,随着腐蚀的不断进行,在低电导率液滴下,主阳极峰更倾向于在靠近阴极区分布[23];而在高浓度液滴下,主阳极峰转移至液滴中心位置。在腐蚀180 min时,低浓度液滴下,阳极区面积进一步扩展,表面腐蚀过程持续发展;而高浓度液滴下,阴阳极电流分布无见显著变化。在腐蚀300 min时,不同浓度液滴下的阴阳极电流均呈现出中心为阳极区,边缘为阴极区的分布特征。与腐蚀初期相对,低浓度液滴的阴阳极电流密度始终保持在较高水平,而高浓度液滴的电流密度则处于较低水平。
2.3 不同浓度液滴下碳钢表面电位分布
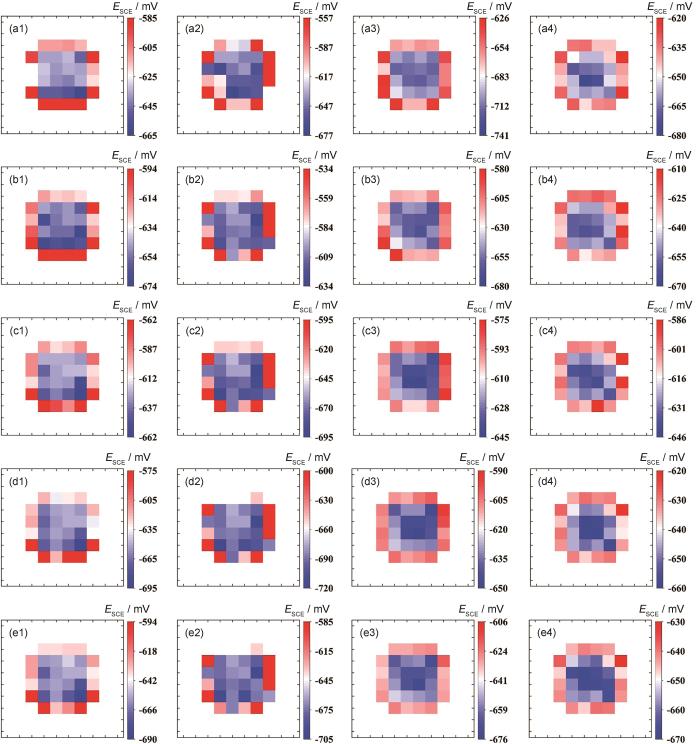
图4展示了碳钢在不同浓度液滴下,于1~5 h这一时间段内各时间点的表面电位分布情况。从图可以看出,液滴覆盖下碳钢表面电化学分布呈现出明显的不均匀性,阳极电位集中于液滴中心区域,而阴极电位则分布于液滴边缘。在浓度为0.001 mol/L的液滴下,阳极区的高电位点主要分布在液滴中心区域,而阳极区的低电位点则紧密靠近阴极区的高电位点分布。当液滴浓度为0.003 mol/L时,其电位分布特征与0.001 mol/L浓度较为相似。而当浓度提升至0.2 mol/L时,阳极区的较低电位点明显倾向于在液滴中心区域分布,并随着腐蚀的进行,液滴阳极区中心位置的阳极点极化程度逐渐增强。当浓度为0.5 mol/L时,阳极区的较低电位点分布与0.2 mol/L浓度下一致,且强度明显增加,随着腐蚀的进行,液滴阳极区中心位置的阳极点极化程度也逐渐增强。
图4
图4
不同浓度液滴下腐蚀不同时间后Q355b碳钢表面电位分布图
Fig.4
Surface potential distribution maps of Q355b carbon steel after corrosion for 1 h (a), 2 h (b), 3 h (c), 4 h (d) and 5 h (e) under droplets with 0.001 mol/L (a1-e1), 0.003 mol/L (a2-e2), 0.2 mol/L (a3-e3) and 0.5 mol/L (a4-e4) concentration
2.4 不同浓度液滴下碳钢表面形貌
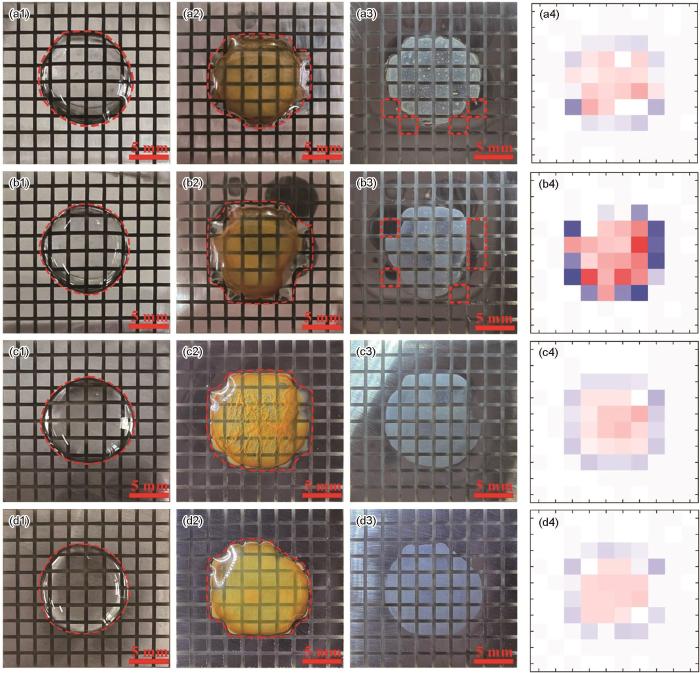
图5呈现了碳钢在浓度分别为0.001、0.003、0.2和0.5 mol/L液滴下,其腐蚀初期、末期、除锈后的形貌图(俯视垂直拍摄),以及腐蚀末期的电流分布图。值得注意的是,腐蚀末期的电流分布与液滴下丝束的位置一一对应,这使得液滴下丝束的阴极区和阳极区得以直观呈现。观察图5可知,随着腐蚀的进行,液滴形状从初始的圆形逐渐向外延展,腐蚀初期和末期的液滴轮廓均以红色虚线标示。研究表明,不同浓度液滴作用下,丝束表面均产生了不同程度的腐蚀,且在除锈后的形貌图中清晰可见腐蚀痕迹。结合腐蚀末期电流分布图来看,在高电导率液滴下,丝束表面的阴极区和阳极区均表现出明显的腐蚀特征;而低浓度液滴下,较大的阴极点未出现明显腐蚀痕迹,丝束表面仍保持光亮状态,这一特征在除锈后的形貌图中以红色虚线标注。根据上述观察结果,阳极区在阳极电流作用下发生腐蚀,而阴极区虽处于电流保护状态,却仍出现腐蚀行为,由此可以推测液滴下碳钢的腐蚀过程是微电池腐蚀与宏电池腐蚀协同作用的结果[19,29]。
图5
图5
不同浓度液滴下腐蚀不同时期的丝束表面形貌图和末期电流分布图
Fig.5
Surface morphologies of the wire beam at the initial (a1-d1), final (a2-d2) and after rust removal (a3-d3) corrosion stages under droplets with 0.001 mol/L (a), 0.003 mol/L (b), 0.2 mol/L (c) and 0.5 mol/L (d) concentration and current distribution maps at the end corrosion stage (a4-d4)
3 讨论
3.1 不同浓度液滴总阳极电流计算
丝束电极在腐蚀的过程中同时发生宏电池腐蚀和微电池腐蚀,虽然宏电池腐蚀电流可通过丝束电极直接测量,但微电池腐蚀电流无法通过直接手段进行测量。总阳极腐蚀电流可通过计算获取,单根电极的总阳极腐蚀电流(Ika)由该电极的宏电池腐蚀电流(Igk)和微电池腐蚀电流(等于Ikc)组成[30],即:
在低浓度液滴下,丝束上的阳极和阴极反应是活化控制的,每根丝束上的腐蚀是均匀的,则可对每根丝束电极应用Butler-Volmer方程[31]:
同理,总阴极腐蚀电流:
由式(
式中,Igk是单根丝束电极电偶电流密度,bak和bck分别是阳极和阴极的Tafel斜率,mV/dec,Tafel斜率代表了电极反应的速率对电位变化的敏感程度,斜率的数值大小反映了氧化或还原过程的速率快慢,斜率越大,反应速率越快。Esys和Ek分别是整个丝束电极耦合的开路电位和单根丝束电极的开路电位,mV。
图6为由
图6
图6
不同浓度液滴下总阳极电流分布图
Fig.6
Total anodic current distribution diagrams under droplets with 0.001 mol/L (a1-e1), 0.003 mol/L (a2-e2), 0.2 mol/L (a3-e3) and 0.5 mol/L (a4-e4) concentration for 1 h (a), 2 h (b), 3 h (c), 4 h (d) and 5 h (e)
图7展示了不同浓度液滴下阳极区电偶电流与总阳极电流的占比情况,该占比直观反映了电偶电流在金属腐蚀过程中的贡献程度。从图中可以清晰看出,低电导率液滴下,阳极区边缘区域主要以宏电池腐蚀为主导;而阳极区中心区域则以微电池为主导。这是由于在低电导率条件下,离子迁移受限,导致阳极区不同部位的离子分布和电荷转移存在差异,从而形成了不同的主导腐蚀类型。在高电导率液滴下,阳极区中心区域宏电池对腐蚀的贡献显著高于边缘区域,这是因为高电导率液滴中存在大量可自由移动的离子,使得阳极与阴极之间的电荷转移更加顺畅,从而加速了宏电池腐蚀反应的进行。随着电导率的进一步升高,离子的迁移速度和数量都显著增加,这进一步强化了宏电池的作用,提升了其对腐蚀的贡献度。
图7
图7
不同浓度液滴下阳极区电偶电流与总阳极电流占比图
Fig.7
Diagrams of the galvanic current in the anodic region and the proportion of the total anodic current under droplets with 0.001 mol/L (a1-e1), 0.003 mol/L (a2-e2), 0.2 mol/L (a3-e3) and 0.5 mol/L (a4-e4) concentration for 1 h (a), 2 h (b), 3 h (c), 4 h (d) and 5 h (e)
3.2 不同浓度液滴碳钢腐蚀机理
图8展示了不同电导率液滴下金属表面腐蚀的机理。高电导率液滴下的金属腐蚀行为符合经典的Evans模型。Evans液滴模型表明,液滴下金属的腐蚀主要受氧浓差电池的影响。在该模型中,液滴呈“边缘厚、中心薄”的经典特征,这种形态使得氧气从液滴边缘向金属表面扩散变得更加容易。在扩散过程中,随着氧气不断到达金属表面,形成了氧浓差梯度。这种氧浓度差异导致电解质溶液中电化学性质的不均匀性,而这种不均匀性正是驱动宏电池腐蚀的关键动力[34]。因此,在高电导率液滴下,液滴中心由于氧浓度相对较低,成为主阳极区,主要的阳极反应是Fe失去电子被氧化,反应式为:Fe → Fe2+ + 2e-。随着电导率的升高,这一阳极过程的强度逐渐增强。而液滴边缘由于氧浓度较高,成为阴极区,主要的阴极反应是O的电子发生还原,反应式为:O2 + 2H2O + 4e- → 4OH-。由于边缘处氧还原速率较高,这不仅促进了宏电池腐蚀的速率,还也加速了阴极区微电池腐蚀的速率。因此,高电导率液滴下,金属的腐蚀是由宏电池和微电池协同作用所引起的。相比之下,低电导率液滴下金属的腐蚀行为与传统的Evans模型存在显著差异。由于液滴电导率极低,液滴中可自由移动的离子数量有限,这极大地阻碍了离子在液滴内的传质过程。这种传质障碍导致阳极反应产生的金属离子在溶液中大量积累,从而抑制了液滴中心阳极反应的进行。为了克服离子传质的障碍,阳极反应倾向于在更有利于离子迁移的区域发生,因此主阳极区倾向于在靠近主阴极区的位置出现。
图8
图8
不同电导率液滴下金属表面腐蚀机理图
Fig.8
Corrosion mechanism diagrams of metals under droplets with 0.001 mol/L (a), 0.003 mol/L (b), 0.2 mol/L (c) and 0.5 mol/L (d) concentration
4 结论
(1) 低电导率液滴(0.001和0.003 mol/L)下碳钢表面的电流强度在腐蚀初期较为微弱,并随着腐蚀的进行逐渐增强;高电导率液滴(0.2和0.5 mol/L)下碳钢表面的电流强度在腐蚀初期达到最大值,但随着腐蚀的进行逐渐减弱。
(2) 在腐蚀初期阶段,0.001 mol/L浓度液滴下碳钢表面的阴阳极电流特征从无序随机状态逐渐转变为Evans模型分布。当浓度提升至0.003 mol/L时,主阳极开始在液滴的中心位置分布,阴极在液滴的边缘分布。并且随着腐蚀的进行,主阳极倾向于靠近主阴极的位置出现。当浓度为0.2和0.5 mol/L时,主阳极始终在液滴中心区域分布。
(3) 液滴的电导率对碳钢的腐蚀有着至关重要的影响。在低电导率液滴作用下,碳钢表面的主阴极区域几乎无腐蚀发生,而阳极边缘区域主要以宏电池腐蚀为主导。在高电导率液滴作用下,碳钢表面的阴极区均出现了腐蚀情况,同时阳极中心区域逐渐演变为以宏电池腐蚀为主导。
参考文献
A synergistic experimental and computational study on CO2 corrosion of X65 carbon steel under dispersed droplets within oil/water mixtures
[J].
Research progress of seawater galvanic coupling corrosion of steels
[J].
钢铁海水电偶腐蚀的研究进展
[J].
Study of correlativity between micro-droplets phenomenon and atmospheric corrosion process
[J].
微液滴现象与大气腐蚀过程相关性研究
[J].
Review of atmospheric corrosivity classification
[J].
大气环境腐蚀性分类分级研究综述
[J].
Corrosion behavior of marine structural steel in tidal zone based on wire beam electrode technology and partitioned cellular automata model
[J].
Study of liquid droplets corrode metal in maritime atmospheric environment
[J].
海洋大气环境下液滴对金属腐蚀
[J].
Atmospheric corrosion of steels for marine engineering and development of weathering steels
[J].
海洋工程用钢的大气腐蚀与耐候钢的发展
[J].
Effect of environmental factors on material transfer in thin liquid film during atmospheric corrosion process in marine environment
[J].
海洋气候大气腐蚀过程环境因素对薄液膜内物质传递的影响
[J].
Initial corrosion behavior of carbon steel and high strength steel in South China sea atmosphere
[J].
碳钢和高强钢在南海大气环境中的初期腐蚀行为研究
[J].
Review of research on mechanical properties of steel structure under atmospheric environment corrosion
[J].
大气环境腐蚀下钢结构力学性能研究综述
[J].
Monitoring the corrosion rate of carbon steel under a single droplet of NaCl
[J].
Atmospheric corrosion of iron under a single droplet: A new systematic multi-electrochemical approach
[J].
An investigation on oxygen reduction under thin electrolyte layer using Kelvin probe reference electrode
[J].
使用Kelvin探头参比电极技术研究液层厚度对氧还原速度的影响
[J].
Wire beam electrode: A new tool for studying localised corrosion and other heterogeneous electrochemical processes
[J].
Sensing electrode inhomogeneity and electrochemical heterogeneity using an electrochemically integrated multielectrode array
[J].
Experimental methods designed for measuring corrosion in highly resistive and inhomogeneous media
[J].
Study of localized corrosion of 304 stainless steel under chloride solution droplets using the wire beam electrode
[J].
The atmospheric corrosion of zinc: The effects of salt concentration, droplet size and dro-plet shape
[J].
Probing top-of-the-line corrosion using coupled multi-electrode array in conjunction with local electrochemical measurement
[J].
Electrochemical formation mechanism of microdroplets on pure iron
[J].
Local electrochemical characteristics of pure iron under a saline droplet II: Local corrosion kinetics
[J].
Atmospheric corrosion local electrochemical response to a dynamic saline droplet on pure iron
[J].
Influences of the three-phase boundary on the electrochemical corrosion characteristics of carbon steel under droplets
[J].
Characteristics of atmospheric environment in China's coastal areas and atmospheric corrosion in typical coastal regions
[J].
我国沿海地区大气环境特征及典型沿海地区大气腐蚀性研究
[J].
Estimation of elfctrochemical kinetic parameters of corrosion processes by weak polarization curve fitting
[J].
由弱极化曲线拟合估算腐蚀过程的电化学动力学参数
[J].
Salt-induced iron corrosion under evaporating sessile droplets of aqueous sodium chloride solutions
[J].
Effect of gas/liquid/solid three-phase boundary zone on cathodic process of metal corrosion
[J].
气/液/固三相线界面区的性质在金属腐蚀阴极过程中的作用
[J].
Research progress on effect of gas/liquid/solid three phase boundary area on cathodic processes
[J].
气/液/固三相线界面区对阴极电化学过程影响的研究进展
[J].
Corrosion of stirrups under different relative humidity conditions in concrete exposed to chloride environment
[J].
Monitoring localized corrosion processes and estimating localized corrosion rates using a wire-beam electrode
[J].
Influence of spreadability of seawater droplet on electrochemical characteristics of carbon steel
[J].
海水液滴铺展因子对碳钢表面电化学特性的影响
[J].
Corrosion behavior of Q235 in simulated natural environment by electrochemical technology
[J].
Q235钢在模拟自然环境下失效行为的电化学研究
[J].
Understanding the effects of electrode inhomogeneity and electrochemical heterogeneity on pitting corrosion initiation on bare electrode surfaces
[J].