添加缓蚀剂是抑制发电机内冷水中铜导线腐蚀的一种经济、有效的手段,通常采用的缓蚀剂是苯并三唑(BTA)[3]。在微酸性、中性环境中,BTA在铜表面易于生成Cu(I)BTA复合物,这是一种无定形晶体。苯并三唑(BTA)在铜表面也会产生包括第1层的[Cu-BTA](内层)和第2层吸附在内层的BTA[4,5]表面保护膜。Grillo等[6]研究表明,在相对高温的环境中BTA仍然能与铜离子保持1∶1络合比,络合物具有较高的分子稳定性,成膜极其牢固。连宇博等[7]通过BTA研发的纳米缓蚀胶囊证实了BTA对Cu的长效保护,Ryu等[8]也证实了经过BTA处理的铜表面接触角由26°提升至63°,用去离子水冲洗Cu表面后,[Cu-BTA]复合物层仍存在。随着运行时间的延长,[Cu-BTA]膜脱落产生沉积,造成发电机空芯铜导线的堵塞[9]。从分子结构上讲,1, 2, 4-三氮唑(TAZ)是BTA的理想替代物[10]。首先,它们含有三唑环,对Cu有特异的亲和作用。另一方面,和BTA相比,TAZ分子较小,钝化能力弱,在Cu表面形成的缓蚀膜更易于清理[4,10,11]。Yin等[12]通过理论计算和电化学测试的方式验证了TAZ与BTA有着相似的抑制机制。Rolland等[13]也观察到在高氯环境下TAZ具有类似BTA的阳极抑制效能。刘萍等[14]通过摩擦磨损实验表明,铝合金化学机械抛光过程中TAZ缓蚀膜比BTA缓蚀膜更易被去除。
本工作利用失重实验和电化学测量考察了TAZ作为缓蚀剂在转子冷却水模拟溶液中对Cu的缓蚀作用,通过椭偏仪光学测量其在铜表面的成膜厚度,采用接触角测试、荧光测试考察其表面成膜状态。通过Dmol3模块对TAZ分子结构进行几何优化,讨论TAZ的缓蚀机理。
1 实验方法
所用试片为纯Cu(99.9%),用不同规格的砂纸(800#、1200#、2000#)打磨,去离子水洗涤,乙醇超声清洁,氮气吹干后放干燥器中待用。1, 2, 4-三唑(TAZ)缓蚀剂为化学纯试剂,采用超纯水为模拟转冷水溶液(pH = 7.0、电导率 ≤ 10 μS·cm-1),每次实验前重新配置,并对浸泡实验前后的溶液溶氧量、pH、电导率进行测试记录。
通过溶液分析法测试40℃下不同TAZ浓度时的缓蚀效率。实验试片选用规格为500 mm × 250 mm × 3 mm的纯铜片,将每组3个平行样悬挂在未加和添加缓蚀剂的100 mL转冷水模拟溶液中,并将其放置在真空干燥箱中120 h后取出试片,使用(1∶1)盐酸溶液对浸泡实验后的模拟溶液调节至pH = 2后,采用孔径为0.22 μm有机滤膜过滤,用TAS-990型原子吸收分光光度计检测溶液中铜离子含量[15]。
采用 F-7000荧光分光光度计,分别对浸泡实验前后的转冷水模拟溶液进行荧光测试,以考察TAZ与Cu配位反应及在溶液中的聚集情况。
电化学测试采用660I型电化学工作站,三电极系统,工作电极为纯铜电极(1 cm2),参比电极为饱和甘汞电极,辅助电极为铂片电极。开路电位(OCP)-时间曲线的时间范围设置为0~600 s。电化学阻抗谱(EIS)测量的频率范围为105~10-2 Hz,正弦交流信号振幅为10 mV,用Zsimpwin软件模拟实验结果。极化曲线的扫描电位为范围为OCP ± 0.3 V,扫描速率为1 mV·s-1。
将腐蚀浸泡实验后的Cu片烘干后,在SE-VE-L型椭偏仪上测试TAZ成膜厚度。利用JC2000CS接触角测量仪测量接触角,使用微量注射器摄取模拟转冷水溶液20 μL滴在已预处理后的Cu片表面上,待液体在Cu片表面上稳定后捕获图像,测量此时的接触角。
采用广义梯度近似(GGA)的(DFT)方法,由Material Studio(MS,2020版)软件的DMol3模块计算量子化学参数。首先,通过振动分析对TAZ分子结构进行优化,以确保测试的分子达到势能的最小点。然后计算并执行相应的量子化学描述符,包含轨道能(EHOMO、ELUMO和EGap)和静电势(ESP)。使用CASTEP模块计算了TAZ吸附在Cu表面上的态密度、差分电荷密度和功函数。使用Forcite模块研究缓蚀剂TAZ在Cu表面上的吸附行为。研究对象是四层Cu(111)、一个缓蚀剂分子和500个水分子。在40℃下进行,使用COMPASSⅢ力场和规范系综(NVT),时间步长为1.0 fs,模拟时间为10 ps。在计算过程中,所有金属原子都被固定,保持吸附分子与金属表面自由相互作用。 通过吸附定位模块研究了缓蚀剂的吸附行为。
2 结果与讨论
2. 1 腐蚀浸泡实验
式中,v0和v分别为不含和含缓蚀剂的溶液中Cu离子释放速率(μg/cm-2·h-1),C(Cu)为溶液中Cu离子浓度(μg/L),L为容器中溶液体积(L),t为试样在溶液中的浸泡时间(h),A为试样表面积(cm2),ηw为缓蚀率(%)。
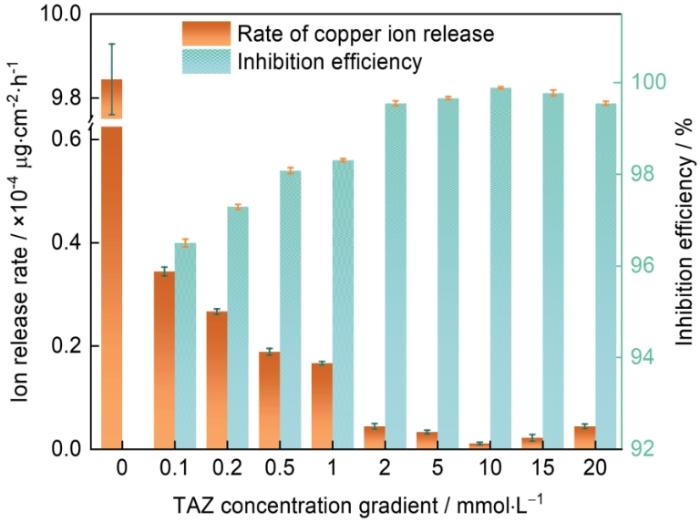
图1为Cu片在40℃模拟转冷水中浸泡120 h的腐蚀速率。在不加入缓蚀剂时下,腐蚀速率为9.84 μg·cm-2·h-1,而在加入10 mmol/L TAZ后腐蚀速率降低至0.011 μg·cm-2·h-1,且平行样差异不大。可以看出,TAZ浓度从2 mmol/L起对转冷水模拟溶液中铜均有较好的缓蚀性能,缓蚀效率在实验浓度范围内均超过了99%,在TAZ浓度为10 mmol/L时达到最佳,且后续随着TAZ浓度的进一步提高缓蚀性能出现下降趋势。
图1
图1
Cu在40℃含不同浓度TAZ的模拟转冷水中静态腐蚀实验数据
Fig.1
Ion release rates of copper in the coolant aqueous solutions containing different concentrations of TAZ at 40oC and inhibition efficiencies of TAZ
TAZ使用前后水质变化如图2所示。由图可见,TAZ的加入,导致溶液pH值略有下降,浸泡后溶液的pH值进一步下降。浸泡前的溶氧测试结果平均值为8.48 mg/L,浸泡后溶液溶氧量显著下降,这与溶液中Cu的氧化反应有关。不同浓度TAZ溶液中Cu片浸泡后溶液的溶氧量变化不大。溶液中的电导率随TAZ的加入呈下降趋势,但在浸泡后溶液电导率随TAZ使用浓度的上升,逐渐趋于稳定。
图2
图2
Cu在不同浓度TAZ的转冷水溶液浸泡前后的pH值、溶氧量和电导率
Fig.2
pH and dissolved oxygen values (a) and conductivities (b) of Cu before and after 120 h immersion in the coolant aqueous solutions containing different concentrations of TAZ
图3
图3
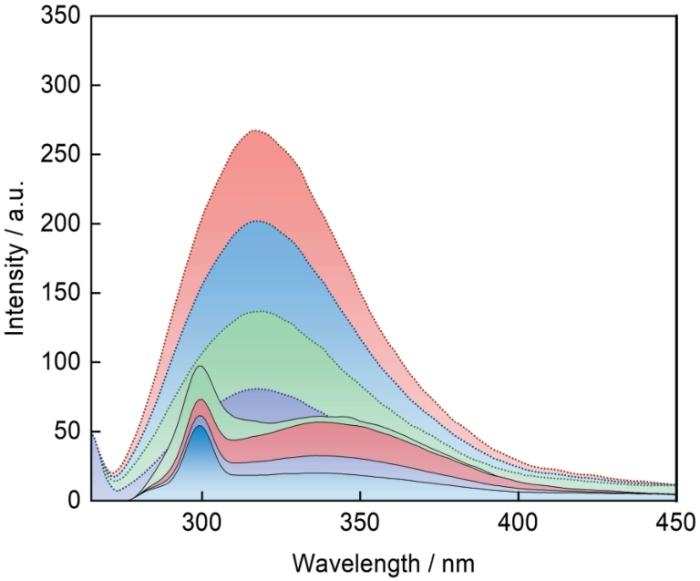
Cu在含不同TAZ浓度的模拟内冷水中浸泡实验前后的荧光光谱
Fig.3
Fluorescence emissions of Cu before and after immersion in the stimulated cooling waters containing different concentrations of TAZ
2.2 电化学测量
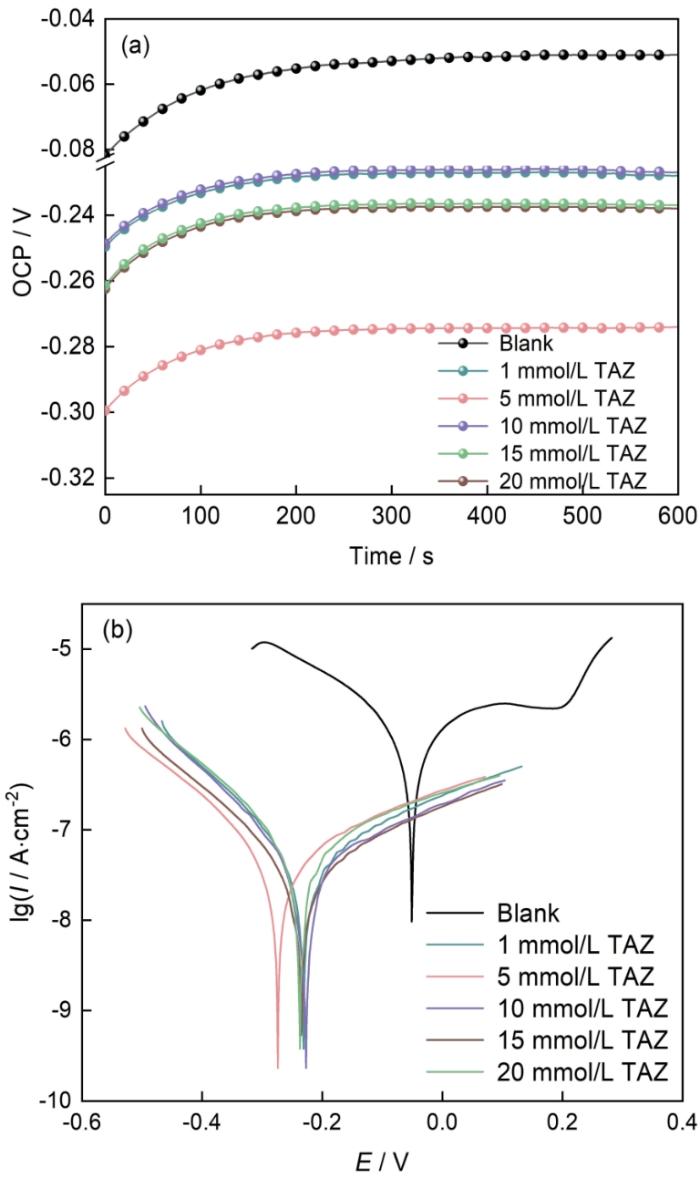
图4为铜电极在添加不同浓度TAZ的室温模拟冷却水中的OCP变化曲线和极化曲线。将铜电极浸入模拟装冷水溶液中10 min,以获得稳定的OCP。TAZ浓度对Cu动电位极化特性的影响如图4a所示,OCP在一定时间内能达到一个接近稳定的值。通过Tafel图来充分解释OCP变化的机理,可以看出,相对于空白溶液中的电极,添加TAZ溶液中的铜电极腐蚀电流密度Icorr值均降低,从Tafel斜率看,缓蚀剂对铜电极的阳极反应和阴极反应抑制作用显著,缓蚀剂存在导致铜电极的自腐蚀电位Ecorr负移,TAZ在模拟内冷水介质中对铜来说是阴极型缓蚀剂,这与高氯介质中BTA缓蚀剂的阳极作用机理有所不同[18]。所得极化曲线参数见表1。
图4
图4
Cu在室温含不同浓度TAZ的模拟冷却水中的开路电位和极化曲线
Fig.4
OCP (a) and polarization curves (b) of copper in simulated cooling waters with different concentrations of TAZ at room temperature
表1 铜在添加不同浓度TAZ的室温模拟冷却水中的极化曲线参数
Table 1
C mmol·L-1 | Ecorr V vs. SCE | Icorr μA·cm-2 | -βc mV·dec-1 | βa mV·dec-1 | ηi % |
|---|---|---|---|---|---|
| Blank | -0.051 | 1.450 | 176.7 | 318.2 | - |
| 0.5 | -0.193 | 5.074 × 10-2 | 129.9 | 211.0 | 96.5 |
| 1 | -0.231 | 4.390 × 10-2 | 132.8 | 216.4 | 97.0 |
| 5 | -0.274 | 4.138 × 10-2 | 140.5 | 226.7 | 97.1 |
| 10 | -0.227 | 2.459 × 10-2 | 126.8 | 213.0 | 98.3 |
| 15 | -0.235 | 3.396 × 10-2 | 139.4 | 218.4 | 97.7 |
| 20 | -0.237 | 4.200 × 10-2 | 135.9 | 222.8 | 97.1 |
缓蚀效率可以用
式中:ηi代表缓蚀效率,其中Icorr, 0和Icorr分别表示铜试样的未受抑制电流密度和受抑制电流密度。
图5
图5
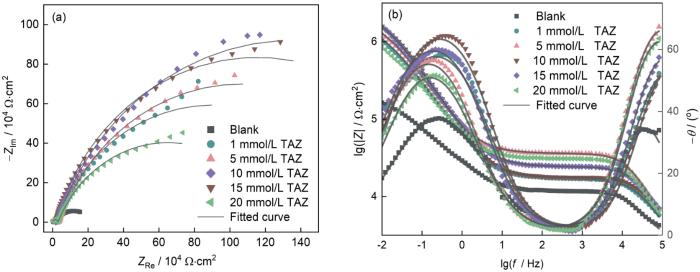
铜电极在含有不同浓度TAZ的模拟内冷水中的电化学阻抗谱
Fig.5
Nyquist (a) and Bode (b) plots of copper electrode in the simulated cooling solutions with different concentrations of TAZ
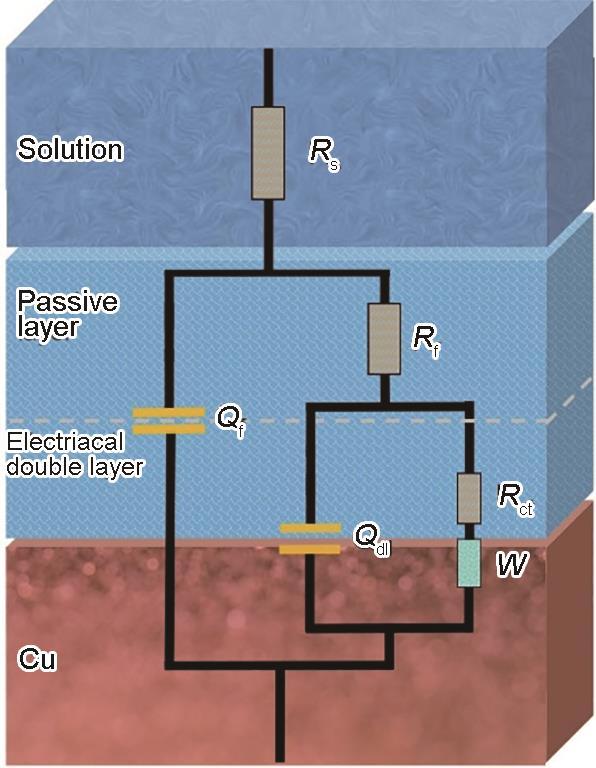
采用图6所示的等效电路对铜电极的阻抗谱进行拟合,其中Rs是溶液电阻,Rf是缓蚀剂的膜电阻、Rct是电荷转移电阻,Qf和Qdl是分别为铜表面形成的钝化膜电容和铜电极/膜界面的双电层电容。由于铜电极表面的非理想电容行为,这些元件将用于替代膜电容(Cf)和双层电容(Cdl)。
其中,恒定相角元件(CPE)采用Q进行表示,Y为导纳,j是虚根,w为扰动信号的角频率(w = 2πf,f为频率,Hz),n为指数项。
图6
极化电阻(Rp)可以约等于Rf和Rct的和,缓蚀效率(ηE)可以用
表2 铜电极在含有不同浓度TAZ的模拟内冷水中的电化学阻抗谱拟合参数
Table 2
TAZ mmol·L-1 | RS kΩ·cm2 | Qf | Rf kΩ·cm2 | Qdl | Rct kΩ·cm2 | Rp kΩ·cm2 | X2 | ηE % | ||
|---|---|---|---|---|---|---|---|---|---|---|
Y0 nS⋅s n ·cm-2 | n | Y0 μS·s n ·cm-2 | n | |||||||
| Blank | 2.565 | 3.010 | 0.91 | 9.022 | 15.45 | 0.64 | 206.1 | 215.122 | 1.28 × 10-3 | - |
| 1 | 1.119 | 1.960 | 0.87 | 15.81 | 4.560 | 0.75 | 1771 | 1786.81 | 1.80 × 10-3 | 88.0 |
| 5 | 0.849 | 0.805 | 0.92 | 35.21 | 3.954 | 0.76 | 2052 | 2087.21 | 7.87 × 10-4 | 89.7 |
| 10 | 1.150 | 1.222 | 0.89 | 23.19 | 3.452 | 0.77 | 2659 | 2682.19 | 1.27 × 10-3 | 92.0 |
| 15 | 1.095 | 1.329 | 0.88 | 16.56 | 3.247 | 0.81 | 2269 | 2285.56 | 9.83 × 10-4 | 90.6 |
| 20 | 1.086 | 0.999 | 0.92 | 28.37 | 4.568 | 0.76 | 1621 | 1266.71 | 6.87 × 10-4 | 87.0 |
式中,Rp,0和Rp分别为Cu在不含缓蚀剂和含有缓蚀剂的转冷水模拟溶液中的极化电阻。
可以看出,随着TAZ浓度的增加,Rct和Rp的值显著增加,表明缓蚀剂加入显著抑制了铜电极上的腐蚀反应[21]。此外,所有的电容值相对于空白溶液的电容值显著降低。这表明,缓蚀剂取代了电极表面吸附的水,在Cu表面形成缓蚀剂吸附膜。当TAZ浓度等于10 mmol/L时,缓蚀效率达到最大值为91.98%。当TAZ浓度大于15 mmol/L时,Rct和Rp减小,表明此时TAZ的缓蚀作用有所降低。EIS的结果与极化曲线的结果一致。
2.3 吸附等温式
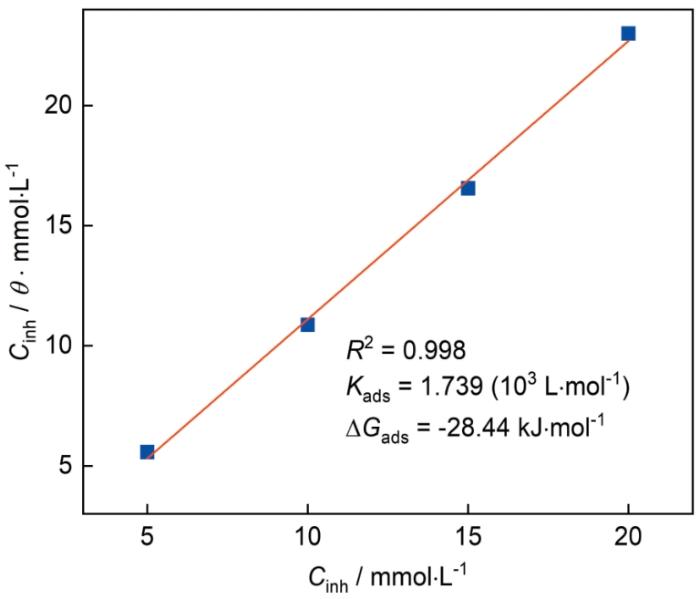
为了确定TAZ在铜表面的吸附类型,采用EIS数据对进行各种Langmuir、Frumkin、Temkin等吸附等温线模型拟合。结果表明,TAZ的吸附过程服从Langmuir单层吸附。Langmuir等温线方程如下所示[22]:
式中,Cinh表示缓蚀剂的浓度,θ表示表面覆盖率。可以用缓蚀效率近似代替缓蚀剂在金属表面的覆盖度θ,表示为ηE/100,Kads表示平衡常数。标准吸附自由能ΔGads可通过Kads值使用以下方程估算[23]:
式中,R和T分别表示摩尔气体常数和绝对温度。
图7
图7
TAZ的Langmuir吸附等温线及相关参数
Fig.7
Langmuir adsorption isotherm of TAZ and relevant parameters
2.4 表面分析实验
通过椭偏仪测量在不同浓度TAZ的模拟内冷水溶液中浸泡后Cu表面膜的厚度,如表3所示。可以看出,在TAZ浓度为2 mmol/L时,样品表面膜厚度为8.78 nm。随着TAZ浓度的提升,表面缓蚀膜的厚度总体变化不大。
表3 TAZ在样品表面的成膜厚度及参数
Table 3
TAZ mmol·L-1 | Goodness of Fitting (GOF) | Mean Square Error (MSE) | Thickness of TA2 nm |
|---|---|---|---|
| 2 | 0.99999 | 2.4642 | 8.78 |
| 5 | 0.99996 | 5.1166 | 7.86 |
| 10 | 0.99995 | 5.6480 | 8.64 |
| 15 | 0.99982 | 10.588 | 8.76 |
| 20 | 0.99936 | 6.5912 | 8.87 |
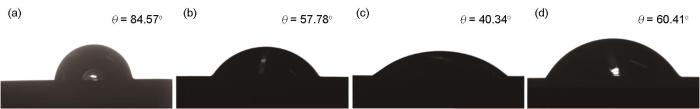
Cu在含有不同浓度TAZ的模拟内冷水浸泡后水的接触角见图8。在不含有缓蚀剂的模拟内冷水中,铜表面的接触角为84.57°;TAZ的加入导致Cu表面的接触角有所降低,这表明TAZ的加入改变了铜表面的润湿性能,使得Cu表面的亲水性有所增加。
图8
图8
铜在含有不同浓度TAZ的模拟内冷水浸泡后的水接触角
Fig.8
Shapes of water drops on Cu immersed in the stimulated cooling waters containing 0 mmol/L (a), 5 mmol/L (b), 10 mmol/L (c) and 15 mmol/L (d) TAZ
2.5 理论计算与缓蚀机理
采用量子化学计算来进一步探索TAZ的活性位点和缓蚀机制。图9显示了TAZ的优化分子结构、ESP、HOMO(最高占有的分子轨道)和LUMO(最低未占有的分子轨道)。
图9
图9
TAZ量子化学计算
Fig.9
Quantum chemical calculations of TAZ molecule structure:(a) optimal structure, (b) ESP, (c) HOMO, (d) LUMO
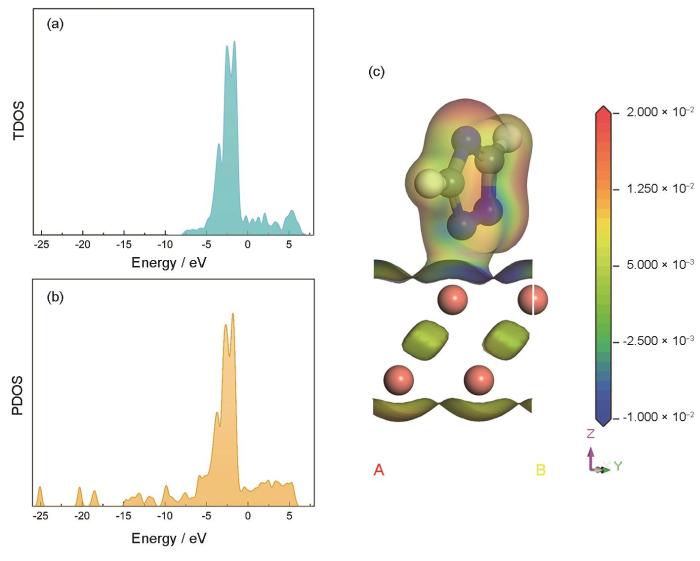
态密度(DOS)可以理解成电子在某一能量范围的分布情况,通过能量的高低分布在不同原子轨道上,反映出原子间的相互作用情况,通过计算未吸附TAZ的总态密度(TDOS)及吸附TAZ分子的投影态密度(PDOS)图分析分子间化学键的成键情况。从图10中可以看出,PDOS图由两部分态密度组成,分别是对应成键分子轨道的低能部分态密度和对应于反键分子轨道的高能部分态密度。根据PDOS图来判断,原子轨道发生 “共振”,形成波峰.如果成键作用增强,那么成键分子轨道会左移.图10a与图10b相比,在-24~-22 eV,-20~-15 eV和-12~-8 eV之间均有“共振”,产生了新的低强度的波峰。可以推测是TAZ分子中的N原子与Cu原子形成了配位键。为了验证N原子与Cu原子之间确实存在这样的吸附行为,通过Cu(111)表面与TAZ复合模型的电荷密度分布来分析。如图10c所示为差分电荷密度,N原子周围电荷密度大,而Cu原子周围电荷密度小,N原子和Cu原子通过配位键相互结合,进一步证实其通过TAZ与Cu原子的相互作用形成保护膜。
图10
图10
Cu表面未吸附TAZ的总态密度和吸附TAZ的投影态密度及体系的差分电荷密度
Fig.10
TDOS of pure copper surface (a), PDOS of copper surface with TAZ molecular (b) and Electronic density profile of copper surface and TAZ molecule composite model (c)
进一步计算Cu(111)表面吸附TAZ前后的功函数,以与其缓蚀能力联系起来。功函数(
其中,Vvac是真空区的静电势,Ef是费米能级。使用5 nm作为真空计算功函数,以确保我们的结果与真空度的收敛。结果表明,加入TAZ后的功函数为4.63 eV,未加入时的功函数为4.621 eV。显然,TAZ分子的缓蚀能力源自质子化的形式,因其具有相对高的功函数。DFT模拟预测TAZ的吸附是化学吸附。质子化形式导致Cu表面功函数得到一定提升,这是其缓蚀作用的根源。
图11
图11
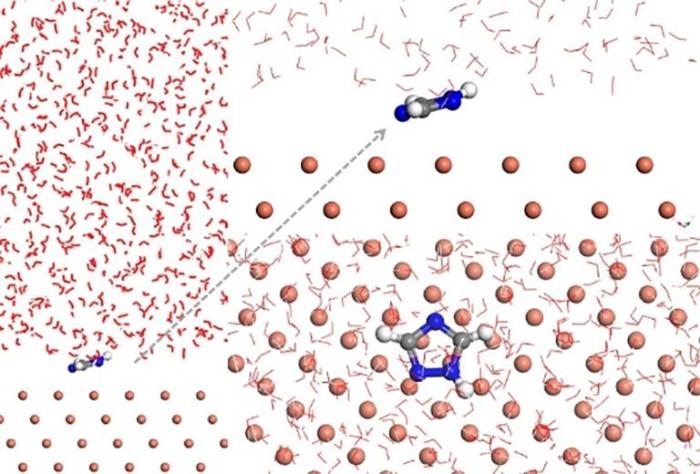
TAZ吸附的分子动力学模拟
Fig.11
Molecular dynamic simulated equilibrium configuration of TAZ adsorption on Cu surface
TAZ在Cu表面上的吸附能计算如下[20]:
式中,Ebinding是分子与Cu表面的结合能;Etotal是整个模拟系统的总能量;Esurface是Cu基体和H2O分子的能量;Eorgan是TAZ分子的能量。计算得出相应的吸附能为-254.4 kJ/mol,表明TAZ在铜合金表面具有较好的吸附作用[28],有效地抑制模拟内冷水溶液中Cu的腐蚀。
3 结论
考察了TAZ对Cu在模拟转冷水溶液中的缓蚀作用。结果表明,TAZ的加入显著降低了Cu在模拟内冷水溶液中的腐蚀速率,对内冷水的水质变化影响不显著。TAZ是一种阴极缓蚀作用为主的混合型缓蚀剂,电化学阻抗实验表明在10 mmol/L浓度条件下TAZ最佳缓蚀率达92.0%。TAZ可以自发吸附在铜表面,符合Langmuir吸附等温式。这对于抑制调相机转冷水中空芯铜导线腐蚀的缓蚀剂应用具有指导意义。
参考文献
Temperature warning and fault diagnosis of air cooler of hydro-generator
[D].
水轮发电机空气冷却器温度预警及故障诊断研究
[D].
Optimization and transformation of rotor cooling water system of 300MW double water internal cooling generator unit
[J].
基于300MW双水内冷发电机组转子冷却水系统优化改造
[J].
Analytical study of copper corrosion inhibitors BTA and MBT in circulating water
[D].
循环水中铜缓蚀剂BTA和MBT的分析研究
[D].
The relationship between the inhibition performances of three benzo derivatives and their structures on the corrosion of copper in 3.5 wt.% NaCl solution
[J].
Kinetics of corrosion inhibition of benzotriazole to copper in 3.5% NaCl
[J].
Copper adatoms mediated adsorption of benzotriazole on a gold substrate
[J].
Inhibition behavior of a nano-corrosion inhibitor capsule prepared from MOFs and BTA for copper
[J].
一种基于MOFs与BTA的纳米缓蚀胶囊对铜的缓蚀行为研究
[J].通过水热法合成了结构立体、具有明显孔道结构的MOF-5。进一步通过负压法将苯并三氮唑负载进MOF-5形成BTA@MOF缓蚀胶囊。采用TEM、SEM、FT-IR、XRD以及电化学测试等手段对BTA@MOF的结构以及缓蚀性能进行表征评价。结果表明:缓蚀剂分子成功负载进MOF-5内部孔道,制备的缓释剂胶囊具有缓慢释放的特性,能够有效抑制铜的腐蚀。
Theoretical validation of inhibition mechanisms of benzotriazole with copper and cobalt for CMP and post-CMP cleaning applications
[J].
Analysis and treatment measures to the TBM-160-2 water cooled generator rotor failure
[J].
TBM-160-2型水冷式发电机转子故障的原因分析及处理对策
[J].
Effect of 1, 2, 4-triazole and benzotriazole on chemical-mechanical polishing of 316L stainless steel
[J].
1, 2, 4–三氮唑和苯并三氮唑对316L不锈钢化学机械抛光的影响
[J].
Research progress of 1, 2, 3-benzotriazole as a corrosion inhibitor for copper
[J].
1, 2, 3-苯并三氮唑铜缓蚀剂的研究进展
[J].
Theoretical and electrochemical analysis on inhibition effect of benzotriazole and 1, 2, 4-triazole on cobalt surface
[J].
Intercalation of 1, 2, 4-triazole in methanol modified-kaolinite: Application for copper corrosion inhibition in concentrated sodium chloride aqueous solution
[J].
Anti-corrosion mechanisms of 1, 2, 4-triazole and benzotriazole on the aluminum during chemical mechanical polishing process
[J].
铝化学机械抛光中1, 2, 4-三唑和苯并三氮唑的缓蚀机制
[J].
Determined copper in aqueous solution by flame atomic absorption spectrometry
[J].
火焰原子吸收光谱法测定水样中铜离子
[J].
Corrosion behavior of T2 copper in static artificial seawater
[J].
T2紫铜在静态人造海水中的腐蚀行为
[J].
Study on synthesis and application of 1.2 4-triazole derivatives
[D].
1, 2, 4-三唑衍生物的合成及应用研究
[D].
Experimental and theoretical studies for mild steel corrosion inhibition in 1M HCl by two new benzothiazine derivatives
[J].
Evaluation of the inhibitive effect of benzotriazole on archeological bronze in acidic medium
[J].
Corrosion inhibition performance of chromone-3-acrylic acid derivatives for low alloy steel with theoretical modeling and experimental aspects
[J].
A combined experimental and theoretical study of the inhibition effect of three disulfide-based flavouring agents for copper corrosion in 0.5 M sulfuric acid
[J].
Potential role of a novel green eco-friendly inhibitor in corrosion inhibition of mild steel in HCl solution: detailed macro/micro-scale experimental and computational explorations
[J].
Insights into triazole derivatives as potential corrosion inhibitors in CMP process: experimental evaluation and theoretical analysis
[J].
Molecular structure optimization design of inhibitors based on frontier orbitals theory
[J].
The inhibition mechanism and adsorption behavior of three purine derivatives on the corrosion of copper in alkaline artificial seawater: structure and performance
[J].
(E)-2-styryl-1H-benzo[d] imidazole as novel green corrosion inhibitor for carbon steel: experimental and computational approach
[J].
Molecular dynamics simulation of the adsorption behavior of amino acid corrosion inhibitor on Cu(001) surface
[J].
The effect of structural properties of benzo derivative on the inhibition performance for copper corrosion in alkaline medium: experimental and theoretical investigations
[J].