相比于火力发电,低温余热发电零消耗、零排放、零污染。但低温余热发电机组的蒸汽温度低、压力小、盐分高等,造成了其转动部件 (如汽轮机转子) 表面更容易形成一层液膜[4,6]。此外,蒸汽中的氧气、腐蚀性杂质盐 (如NH4H2PO4) 等又会溶于液膜中而形成强电解质溶液。再加上,低温余热发电机组频繁启停机,造成了其汽轮机转子表面的液膜失而复得,得而复失,即使汽轮机转子材料处于干湿交替状态。黄涛等[7]将材料在干湿交替状态中的腐蚀过程分为表面浸润阶段、表面完全润湿阶段、表面干燥阶段,其中表面干燥阶段为决定性步骤。在表面干燥阶段,受液膜影响,氧供应充分,并且腐蚀性杂质盐 (如NH4H2PO4) 也会发生富集,再加上生成的腐蚀产物起到了强烈的阴极去极化作用,诱发汽轮机转子材料产生腐蚀损伤,并给低温余热发电机组的安全运行带来巨大隐患[7-11]。
目前,关于干湿交替环境状态对材料腐蚀行为影响的研究更多集中于海洋干湿交替环境中低合金钢或碳钢的腐蚀行为研究[8-13]。张庆普等[11]研究了模拟海洋干湿交替环境中干湿比对Q235钢腐蚀行为的影响,表明随着干湿比的增大,Q235钢的腐蚀速率增大,但增大幅度越来越小,即腐蚀速率存在极大值。Li等[12]研究了模拟海洋干湿交替环境中相对湿度对Corten-A合金钢腐蚀行为的影响,表明相对湿度是影响薄液膜厚度和材料腐蚀行为的关键因素之一;Hao等[13]研究了模拟海洋干湿交替环境对E690合金钢应力腐蚀行为的影响,表明E690合金钢在干湿交替条件下具有较高的应力腐蚀敏感性,此外,材料还遵循氢脆机理;然而,汽轮机转子常见材料在干湿交替的含NH4H2PO4溶液环境中的腐蚀行为鲜有报道。
结合机组运行介质和实际情况,本文选取2Cr-1Ni-1.2Mo-0.2V钢和2Cr-4Ni-0.4Mo-0.1V钢作为研究对象,120 mmol/L 的NH4H2PO4溶液作为研究介质,通过激光共聚焦显微镜 (CLSM) 分析不同干湿比条件下材料表面的腐蚀形貌[14];采用X射线衍射仪 (XRD)、X射线光电子能谱 (XPS) 分析腐蚀产物膜的组成;利用失重法研究干湿比对材料腐蚀速率的影响;利用开路电位、电化学阻抗谱等电化学测量方法研究干湿比对材料电化学性能的影响。探讨了相关的腐蚀机理,研究结果可为利用NH4H2PO4生产行业产生的低温余热资源发电所用装备的开发及其腐蚀防护提供理论依据及数据支持。
1 实验方法
实验钢为2Cr-1Ni-1.2Mo-0.2V钢 (IR钢) 和2Cr-4Ni-0.4Mo-0.1V钢 (2R钢),其成分 (质量分数,%) 分别为:C 0.28,Si 0.066,Mn 0.63,S 0.0053,P 0.0013,Cr 2.23,Mo 1.17,Ni 0.98,V 0.21,Al 0.011,Cu 0.048,As 0.006,Fe余量;C 0.24,Si 0.015,Mn 0.035,S 0.0035,P 0.001,Cr 1.63,Mo 0.41,Ni 3.61,V 0.093,Al 0.0037,Cu 0.016,As 0.0082,Fe余量。
利用线切割的方式将实验钢1R钢和2R钢加工成50 mm×20 mm×4 mm的失重试样和10 mm×10 mm×10 mm的电化学试样,电化学试样采用环氧树脂对其进行真空冷镶。以上所有试样均利用SiC水性砂纸打磨至800#,随后将试样放入无水乙醇中超声处理5 min,以去除试样表面残留的SiC颗粒,最后用去离子水清洗试样表面,无水乙醇脱除残留水分、冷风吹干放入干燥皿中待用。其中,用于腐蚀失重测量的试样在干燥皿中静置24 h后称重 (精确至0.1 mg)。此外,对腐蚀失重后的试样除锈所用的酸洗液由500 mL盐酸 (HCl,ρ=1.19 g/mL)+5 g 1,3-二丁基-2-硫脲+500 mL去离子水配置而成。酸洗后,迅速用去离子水、无水乙醇清洗试样,冷风吹干,放于干燥皿中静置24 h后称重 (精确至0.1 mg)。并用
其中,R为平均腐蚀速率 (g·m-2·h-1);M和Mt为试样除膜前后质量 (
实验介质为120 mmol/L NH4H2PO4溶液,通过纯度为99%的NH4H2PO4药剂和去离子水混合而成。全浸 (dry/wet=0) 实验在烧杯中进行,外界环境温度控制在 (25±2) ℃,实验时长为21 d;而干湿交替实验在手动周浸实验箱中进行,控制温度为 (25±2) ℃,相对湿度为 (55±5)%。其中,干湿交替实验以1 d为一个循环,设置3种干湿比:干燥/浸没时间分别为6 h/18 h (dry/wet=1/3)、12 h/12 h (dry/wet=1)、18 h/6 h (dry/wet=3),干湿交替实验共进行了21个循环。
随后,采用LEXT-OLS5000激光共聚焦显微镜 (CLSM) 观察两种钢在上述4种环境中的腐蚀形貌;此外,刮取两种钢在上述4种环境中生成的腐蚀产物粉末,并使用X射线衍射仪 (XRD,Bruker D8 Advance) 对其进行物相分析 (采用Cu靶材,扫描角度范围为10°~90°)。然后选取两种钢在干燥/浸没时间为6 h/18 h (dry/wet=1/3) 条件下生成的腐蚀产物膜进行XPS分析,XPS测试在Thermo Scientific K-Alpha X射线光电子能谱仪上进行,所用光源为单色AlKa (hν=1486.6 eV),工作电压为12 kV,并用C 1s (284.8 eV) 为校准峰进行荷电校正,最后利用XPS PEAK41软件处理数据。另外,利用失重法计算两种钢在上述4种环境中的腐蚀速率。
电化学实验在PARSTAT4000型电化学工作站上进行,采用三电极体系,电解质溶液为120 mmol/L NH4H2PO4溶液,1R钢或2R钢为工作电极,铂片为辅助电极,饱和甘汞电极 (SCE) 为参比电极,测试温度为 (25±2) ℃。先测900 s开路电位,待开路电位稳定后再测电化学阻抗谱 (EIS),电化学阻抗谱测试频率为105~10-2 Hz,交流扰动电压为5 mV,并使用ZSimDemo软件对其数据进行拟合分析,每个测试点设置6个平行试样。
2 结果与讨论
2.1 腐蚀速率
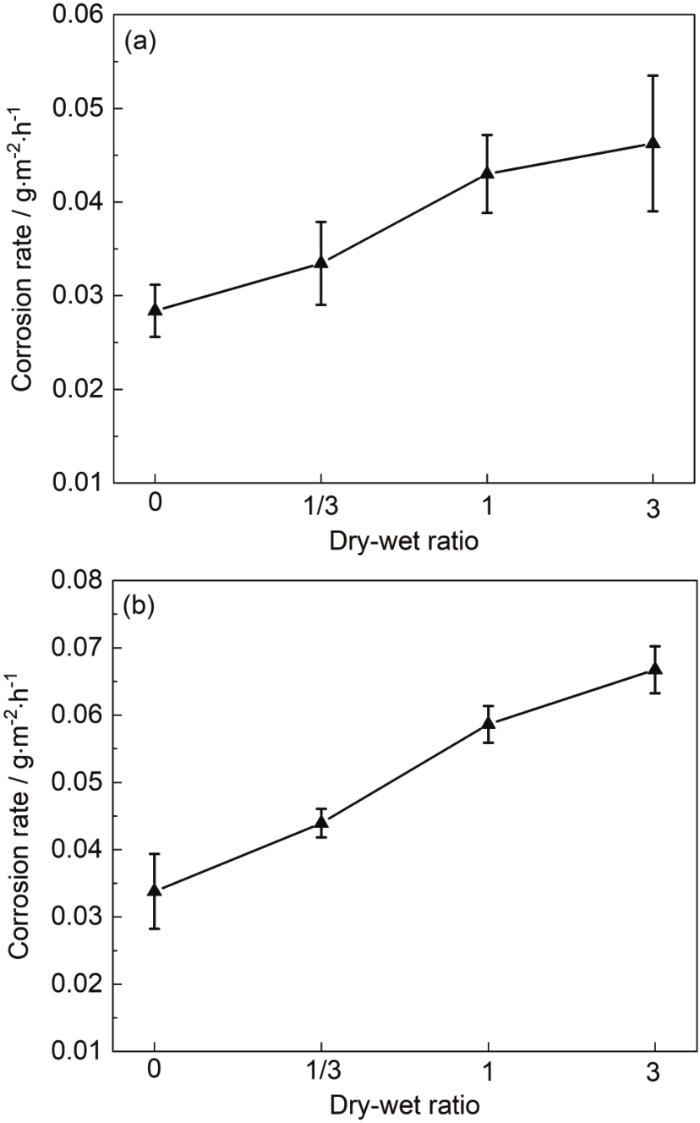
1R钢和2R钢在不同干湿比条件下的120 mmol/L NH4H2PO4溶液中的平均腐蚀速率见图1。从图1a中可知,1R钢在干湿比为0 (全浸) 条件下的腐蚀速率为0.028 g/(m2·h),而其在干湿比为1/3、1、3条件下的腐蚀速率分别为0.033、0.043和0.046 g/(m2·h),即1R钢的腐蚀速率随干湿比增大而增大,但增大幅度呈减小趋势;从图1b中获知,2R钢在干湿比为0 (全浸)、1/3、1、3条件下的腐蚀速率分别为0.034、0.044、0.059和0.067 g/(m2·h),2R钢的腐蚀速率与干湿比的关系与1R钢一致。综上,1R钢和2R钢的腐蚀速率均随干湿比增大而增大,但增大幅度呈减小趋势。
图1
图1
1R钢和2R钢的腐蚀速率随干湿比的变化
Fig.1
Changes of corrosion rate of 1R steel (a) and 2R steel (b) with dry/wet ratio
此外,1R钢在不同干湿比条件下的腐蚀速率均低于2R钢。其中,在干湿比为0 (全浸) 条件下,2R钢的腐蚀速率是1R钢的1.214倍;而当干湿比为1/3、1、3时,2R钢的腐蚀速率分别是1R钢的1.333倍、1.372倍、1.457倍。该结果表明在不同干湿比条件的120 mmol/L NH4H2PO4溶液环境下,1R钢的耐蚀性好于2R钢。
2.2 腐蚀形貌
图2
图2
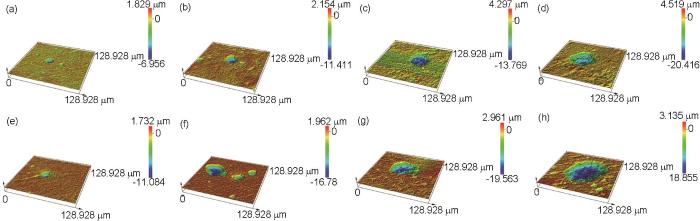
1R钢和2R钢在不同浸泡条件实验21 d后的腐蚀产物形貌
Fig.2
Corrosion images of corrosion products of 1R (a-d) and 2R (e-h) steel at dry/wet=0 (a, e), dry/wet=1/3 (b, f), dry/wet=1 (c, g) and dry/wet=3 (d, h) after test for 21 d
利用激光共聚焦显微镜测量1R钢和2R钢在不同干湿比条件下的120 mmol/L NH4H2PO4溶液中实验21 d后的表面粗糙度和表面积比参数,其结果见表1。从表1中可知,在干湿比为0 (全浸) 条件下,1R钢的表面粗糙度Ra和表面积比分别为0.7 μm和1.5,而2R钢的表面粗糙度Ra和表面积比分别为0.8 μm和1.6。随着干湿比的增大,1R钢和2R钢的表面粗糙度Ra和表面积比均增大。此外,在干湿比为0、1/3、1、3条件下,2R钢的粗糙度Ra分别是1R钢的1.143倍、1.154倍、1.235倍、1.116倍,2R钢的表面积比分别是1R钢的1.067倍、1.050倍、1.087倍、1.132倍。通常,腐蚀产物膜的表面积比越大则表明腐蚀产物覆盖程度及致密程度越小,腐蚀产物膜的保护能力降低,这与图1所得结论一致[16]。由图3不同干湿比条件下的120 mmol/L NH4H2PO4溶液中实验21 d除锈后的腐蚀形貌可以看出,在干湿比为0 (全浸) 条件下,1R钢和2R钢的基体表现出明显的均匀腐蚀特征,此外,两种钢的基体表面上也存在着少量腐蚀坑 (图3a,e)。随着干湿比的增大,1R钢和2R钢的基体表面上的腐蚀坑增多、增大。另外,在不同干湿比条件下,2R钢的点蚀程度高于1R钢。
表1 在1R钢和2R在不同浸泡条件实验21 d后的表面粗糙度及表面积比参数
Table 1
| Steels | Condition | Surface roughness / μm | Specific surface area | ||
|---|---|---|---|---|---|
| Ra | Rq | Rz | |||
| 1R | Dry/wet=0 | 0.7 | 0.8 | 4.0 | 1.5 |
| Dry/wet=1/3 | 1.3 | 1.7 | 7.6 | 2.0 | |
| Dry/wet=1 | 1.7 | 2.0 | 8.1 | 2.3 | |
| Dry/wet=3 | 4.3 | 5.3 | 25.9 | 5.3 | |
| 2R | Dry/wet=0 | 0.8 | 1.0 | 4.3 | 1.6 |
| Dry/wet=1/3 | 1.5 | 1.8 | 8.0 | 2.1 | |
| Dry/wet=1 | 2.1 | 2.5 | 11.3 | 2.5 | |
| Dry/wet=3 | 4.8 | 6.1 | 28.4 | 6.0 | |
图3
图3
1R和2R钢在不同浸泡条件实验21 d除锈后的腐蚀产物形貌
Fig.3
Corrosion images of 1R (a-d) and 2R (e-h) after removal of corrosion products at dry/wet=0 (a, e), dry/wet=1/3 (b, f), dry/wet=1 (c, g) and dry/wet=3 (d, h) after test for 21 d
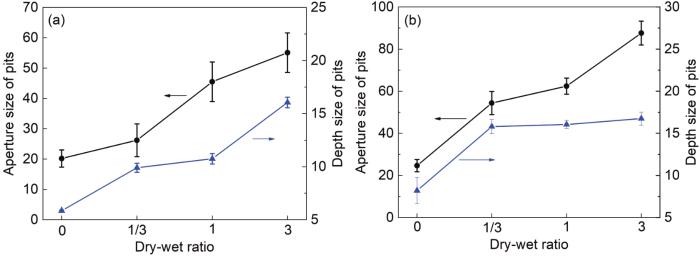
1R钢和2R钢在不同干湿比条件下的120 mmol/L NH4H2PO4溶液中实验21 d除锈后的表面三维形貌见图4,并测量出腐蚀坑的孔径及孔深,其结果见图5。可以看出,在干湿比为0、1/3、1、3条件下,1R钢基体上的腐蚀坑平均孔径分别为20.2、26.2、45.5和55.1 μm,2R钢基体上的腐蚀坑平均孔径分别为24.7、54.4、62.4和87.6 μm,1R钢基体上的腐蚀坑平均孔深分别为5.9、9.9、10.8和16.1 μm,2R钢基体上的腐蚀坑平均孔深分别为8.2、15.8、16.1和16.8 μm。即1R钢和2R钢基体表面上的腐蚀坑的孔径和孔深均随干湿比的增大而增大,且其孔径增大幅度大于孔深。此外,在不同干湿比条件下,2R钢基体表面上的腐蚀坑的孔径和孔深均大于1R钢 (图4和5)。通常,随着干湿比的增大,材料受液膜影响时间延长,但当液膜厚度小于某一临界值后,材料的腐蚀过程便变得缓慢,甚至停滞,这主要是氧的盐效应和阴极电流不均匀分布造成的[13,18,19]。同时,这也是图1中出现材料腐蚀速率的增大幅度随干湿比的增大而减小的原因之一。
图4
图4
1R钢和2R钢在不同浸泡条件实验21 d后的腐蚀坑三维形貌
Fig.4
Three-dimensional morphologies of pits on 1R (a-d) and 2R (e-h) at dry/wet=0 (a, e), dry/wet=1/3 (b, f), dry/wet=1 (c, g) and dry/wet=3 (d, h) after test for 21 d
图5
图5
1R钢和2R钢在不同浸泡条件实验后的腐蚀坑的孔径及孔深
Fig.5
Aperture and depth of pits on 1R steel (a) and 2R steel (b) after test under different immersion conditions
2.3 XRD测试
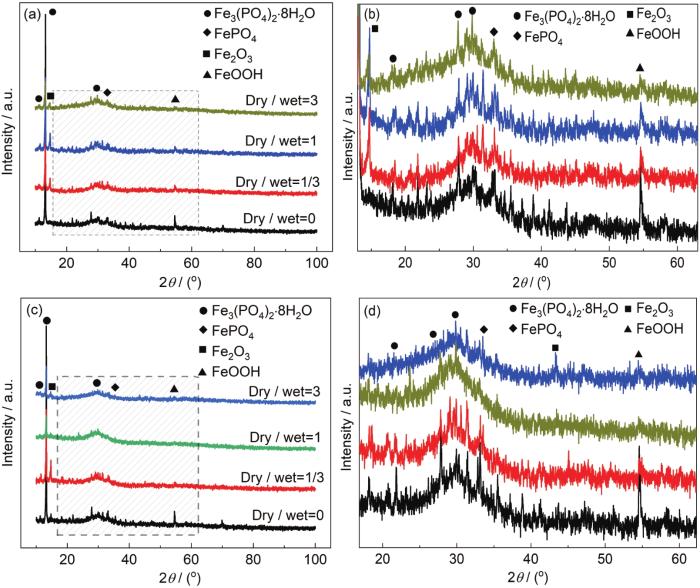
图6为不同干湿比条件下的120 mmol/L NH4H2PO4溶液中实验21 d后生成的腐蚀产物的XRD谱。由图可知,在干湿比为0 (全浸)、1/3、1、3条件下,1R钢和2R钢的腐蚀产物的XRD谱图中均含有明显的Fe3(PO4)2·8H2O衍射峰,说明Fe3(PO4)2为腐蚀产物中的主要物质组成之一,腐蚀过程中,两种钢基体溶解而形成的Fe2+与NH4H2PO4溶液中的PO43-相互结合并沉积在基体上[19]。此外,两种钢的腐蚀产物的XRD谱图也表现出FePO4、Fe2O3、FeOOH的衍射峰,说明FePO4、Fe2O3、FeOOH也是1R钢和2R钢的腐蚀产物中的物质组成。另外,腐蚀产物中也可能存在XRD无法检查到的非晶物质、超细晶物质等[20]。
图6
图6
1R钢和2R钢在不同浸泡条件实验后的腐蚀产物XRD谱图
Fig.6
XRD patterns of the corrosion product on the 1R steel (a, b) and 2R steel (c, d) after test under different immersion conditions
由图6还可看出,随着干湿比增大,1R钢和2R钢生成的腐蚀产物的XRD谱图中FeOOH的衍射峰强度减弱 (图6b,d),结果表明1R钢和2R钢生成的腐蚀产物中FeOOH的含量随干湿比的增大而减少。这是因为在干湿交替的表面干燥阶段,腐蚀产物中部分FeOOH脱水而形成Fe2O3,而干湿比越大,干燥阶段时间越长,从而造成更多的FeOOH脱水而形成Fe2O3[21]。再加上在干燥阶段,材料受液膜影响,氧供应充分,实验钢基体中Fe更容易被氧化成Fe2O3,从而造成了相较于全浸 (dry/wet=0) 条件,在干湿交替条件下,1R钢和2R钢生成的腐蚀产物的XRD谱图中Fe2O3的衍射峰强度较高的结果 (图6a,b)[22]。此外,值得注意的是1R钢和2R钢生成的腐蚀产物的XRD谱图中Fe3(PO4)2·8H2O衍射峰强度随干湿比的增大而减弱,这是因为随着干湿比的增大,表面干燥阶段时间延长,更多Fe3(PO4)2·8H2O脱水或被氧化而消失[23]。
2.4 XPS测试
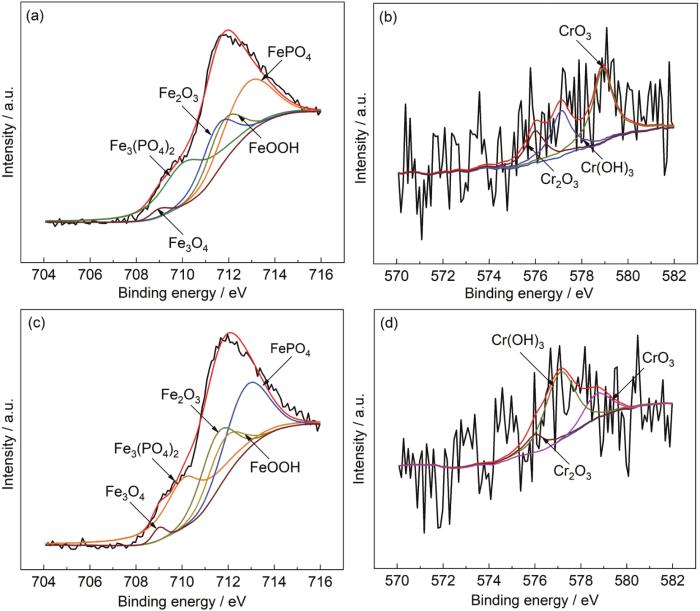
为了进一步表征1R钢和2R钢在不同干湿比条件下的120 mmol/L NH4H2PO4溶液中实验21 d后生成的腐蚀产物膜,本文选取两种钢在干湿比为1/3条件下生成的腐蚀产物膜,并做XPS分析。图7为1R钢和2R钢在干湿比为1/3的120 mmol/L NH4H2PO4溶液环境下形成腐蚀产物膜中Fe 2P3/2、Cr2p3/2的XPS图谱。利用NIST的原子谱数据库和相关文献对图谱进行分峰,表2为各主要组成相的结合能,表3为XPS谱图拟合出的各峰面积及其面积比[14,20,24-27]。1R钢和2R钢的腐蚀产物膜中Fe 2P3/2的XPS图谱可以拟合出5个峰,分别对应Fe3O4、Fe2O3、FeOOH、Fe3(PO4)2、FePO4,其中Fe3(PO4)2和FePO4对应的峰面积更大 (见图7a,c),说明1R钢和2R钢的腐蚀产物膜中Fe更倾向于形成Fe的磷酸盐化合物Fe3(PO4)2和FePO4;1R钢和2R钢的腐蚀产物膜中Cr 2p3/2的XPS图谱可以拟合出3个峰,分别对应Cr2O3、CrO3、Cr(OH)3,其中1R钢的CrO3对应的峰面积最大 (图7b),而2R钢的Cr(OH)3对应的峰面积最大 (见图4b),说明1R钢的腐蚀产物膜中Cr更倾向于形成Cr的氧化物CrO3,而2R钢的腐蚀产物膜中Cr更倾向于形成Cr的氢氧化物Cr(OH)3。
图7
图7
1R钢和2R钢在干湿比为1/3条件下形成的腐蚀产物膜的XPS谱图
Fig.7
XPS spectra of corrosion product film on the 1R steel and 2R steel after test under dry/wet=1/3 condition for 21 d: (a) 1R steel, Fe2p3/2, (b) 1R steel, Cr2p3/2, (c) 2R steel, Fe2p3/2, (d) 2R steel, Cr2p3/2
表2 腐蚀产物膜中主要组成相的结合能
Table 2
| Element | Peak | Species / binding energy |
|---|---|---|
| Fe | 2p3/2 | Fe3O4/709 eV; Fe2O3/711.5 eV; FeOOH/711.8 eV;Fe3(PO4)2/710.1 eV; FePO4/712.8 eV |
| Cr | 2p3/2 | CrO3/578.9 eV;Cr2O3/576 eV; Cr(OH)3/577.1 eV |
表3 腐蚀产物膜中Fe 2p3/2、Cr 2p3/2的XPS谱图拟合出的各峰面积及其面积比
Table 3
| Elements | Product | Peak areas (Percentage of peak area / %) | |
|---|---|---|---|
| 1R | 2R | ||
| Fe 2p3/2 | Fe3O4 | 931 (1.79) | 884.38 (1.81) |
| Fe2O3 | 10257.22 (19.7) | 10204.03 (20.88) | |
| FeOOH | 8668.64 (16.65) | 7254.12 (14.85) | |
| Fe3(PO4)2 | 16828.17 (32.33) | 15985.2 (32.72) | |
| FePO4 | 15373.17 (29.53) | 14529.2 (29.74) | |
| Cr 2p3/2 | Cr2O3 | 400.8 (20.73) | 274 (14.71) |
| CrO3 | 948.52 (49.05) | 1239.64 (18.72) | |
| Cr (OH)3 | 584.49 (30.22) | 3765.1 (66.57) | |
为了进一步分析1R钢和2R钢的腐蚀产物膜的差异性,本文通过
2.5 开路电位
图8
图8
1R钢和2R钢在不同浸泡条件实验21 d后的开路电位
Fig.8
Open circuit potentials of 1R steel (a) and 2R steel (b) aftertest under different immersion conditions for 21 d
2.6 电化学阻抗谱
图9
图9
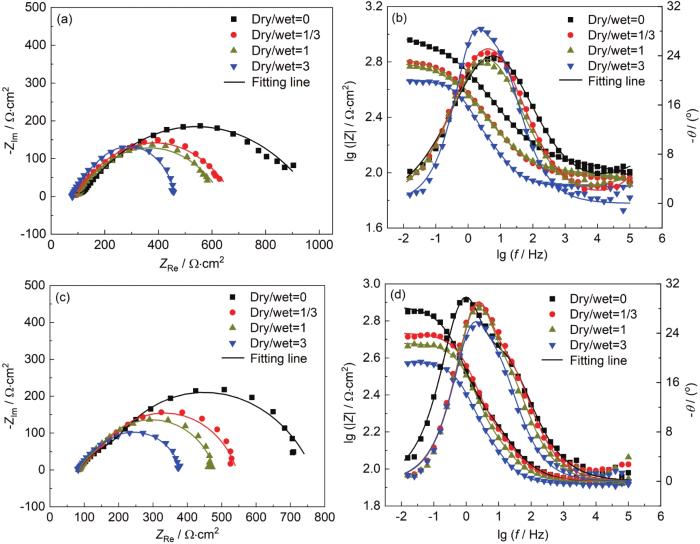
1R钢和2R钢在不同浸泡条件实验21 d后的电化学阻抗谱
Fig.9
Nyquist plots (a, c) and Bode plots (b, d) of the 1R steel (a, b) and 2R steel (c, d) after test under different immersion conditions for 21 d
图10
图10
1R钢和2R钢在不同浸泡条件实验21 d后的等效电路
Fig.10
Equivalent circuits of the 1R steel and 2R steel aftertest under different immersion conditions for 21 d
表4 1R钢和2R钢在不同浸泡条件实验21 d后的电化学阻抗谱参数
Table 4
| Steel | Condition | Rs / Ω·cm2 | Qf | Rf / Ω·cm2 | Qdl | Rct / Ω·cm2 | ||
|---|---|---|---|---|---|---|---|---|
| Y0 / Ω-1·cm-2·S n | Y0 / Ω-1·cm-2·S n | n | ||||||
| 1R | Dry/wet=0 | 80.36 | 3.19 | 0.31 | 118.2 | 5.1 | 0.52 | 861.9 |
| Dry/wet=1/3 | 81.03 | 2.33 | 0.62 | 93.03 | 7.08 | 0.57 | 585.6 | |
| Dry/wet=1 | 80.93 | 3.26 | 0.74 | 18.11 | 7.86 | 0.57 | 539 | |
| Dry/wet=3 | 79.4 | 4.7 | 0.76 | 20.57 | 6.29 | 0.74 | 181 | |
| 2R | Dry/wet=0 | 85.09 | 4.76 | 0.65 | 224.7 | 5.76 | 0.91 | 455.7 |
| Dry/wet=1/3 | 86.58 | 3.24 | 0.73 | 160.3 | 3.39 | 0.92 | 297.2 | |
| Dry/wet=1 | 85.51 | 3.64 | 0.77 | 132 | 3.81 | 0.90 | 262.4 | |
| Dry/wet=3 | 82.65 | 6.02 | 0.76 | 120.3 | 7.14 | 0.95 | 139.1 | |
2.7 腐蚀机理
实验钢1R钢和2R钢在120 mmol/L NH4H2PO4溶液中全浸实验时,发生腐蚀反应,其中阳极反应为基体中Fe失去两个电子而形成Fe2+,而阴极反应为氧的去极化反应,但随着浸泡时间的延长,材料表面的腐蚀产物增多增厚,一定程度抑制氧的扩散,所以腐蚀反应的阴极过程也会出现铁锈的还原反应,如FeOOH的阴极还原反应具体反应如下:
当然,部分Fe2+会被溶液中的溶解氧氧化为Fe3+,随着腐蚀的进行,H+、Fe2+、Fe3+、NH4+等阳离子向阴极方向运动,而OH-、H2PO4-、HPO42-、PO43-等阴离子则向阳极方向运动,并在活化阳极区附近发生的反应如下所示[20]:
而1R钢和2R钢在干湿交替实验时,所发生的腐蚀反应基本与全浸条件下一样。唯一的区别是,相较于全浸条件,在干湿交替条件下,尤其在表面干燥阶段,Fe(OH)2和FeOOH会脱水而形成FeO和Fe2O3,而此时,材料受液膜影响,氧供应充分,所以FeO会被氧化成Fe2O3[22]。
3 结论
(1) 在干湿比为0 (全浸)、1/3、1、3条件下的120 mmol/L NH4H2PO4溶液环境中,2Cr-1Ni-1.2Mo-0.2V钢和2Cr-4Ni-0.4Mo-0.1V钢均发生均匀腐蚀和点蚀。随着干湿比增大,,两种钢的腐蚀速率增大,点蚀程度变大,但2Cr-1Ni-1.2Mo-0.2V钢的耐蚀性好于2Cr-4Ni-0.4Mo-0.1V钢。
(2) 在干湿比为0 (全浸)、1/3、1、3条件下的120 mmol/L NH4H2PO4溶液环境中,2Cr-1Ni-1.2Mo-0.2V钢和2Cr-4Ni-0.4Mo-0.1V钢生成的腐蚀产物膜主要由Fe3(PO4)2、FePO4、Fe2O3、FeOOH构成,且随着干湿比增大,腐蚀产物中FeOOH和Fe3(PO4)2的含量减少,Fe2O3含量增多。此外,随着干湿比的增大,2Cr-1Ni-1.2Mo-0.2V钢和2Cr-4Ni-0.4Mo-0.1V钢的腐蚀产物膜的保护性变差,但2Cr-1Ni-1.2Mo-0.2V钢的腐蚀产物膜的保护性优于2Cr-4Ni-0.4Mo-0.1V钢。
(3) 随着干湿比增大,2Cr-1Ni-1.2Mo-0.2V钢和2Cr-4Ni-0.4Mo-0.1V钢的开路电位负移,腐蚀产物膜的膜层电阻减小,电荷转移电阻变小,而2Cr-4Ni-0.4Mo-0.1V钢的腐蚀速率高于2Cr-1Ni-1.2Mo-0.2V钢。
参考文献
Production of environmental ammonium phosphate powder extinguishing agent from fertilizer grade monoammonium phosphate
[J].
用肥料级磷酸一铵生产环保型磷酸铵盐干粉灭火剂
[J].
Determination of phosphorus content in MAP and DAP by ICP-AES
[J].
电感耦合等离子体发射光谱法测定磷酸一铵和磷酸二铵中磷含量
[J].
Technical status of industrial grade monoammonium phosphate production by WPA purification method and industrial application of its key technology
[J].
湿法磷酸净化生产工业级磷酸一铵的技术现状及关键技术的工业应用
[J].
Application and problem analysis of industrial waste heat power generation system
[J].
工业余热发电系统的应用及问题分析
[J].
Comprehensive utilization of low temperature waste heat resources in chemical industry
[J].
综合利用化工行业低温余热资源
[J].
Deflection behaviour of corrosion crack growth in the heat affected zone of CrNiMoV steel welded joint
[J].
Research on corrosion behavior of weathering steel in marine atmosphere of the south China sea
[D].
耐候钢在南海海洋大气环境下的腐蚀行为研究
[D].
Weathering steels: from empirical development to scientific design. A review
[J].
Atmospheric corrosion monitoring of a weathering steel under an electrolyte film in cyclic wet-dry condition
[J].
Influence of dry-wet cycles on the marine corrosion behavior of carbon steel
[J].
干湿交替环境状态对碳钢海洋腐蚀行为的影响
[J].
EIS monitoring study of atmospheric corrosion under variable relative humidity
[J].
Electrochemical characterization and stress corrosion cracking of E690 high strength steel in wet-dry cyclic marine environments
[J].
Electrochemical corrosion behavior of a CrNiMoV steel in NH4H2PO4 solution
[J].
一种CrNiMoV钢在NH4H2PO4溶液中的电化学腐蚀行为研究
[J].
Behaviors of corrosion and inhibition of X70 steel in (NH4)2CO3 solutions
[J].
X70钢在 (NH4)2CO3溶液中腐蚀及缓蚀行为
[J].
Influence of peening on the corrosion properties of AISI 304 stainless steel
[J].
Effect of surface mechanical attrition treatment on corrosion behavior of 316 stainless steel
[J].
Development of the electrochemical theory of metallic corrosion
[J].
Electrochemical measurements under thin electrocute laer using kelvin probe reference electrode
[J].
使用Kelvin探头参比电极技术进行薄液层下电化学测量
[J].
Corrosion behavior of Cr bearing weathering steel in simulated marine atmosphere
[J].
含铬耐候钢在模拟海洋大气环境中的腐蚀行为
[J].
Corrosion behavior of automotive cold rolled steels DC06 and DP600 in NaHSO3 solution
[J].
汽车冷轧钢DC06和DP600在NaHSO3溶液中的腐蚀行为
[J].
Advances in understanding atmospheric corrosion of iron. II. Mechanistic modelling of wet-dry cycles
[J].
Enhanced phosphate removal efficiency by using ferrous iron and its mechanism
[D].
亚铁强化去除水中磷酸盐的作用机制与效能
[D].
Effect of CO32- on the electrochemical behaviour of 14Cr12Ni3Mo2VN stainless steel in a sodium chloride solution
[J].
Investigation of multiplet splitting of Fe 2p XPS spectra and bonding in iron compounds
[J].
Characterization of passive film on 2205 duplex stainless steel in sodium thiosulphate solution
[J].
Effect of pH on corrosion behavior of 14Cr12Ni3WMoV stainless steel in chlorine-containing solutions
[J].
pH对14Cr12Ni3WMoV不锈钢在含氯溶液中腐蚀行为的影响
[J].
Corrosion inhibition effect research of compound corrosion inhibitor for N80 steel in HCl solution medium
[J].
盐酸介质中复配缓蚀剂对N80钢缓蚀效果分析研究
[J].
Effect of temperature on corrosion behavior of 14Cr12Ni3WMoV stainless steel in 0.02 mol/L NaCl solution
[J].
温度对14Cr12Ni3WMoV不锈钢在0.02 mol/LNaCl溶液中腐蚀行为的影响
[J].
The formation and impacting mechanism of corrosion product film of low chromium alloy steel in CO2/H2S environment
[D].
含Cr低合金钢CO2/H2S环境腐蚀产物膜形成及作用机理研究
[D].
The influence of chromium content on the electrochemical behavior of weathering steels
[J].
Influence of alloyed chromium on the atmospheric corrosion resistance of weathering steels
[J].