氟化物熔盐是一种工作温度高、蒸汽压低、工作温度范围宽的流体,可用作熔盐反应堆的冷却剂和核燃料载体[1,2]。另外,氟化物熔盐的高导热性和热容量也使其成为太阳能集蓄热载体的候选材料[3]。但结构材料 (通常是合金) 与熔盐的相容性是氟化物熔盐应用中需要关注的一大问题[4]。为解决材料与氟熔盐的相容性问题,美国橡树岭实验室 (ORNL) 研发了以Ni作为材料基体的Hastelloy N合金[5],实验证明镍基合金在高温氟化物熔盐中具有良好的耐腐蚀性能[6,7,8,9]。然而,这些高温合金的高价格及其相对复杂的制造工艺限制了其工业应用。316L不锈钢 (316LSS) 是一种应用较广的合金材料,其制造工艺及成本均明显优于镍基合金,但由于316L合金中Cr含量较高,且Cr相对于合金中的其他元素最易被氧化,这使其在熔盐中的腐蚀较为严重[10,11,12,13]。许多研究人员提出采用还原性缓蚀剂,即控制熔盐中的氧化还原电位的方法来抑制腐蚀[14,15,16],取得显著的抑制效果。但该技术目前仅处于起步阶段,缺少量化数据且对氧化还原缓冲熔盐的性质缺乏系统认识。本文拟向熔盐中引入Cr2+/Cr3+电极电对形成氧化还原缓冲熔盐,通过调节电对的浓度比控制熔盐电位使之处于较负 (还原) 的状态,从而抑制316L不锈钢在氟化物熔盐中的腐蚀。实验过程中,拟采用一种修正的Tafel方法测试316L不锈钢在FLiNaK-CrF3/CrF2缓冲熔盐中的腐蚀电流,从而获得氧化还原缓冲熔盐对腐蚀抑制作用的量化数据,加深对这类体系的认识。
1 实验方法
1.1 实验准备
在手套箱中称取一定质量的高纯FLiNaK盐 (约300 g) 置于玻璃碳坩埚中,逐步添加CrF3 (Sigma-Aldrich,99.99%,质量分数) 和CrF2(Alfa Aesar, 95%,质量分数) 到FliNaK熔盐中形成氧化还原缓冲熔盐。将玻璃碳坩埚转移至真空管式炉中升温加热,并采用镍铬热电偶插入熔盐中以实时测定熔盐的温度。
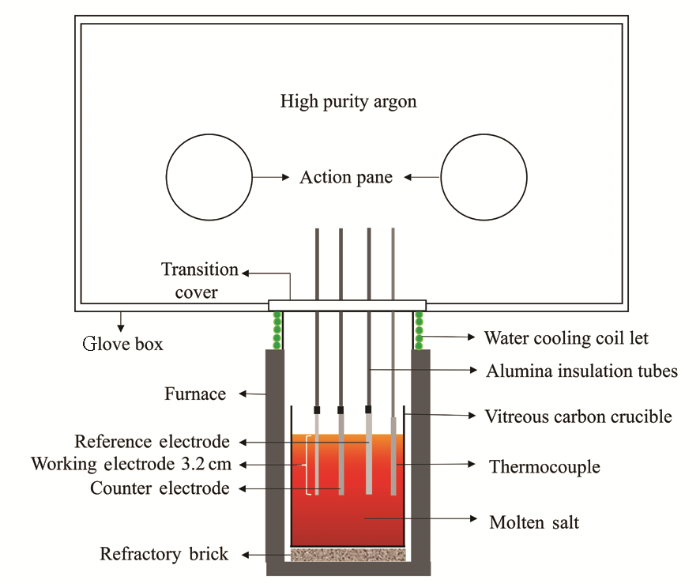
整个电化学实验在低湿度、低氧环境的手套箱内完成 (H2O<10×10-6,O2<10×10-6,体积分数),如图1所示。待熔盐熔融后,采用三电极体系进行电化学测试,工作电极为Φ=1 mm的316L不锈钢丝 (Fe-17%Cr-13%Ni-2.5%Mo, 质量分数)、纯Fe丝 (纯度>99%)、镍基合金Hastelloy C-276(HC276,Ni-16%Cr-16%Mo-5%Fe-4%W,质量分数) 丝和Ag丝,插入熔盐的深度均为3.2 cm,工作电极的工作面积为1 cm×1 cm。对电极采用光谱纯的石墨棒 (Φ=10 mm),并使其浸入熔盐中的面积远大于工作电极的面积。参比电极采用热压氮化硼管封装的FLiNaK-23.5%NiF2 (质量分数) 和Ni丝组成的Ni/NiF2参比电极,其结构如图2所示。采用AUTOLAB电化学工作站对熔盐体系电化学参数进行测量。
图1
图2
图2
具有离子导通功能的热压氮化硼管参比电极
Fig.2
Ion-conducting tube made from HPBN for the Ni/NiF2 reference electrode
线性极化曲线测试前用粒径6.5 μm的SiC砂纸对金属电极打磨。测试时,将测试电极提前约15 min插入熔盐中,待开路电压 (OCP) 稳定后,以0.5 mV/s的速率由开路电压向正或负150 mV方向扫描。
1.2 经典Tafel方法
图3
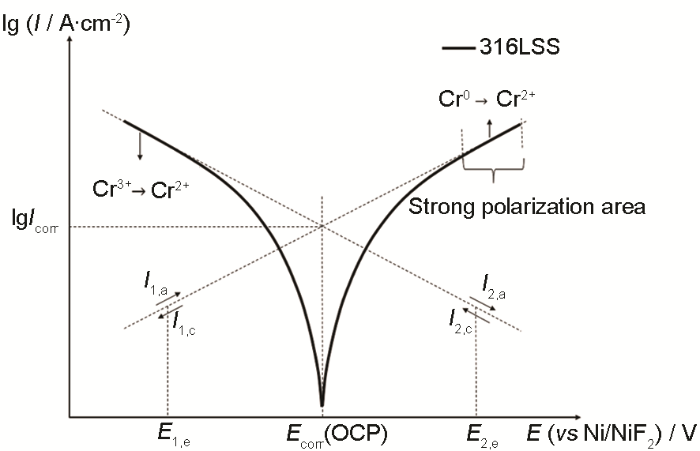
图3
经典Tafel方法在非氧化还原缓冲体系中应用原理图
Fig.3
Illustration of Tafel extrapolation method in non-redox buffering molten salt system
阳极极化过程中则对应Cr0氧化为Cr2+:
然而316L不锈钢在氧化还原缓冲体系 (FLiNaK-CrF3/CrF2体系) 中由于阳极极化曲线含有干扰电流 (Cr2+→Cr3+),而导致经典Tafel方法不再适用。
1.3 修正的Tafel方法
本文采取一种修正的Tafel方法获得316L不锈钢在氧化还原缓冲体系中的腐蚀电流密度,其原理如图4所示。
图4
图4
修正的Tafel方法在氧化还原缓冲体系中应用原理图
Fig.4
Illustration of modified Tafel extrapolation method in redox buffering molten salt system
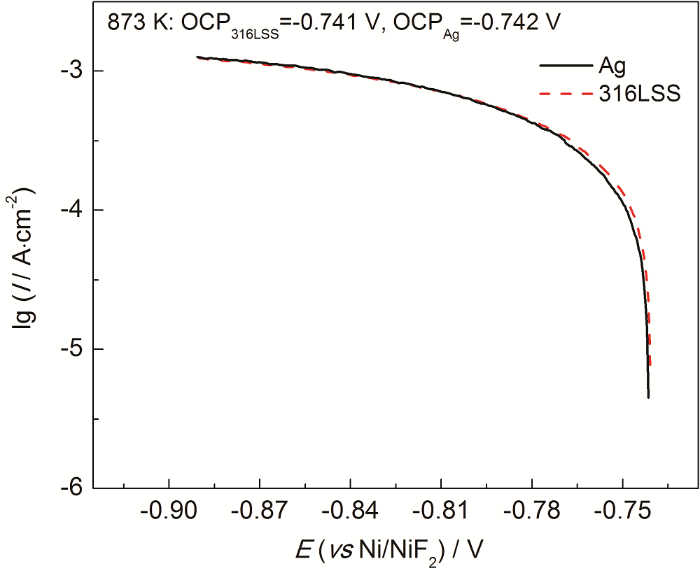
在氧化还原缓冲体系 (FLiNaK-CrF3/CrF2体系) 中,316L不锈钢和Ag电极上有着相同的开路电压,且它们的阴极极化过程发生相同的电化学反应 (Cr3+→Cr2+和Cr2+→Cr0),从而使其阴极极化曲线几乎重合。图5为实际在FLiNaK-CrF3/CrF2体系中测得316L不锈钢和Ag电极上的阴极极化曲线,它们几乎重合,所以从阴极极化曲线不能获得准确的腐蚀电流密度。
图5
图5
316L不锈钢和Ag电极在氧化还原缓冲体系 (FLiNaK-CrF3/CrF2) 中的阴极极化曲线
Fig.5
Cathodic polarization curves of 316LSS and Ag electrode in FLiNaK-CrF3/CrF2 redox buffering molten salt system
316L不锈钢电极上的阳极极化曲线在强极化区 (约为-0.7~-0.6 V vs Ni/NiF2,是Cr的氧化还原反应区间) 发生的反应主要为:
而Ag电极上的阳极极化曲线在强极化区发生的反应主要为反应式 (4)。
2 结果与讨论
2.1 熔盐体系循环伏安测试
图6
图6
Ag在873 K下纯FliNaK熔盐中的循环伏安曲线 (扫描速率100 mV/s)
Fig.6
CV curves of Ag working electrode at 873 K in pure FLiNaK molten salt (scanning rate: 100 mV/s)
图7
图7
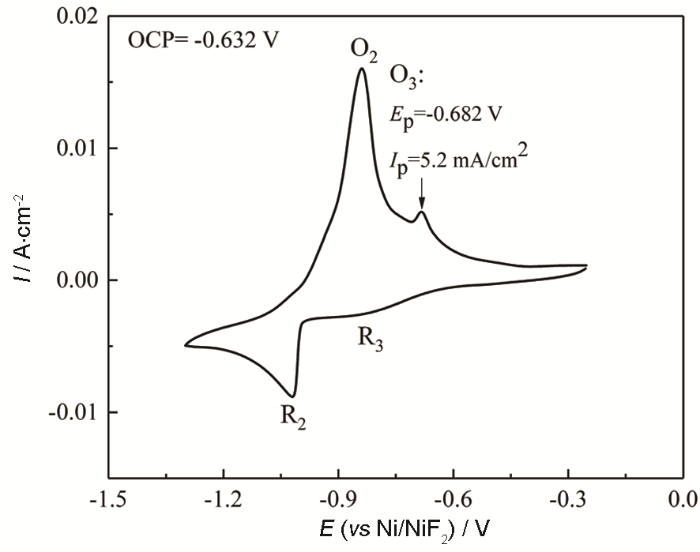
Ag在873 K下FLiNaK-CrF3/CrF2体系中的循环伏安曲线 (扫描速率100 mV/s)
Fig.7
CV curves of Ag working electrode at 873 K in FLiNaK-CrF3/CrF2 molten salt (scanning rate: 100 mV/s)
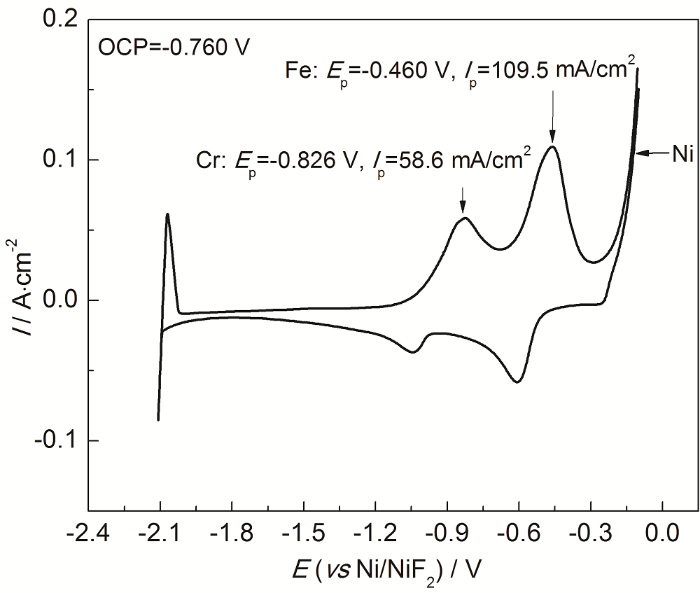
316L不锈钢在FLiNaK-CrF3/CrF2体系中的循环伏安测试如图8所示。Cr的氧化峰同样位于约为-1.1~-0.6 V,由于316L不锈钢电极上的反应电流较大,导致无法分辨出Cr的分步氧化反应峰电势。根据金属的氧化电位顺序可知,其后位于-0.6~-0.3 V的氧化峰为Fe的氧化区间。实验中使用的是Ni/NiF2参比电极,所以位于约0 V的氧化反应为Ni的氧化峰。
图8
图8
316L不锈钢在873 K下FLiNaK-CrF3/CrF2体系中的循环伏安曲线 (扫描速率: 100 mV/s)
Fig.8
CV curves of 316LSS working electrode at 873 K in FLiNaK-CrF3/CrF2 molten salt (scanning rate: 100 mV/s)
2.2 氧化还原缓冲熔盐中Cr3+/Cr2+标准电极电势EꝊ的近似处理
式中,R为气体常数,8.314 J/(K·mol);T为温度;n为电极反应中电子转移数;F为Faraday常数,96.487 kJ/(V·mol)。
通过多次循环伏安曲线测试可以获取不同CrF2/CrF3浓度比和不同温度条件下的Cr3+/Cr2+反应的峰电势Ep。由于半波电势E1/2接近于标准电极电势EꝊ,所以本文中用E1/2近似替代EꝊ。873和823 K条件下的标准电极电势如表1所示。Cr3+/Cr2+反应电对在873和823 K时的准标准电极电位分别为-0.755和-0.743 V。标准电极电势的获得将有助于后面计算氧化还原缓冲熔盐中Cr3+/Cr2+的浓度比值。
表1 通过循环伏安法获得Cr3+/Cr2+的峰电势EP,并计算出半波电势E1/2
Table 1
| Temperature / K | Ep / V | Average / V | RT/nF | E1/2 (EꝊ) / V |
|---|---|---|---|---|
| 873 | -0.682 | --- | --- | --- |
| -0.667 | -0.672 | 0.075 | -0.755 | |
| -0.666 | --- | --- | --- | |
| 823 | -0.669 | --- | --- | --- |
| -0.659 | -0.664 | 0.071 | -0.743 | |
| -0.665 | --- | --- | --- |
2.3 氧化还原缓冲熔盐体系的建立与熔盐电位和腐蚀电位Ecorr的讨论
本文通过向含有1000 μg·g-1 CrF3的FLiNaK熔盐中逐步添加CrF2来形成氧化还原缓冲熔盐。在形成氧化还原缓冲熔盐的过程中,Ag和316L不锈钢电极在熔盐中的电位变化情况如图9所示。
图9
图9
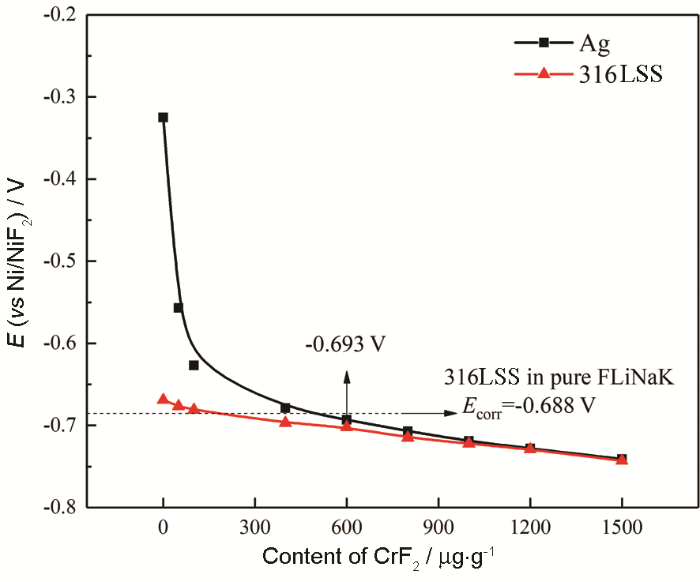
在873 K时随着CrF2逐步添加到含有1000 μg·g-1 CrF3的FLiNaK熔盐中,Ag和316L不锈钢上开路电位的变化
Fig.9
Variations of OCP of Ag and 316LSS at 873 K in FLiNaK molten salt containing 1000 μg·g-1 CrF3 with the content of added CrF2
随着熔盐中CrF2含量的增加,Ag和316L不锈钢电极在熔盐中的电位逐渐趋于一致。当添加600 μg·g-1 CrF2时,Ag和316L不锈钢电极上的电位分别是-0.693和-0.702 V,此时两种金属电极上的电位差小于0.01 V,且后面随着熔盐中CrF2含量的增加电位下降趋于平缓,可认为此时FLiNaK熔盐中已经形成了良好的缓冲效应。当熔盐中添加1000 μg·g-1 CrF2时,Ag和316L不锈钢电极上的电位几乎没有差别。
熔盐中F-、Li+、Na+、K+等离子化学性质稳定对金属材料在熔盐中电位的贡献远小于大量存在的Cr2+和Cr3+,所以金属材料在熔盐中的电位主要取决于熔盐中氧化还原缓冲电对的浓度比值。Ag为惰性金属电极,在熔盐中的电位 (相对于Ni/NiF2参比电极) 即为与熔盐环境氧化性相关的熔盐电位E。根据Nernst方程可知FLiNaK-CrF3/CrF2氧化还原缓冲体系的熔盐电位的表达式如下:
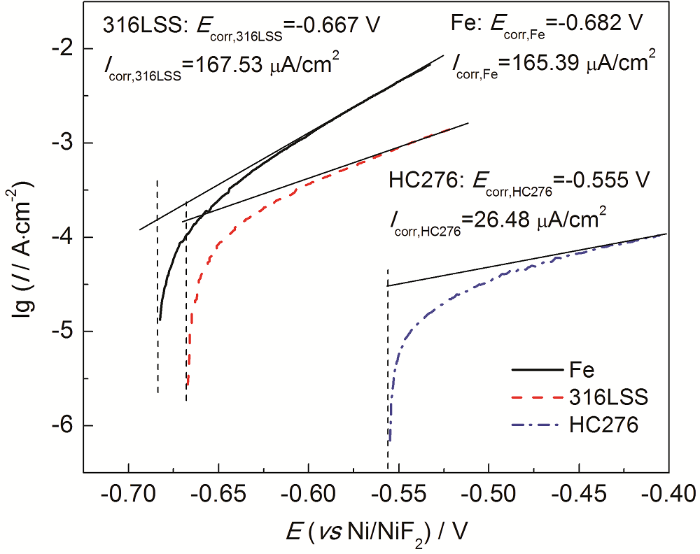
316L不锈钢电极在熔盐中的电位是合金中的金属元素与熔盐环境耦合出来的腐蚀电位Ecorr。根据文献报道Cr、Fe、Ni等纯金属在含有CrF3的FLiNaK熔盐中腐蚀电位的顺序为:Ecorr,Cr<Ecorr,Fe<Ecorr,Ni,腐蚀电流密度顺序为:Icorr,Cr>Icorr,Fe>Icorr,Ni[18]。在本文中也对纯Fe丝、316L不锈钢和镍基合金Hastelloy C-276在含有500 μg·g-1 CrF3的FLiNaK的熔盐中进行了阳极极化曲线测试,如图10所示。其中镍基合金Hastelloy C-276耐腐蚀性能较好,腐蚀电位为-0.555 V高于其它两种金属,腐蚀电流密度26.48 μA/cm2明显低于其它两种金属,这与文献中的报导一致。铁基合金316L不锈钢与纯Fe丝的腐蚀电流密度相近,而腐蚀电位则略高于Fe丝的腐蚀电位。Ag在这个熔盐体系中的电位为-0.422 V,高于以上3种材料的腐蚀电位。
图10
图10
纯Fe丝、316L不锈钢和Hastelloy C-276 (HC276) 在873 K下含有500 μg·g-1 CrF3的FLiNaK中的阳极极化曲线
Fig.10
Anodic polarization curves of pure Fe wire, 316LSS and Hastelloy C-276 (HC276) in FliNaK molten salt containing 500 μg·g-1 CrF3 at 873 K
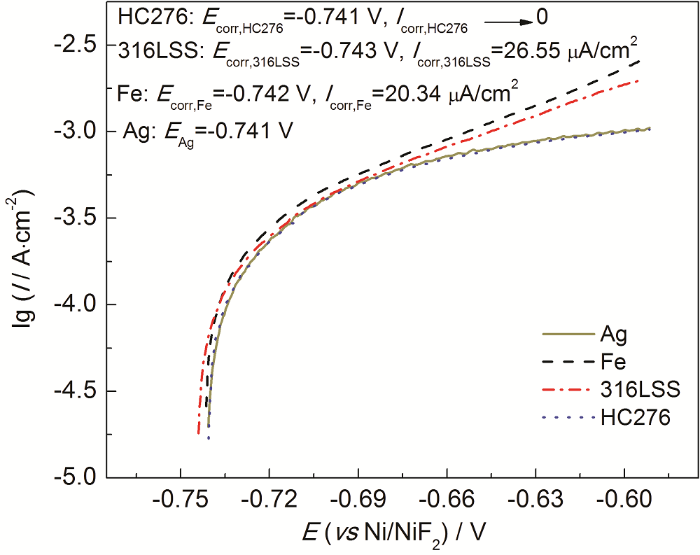
Ag丝、纯Fe丝、316L不锈钢和Hastelloy C-276在熔盐电位为-0.741 V的FLiNaK-CrF3/CrF2熔盐体系中的阳极极化曲线测试如图11所示。纯Fe丝、316L不锈钢和Hastelloy C-276在熔盐中的电位与熔盐电位-0.741 V十分接近。熔盐电位处于较负的状态下,熔盐环境对金属材料的氧化性较低。用修正的Tafel方法得到的纯Fe丝和316L不锈钢的腐蚀电流密度分别为20.34和26.55 μA/cm2,远低于它们在含有500 μg·g-1 CrF3的FLiNaK熔盐中的腐蚀电流密度。Ag和Hastelloy C-276的极化曲线重合,它们的极化电流几乎全由Cr2+→Cr3+反应贡献,材料自身合金元素的氧化对阳极极化电流的贡献极小,这种情况无法用修正的Tafel方法处理,但可推测此时熔盐对Hastelloy C-276的腐蚀电流密度十分微小。
图11
图11
Ag丝、纯Fe丝、316L不锈钢和Hastelloy C-276 (HC276) 在873 K下FLiNaK-CrF3/CrF2熔盐体系中的阳极极化曲线
Fig.11
Anodic polarization curves of Ag wire, pure Fe wire, 316LSS and Hastelloy C-276 (HC276) in FLiNaK-CrF3/CrF2 redox buffering molten salt system at 873 K
在FLiNaK-CrF3熔盐体系中,金属材料的腐蚀电位越低,则越容易被氧化,它们的腐蚀也就越严重。然而在FLiNaK-CrF3/CrF2熔盐体系中,较负的熔盐电位对金属材料有保护作用。此时金属材料的腐蚀电位与熔盐电位表现出相近的现象,在该还原性较强的电位下,它们的腐蚀电流密度也就越低。所以单一的腐蚀电位无法作为材料耐腐蚀性能的评判标准。
当氧化还原缓冲熔盐的熔盐电位处于较负的状态下 (如低于316L不锈钢在纯FLiNaK盐中的Ecorr (873 K时为-0.688 V)),熔盐中存在大量Cr2+和Cr3+。316L不锈钢在熔盐中的电位也和Ag电极一样取决于熔盐中Cr3+/Cr2+的浓度比值,自身的合金元素对电位贡献较小,如图11中所示多种金属材料有着和Ag电极相近的电位。873 K时Cr3+/Cr2+的标准电势为-0.755 V,根据式 (8) 熔盐中Cr2+浓度增加时,316L不锈钢在氧化还原缓冲熔盐体系中的电位很容易就低于其在纯FLiNaK盐中的Ecorr(-0.688 V),表现出316L不锈钢在缓冲熔盐中的Ecorr与Ag上的熔盐电位相近的现象。当熔盐电位较正时 (熔盐中Cr2+含量少),316L不锈钢的Ecorr与熔盐电位表现出较大的差别,这是因为合金中活泼金属元素对Ecorr的贡献增大。
2.4 氧化还原缓冲熔盐中Cr3+/Cr2+浓度比计算
添加1000 μg·g-1 CrF3后的FLiNaK盐冷却后的实物图如图12a所示,呈淡蓝色。当向含有1000 μg·g-1 CrF3的FLiNak熔盐中添加800 μg·g-1 CrF2后,熔盐冷却后的颜色呈暗灰色如图12b所示,并且盐表面有金属光泽。根据文献报道Cr2+在FLiNaK熔盐中会发生歧化反应3Cr2+
图12
图12
添加了1000 μg·g-1 CrF3的FLiNaK盐及添加了1000 μg·g-1 CrF3和800 μg·g-1 CrF2的FLiNaK盐冷却后的实物图
Fig.12
Photos of the salt cakes: (a) FLiNaK+1000 μg·g-1 CrF3, (b) FLiNaK+1000 μg·g-1 CrF3+800 μg·g-1 CrF2
当FLiNaK盐中CrF2与CrF3的添加量分别为600和1000 μg·g-1,转换成浓度比值为0.73。而此时Ag电极上的熔盐电位E为-0.693 V,根据式 (8) 可以计算出对应的Cr2+/Cr3+的浓度比为0.44。可以看出,通过熔盐电位计算出来的Cr2+/Cr3+的浓度比值小于添加的浓度比值,这说明添加到熔盐中CrF2有部分转化成了CrF3,这与文献[19]报道结果一致,同时,该实验结果也验证了通过测定熔盐电位获取熔盐中Cr2+/Cr3+浓度比值的可行性。
2.5 316L不锈钢在熔盐中的腐蚀数据
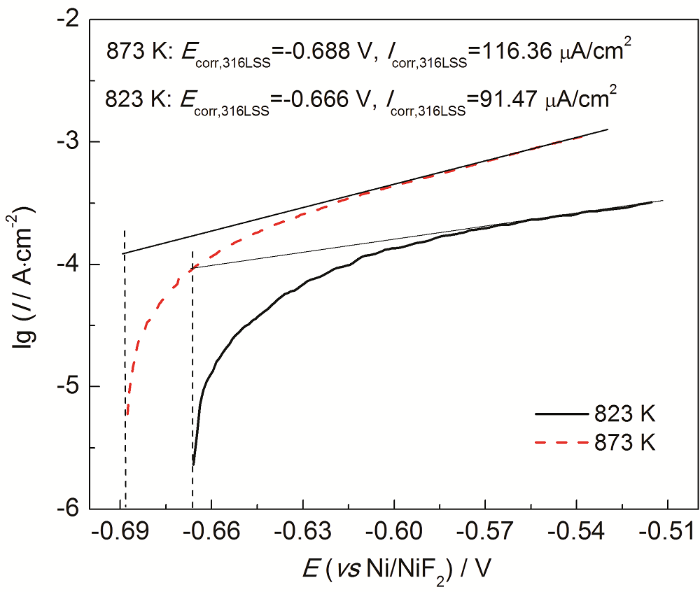
316L不锈钢在纯FLiNaK熔盐中的阳极极化曲线如图13所示。873 K时,316L不锈钢在纯盐中的腐蚀电流密度为116.36 μA/cm2,腐蚀电位为-0.688 V。823 K时,316L不锈钢在纯盐中的腐蚀电流密度为91.47 μA/cm2,腐蚀电位为-0.666 V。温度越高,反应越活泼,316L不锈钢的腐蚀电位越低,越容易被腐蚀,腐蚀电流密度也就越高。
图13
图13
316L不锈钢在873和823 K下纯FLiNaK熔盐中的阳极极化曲线
Fig.13
Anodic polarization curves of 316LSS in FLiNaK molten salt at 873 and 823 K
通过调节FLiNaK熔盐中Cr2+/Cr3+的比值,可以改变熔盐电位。不同熔盐电位下,316L不锈钢在熔盐中的腐蚀电流密度如图14所示。
图14
图14
316L不锈钢在873和823 K、不同熔盐电位条件下的腐蚀电流密度
Fig.14
Corrosion currents density of 316LSS in FLiNaK-CrF3/CrF2 redox buffering molten salt system under different molten potential conditions at 873 and 823 K
在熔盐电位较正时 (873 K时,高于-0.693 V;823 K时,高于-0.660 V),熔盐中CrF2的含量较少,用经典的Tafel方法即可得到316L不锈钢的腐蚀电流密度。在熔盐电位较负时,熔盐中含有较多的CrF2,导致316L不锈钢阳极极化曲线含有较多的干扰电流 (Cr2+→Cr3+),需要用修正的Tafel方法消除,才能得到316L不锈钢实际的腐蚀电流密度。为了能较好的抑制腐蚀,建议在873和823 K时分别将熔盐电位控制在-0.741和-0.703 V以下,此时316L不锈钢的腐蚀电流密度都低于纯盐环境下的腐蚀电流密度,这样能达到较好的抑制腐蚀的效果。本文通过873 K下的浸泡实验验证了这个结论。图15a是在熔盐电位为-0.741 V的氧化还原缓冲熔盐中浸泡100 h后,316L不锈钢丝的截面SEM像,图中未见明显的腐蚀现象。图15b是在纯FLiNaK熔盐中浸泡100 h后,316L不锈钢丝的截面SEM像,可以看到腐蚀深度达到了近15 μm。这很好地验证了氧化还原缓冲熔盐抑制腐蚀的效果,和修正的Tafel方法评价腐蚀状况的可行性。
图15
图15
在熔盐中浸泡100 h后的316L不锈钢丝截面SEM像
Fig.15
Cross sections of 316LSS after 100 h immersion in FLiNaK molten salt containing redox buffer salt under the condition of 873 K and -0.741 V potential (a) and in pure FLiNaK molten salt (b)
在氧化还原缓冲熔盐FLiNaK-CrF3/CrF2体系中,熔盐电位越负,熔盐环境对金属结构材料的氧化性越低,抑制腐蚀的效果越好。这与316L不锈钢在纯FLiNaK熔盐中,腐蚀电位随温度升高而降低,自身更容易被熔盐环境中氧化性杂质腐蚀的情况不同。同样在氧化还原缓冲熔盐中,温度越高腐蚀越严重,在相同电位下,873 K时,316L不锈钢的腐蚀电流密度比823 K时的更高。
图16
图16
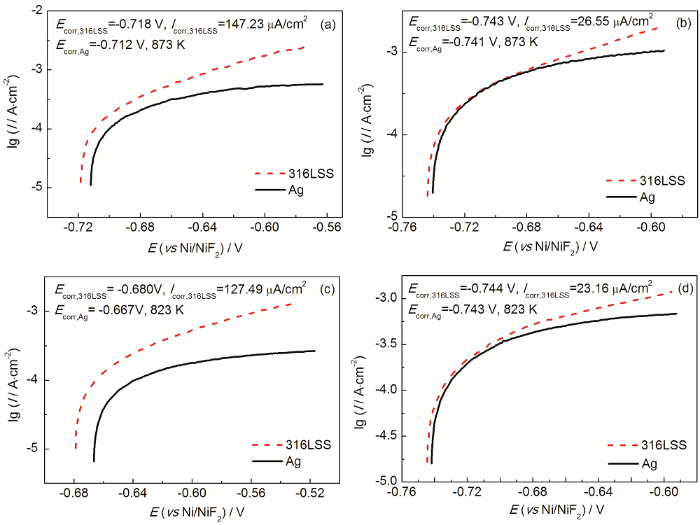
在不同的温度和电位下316L不锈钢和Ag电极在FLiNaK-CrF3/CrF2氧化还原缓冲体系中的阳极极化曲线
Fig.16
Anodic polarization curves of 316LSS and Ag electrodes at 873 and 823 K in FLiNaK-CrF3/CrF2 redox buffering molten salt with the different potentials of -0.712 V (a), -0.741 V (b), -0.667 V (c) and -0.743 V (d)
将图16b用修正的Tafel方法进行处理后,结果见图17。其与图4的理论结果一致。图17中将316L不锈钢和Ag电极的阳极极化曲线的起始电位作为坐标0点进行作图,在阳极强极化区用316L不锈钢上的极化电流减去Ag电极上的极化电流得到了316L不锈钢与腐蚀相关的电流 (蓝色实线)。对蓝色实线进行线性拟合 (拟合度R2=0.9934),拟合的一次函数在0电位点 (即Ecorr,316LSS=-0.743 V,熔盐电位-0.741 V) 的截距为-4.5759,转换成316L不锈钢的腐蚀电流密度即为26.55 μA/cm2。若用未经修正的经典Tafel方法对316L不锈钢进行处理,得到的腐蚀电流密度为310.24 μA/cm2 (远大于316L不锈钢在纯FLiNaK中的腐蚀电流密度116.36 μA/cm2),这显然与实际的腐蚀结果不符 (对比图15中的SEM像)。这一现象验证了经典Tafel方法不适用于FLiNaK-CrF3/CrF2体系中316L不锈钢的腐蚀评价。
图17
图17
用修正的Tafel方法处理后获得的316L不锈钢和Ag电极在FLiNaK-CrF3/CrF2氧化还原缓冲体系中的阳极极化曲线
Fig.17
Anodic polarization curves obtained by applying modified Tafel method for 316LSS and Ag electrodes in FLiNaK-CrF3/CrF2 redox buffering system
3 结论
(1) 温度越高,316L不锈钢在FLiNaK熔盐中的腐蚀越严重。熔盐电位主要取决于熔盐中的氧化还原缓冲电对的Cr3+/Cr2+浓度比。当熔盐电位远低于316L不锈钢在纯FLiNaK中的Ecorr (-0.688 V) 时,能够有效降低316L不锈钢的腐蚀。
(2) FLiNaK-CrF3/CrF2氧化还原缓冲体系中,873 K时,熔盐电位为-0.741 V (Icorr,316LSS=26.55 μA/cm2) 对应的Cr2+/Cr3+的浓度比值为0.83;823 K时,熔盐电位为-0.703 V (Icorr,316LSS=37.37 μA/cm2) 对应Cr2+/Cr3+的浓度比值为0.57。
(3) 在873和823 K时,建议将熔盐电位分别控制在-0.741和-0.703 V以下,或将熔盐中Cr2+/Cr3+的有效浓度比值分别维持在0.83和0.57以上,以达到良好的抑制316L不锈钢腐蚀的效果。
参考文献
Fluoride salt coolant properties for nuclear reactor applications: A review
[J].
Heat transfer fluids for concentrating solar power systems-A review
[J].
High-temperature corrosion behavior of superalloys in molten salts-a review
[J].
New developments in materials for molten-salt reactors
[J].
Investigation on corrosion behavior of Ni-based alloys in molten fluoride salt using synchrotron radiation techniques
[J].
Grain boundary engineering for control of tellurium diffusion in GH3535 alloy
[J].
Effects of SO42- ions on the corrosion of GH3535 weld joint in FLiNaK molten salt
[J].
Electrochemical study of the corrosion of a Ni-based alloy GH3535 in molten (Li, Na, K)F at 700 ℃
[J].
Corrosion of 316L stainless steel alloy and hastelloy-N superalloy in molten eutectic LiF-NaF-KF salt and interaction with graphite
[J].
The effect of cold-rolling on the microstructure and corrosion behaviour of 316L alloy in FLiNaK molten salt
[J].
Effect of CrF3 on the corrosion behaviour of Hastelloy-N and 316L stainless steel alloys in FLiNaK molten salt
[J].
Corrosion behavior of Hastelloy N and 316L stainless steel in molten LiF-NaF-KF
[J].
Hastelloy N合金和316L不锈钢在LiF-NaF-KF熔盐中的腐蚀行为研究
[J].
A way to limit the corrosion in the Molten Salt Reactor concept: the salt redox potential control
[J].
Measurement of europium (III)/europium (II) couple in fluoride molten salt for redox control in a molten salt reactor concept
[J].
Redox potential control in molten salt systems for corrosion mitigation
[J].
Validation of corrosion rates measured by the Tafel extrapolation method
[J].
Effects of the oxidants H2O and CrF3 on the corrosion of pure metals in molten (Li, Na, K)F
[J].
Electrochemical investigation of the stable chromium species in molten FLINAK
[J].
Simple analysis of quasi-reversible steady-state voltammograms
[J].