B含量对Mo-Si-B化合物氧化性能的影响已有广泛研究。在早期的研究中,掺杂了1%B (原子分数,下同)的MoSi2在1250 ℃下氧化100 h后,增重为0.72 mg/cm2[13]。也有研究表明[14],在1300 ℃下氧化100 h后,含5%B的Mo-Si-B化合物的增重(0.41 mg/cm2)低于含10%B (0.79 mg/cm2)和15%B (1.58 mg/cm2) Mo-Si-B化合物。Mo-Si化合物中不同B含量导致的抗氧化性显著差异可归因于化合物的微观结构和形成的氧化层的特性的不同。研究还表明[14],当B含量较低时(< 1%),它会溶解在MoSi2相中,当B含量超过5%时,Mo-Si-B化合物中会出现MoB相[14]。Wen等[14]还提出B含量的增加降低了氧化层的粘度,增加了氧气通过氧化层的传输。然而,迄今为止由于缺乏从微观角度对实验结果的模拟与解释,导致B含量对MoSi2抗氧化性影响机制仍然不清楚。本文采用第一性原理来全面揭示不同B含量影响MoSi2抗高温氧化行为的机制,为Mo-Si-B化合物的抗高温氧化设计提供技术支撑和理论指导。
1 计算模型与方法
图1
图1
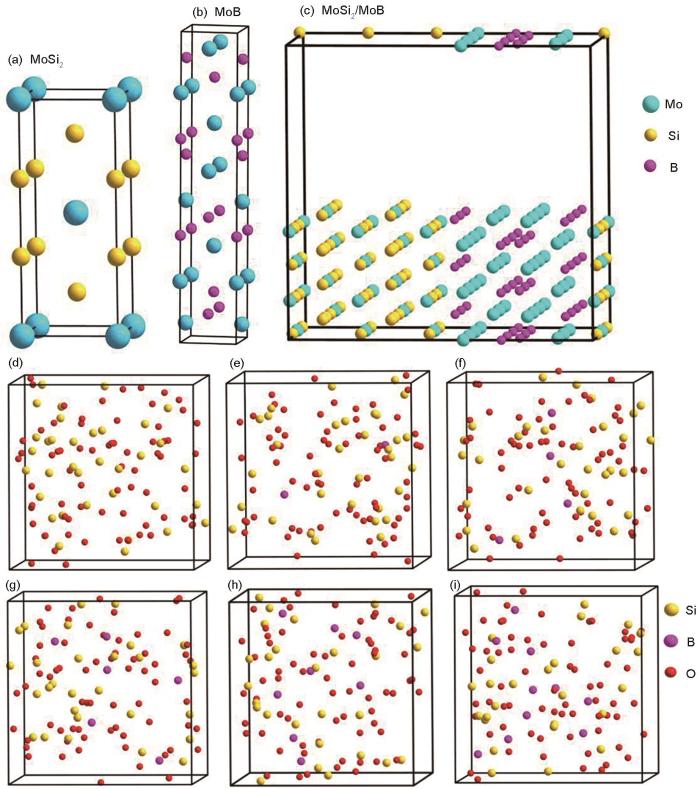
模拟的不同材料原子结构模型
Fig.1
Simulated atomic structure models of different materials: (a) MoSi2 crystal, (b) MoB crystal, (c) MoSi2/MoB interface, and (d-i) amorphous borosilicates containing 0%, 2%, 4%, 6%, 8%, and 10% (atom fraction) B, respectively
对于硼硅酸盐模型的构建,本文通过构建1 nm × 1 nm × 1 nm的晶格模型,然后按照B原子含量为0%、2%、4%、6%、8%和10%的原子配比将0B-34Si-68O、2B-32Si-67O、4B-30Si-66O、6B-28Si-65O、8B-27Si-66O和10B-25Si-65O的原子数放入到1 nm × 1 nm × 1 nm的晶格模型中。因为硼硅酸盐在高温下为非晶态,因而将上述6个模型利用分子动力学(MD)在1700 K熔融温度下充分弛豫,以达到其全局稳定结构,从而确定硼硅酸盐在液态条件下的非晶态,接着在工作温度1523 K温度下再次弛豫,得到其符合实际情况的固态非晶态,如图1d~i所示。
本研究采用了基于密度泛函理论的第一性原理赝势平面波方法,该方法通过使用剑桥连续总能量包(CASTEP)软件实现[17]。在优化和总能量计算中,电子交换相关能量函数使用了包含Perdew-Burke-Ernzerhof (PBE)泛函的广义梯度近似(GGA)[18]。采用的截断能为320 eV,在常规晶胞的布里渊区内使用了至少8 × 8 × 11的k点网格。对于MoSi2/MoB界面模型相关的计算,使用了4 × 4 × 1的k点网格。根据晶胞优化标准,使用Broyden、Fletcher、Goldfarb和Shanno (BFGS)方案[19]对原始晶格中的所有原子位置进行了弛豫。自洽场的收敛标准设定为5.0 ×10-6 eV/atom,能量容差设定为5.0 × 10-7 eV/atom。
2 结果与讨论
2.1 吸附能
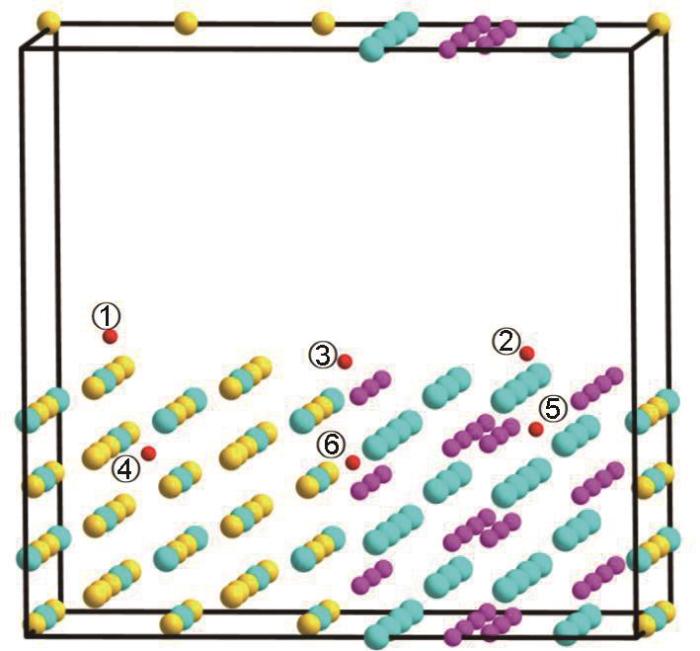
氧化过程总是从氧在化合物表面的吸附和扩散开始。为了模拟这一初始阶段,本文采用分子动力学(MD)方法对1523 K下O占据Mo-Si-B化合物表面和内部位置的表面模型进行弛豫处理,以确定O原子的最稳定位置(图2)。①、②和③代表O原子吸附在MoSi2、MoB和MoSi2/MoB表面上的最稳定位置,而④、⑤和⑥代表O原子占据MoSi2、MoB和MoSi2/MoB内部的最稳定位置。吸附在几个位置上的O原子的吸附能(Ead)通过
其中,Emodel+O代表表面模型上吸附一个O原子的总能量,Emodel是表面模型的能量。E
图2
图2
计算氧吸附能的MoSi2/MoB模型
Fig.2
MoSi2/MoB model for simulating the adsorption energies of oxygen
表1 几个吸附位点的氧吸附能
Table 1
| Model | Position | Eadsorption / eV |
|---|---|---|
| MoSi2/MoB | O occupy surface site of MoSi2① | -6.078 |
| O occupy surface site of MoB② | -6.793 | |
| O occupy surface site of MoSi2/MoB③ | -8.306 | |
| O occupy the site inside MoSi2④ | -6.363 | |
| O occupy the site inside MoB⑤ | -3.004 | |
| O occupy the site inside MoSi2/MoB⑥ | -5.337 |
2.2 扩散激活能
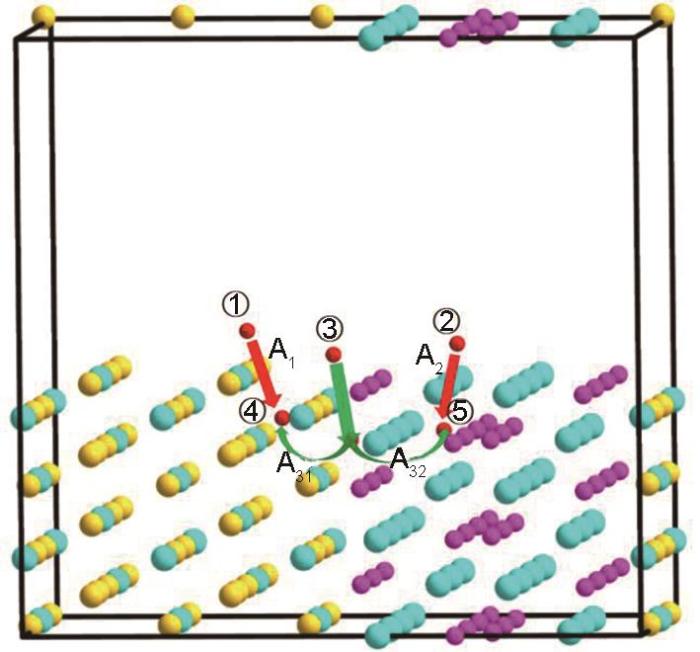
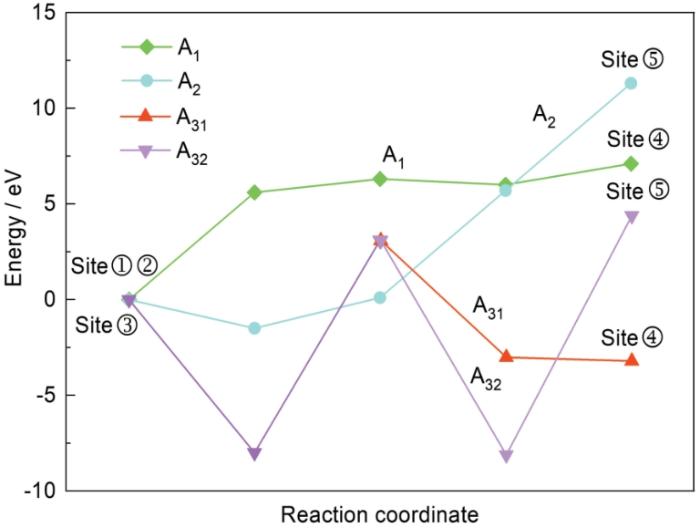
高温氧化过程除了氧吸附在化合物表面以外,也包括氧从化合物表面向化合物内部中扩散。为此本文将模拟和计算MoSi2/MoB界面及周围相的氧的扩散行为。本文采用嵌入在爬坡图像/微调弹性带方法(CI-NEB)中的最小能量路径来计算各种相模型中的氧的扩散。为了研究氧沿MoSi2/MoB界面的扩散,本文讨论了两种不同类型的扩散路径,如图3所示。第一种扩散路径是氧直接从表面扩散到MoSi2和MoB相的内部,即路径A1和A2。路径A1代表氧从位置① (MoSi2表面)扩散到位置④ (MoSi2内部)的反应过程。同样,路径A2代表氧从位置② (MoB表面)扩散到位置⑤ (MoB内部)的反应过程。第二种扩散方法是氧通过MoSi2/MoB界面通道扩散到MoSi2和MoB相的内部,如A31和A32。A31代表氧从MoSi2/MoB表面(位置③)沿MoSi2/MoB界面扩散到MoSi2(位置④),A32代表氧从MoSi2/MoB表面(位置③)沿MoSi2/MoB界面扩散到MoB (位置⑤)。从氧扩散到化合物中的不同途径的扩散激活能(图4)可知,比较A1和A31两种不同的路径,路径A31的扩散激活能(E
图3
图3
计算氧扩散激活能的MoSi2/MoB模型
Fig.3
MoSi2/MoB model for simulating the diffusion activation energies of oxygen
图4
图4
氧沿不同途径扩散到化合物中相应的扩散激活能
Fig.4
Reaction energy profiles of oxygen diffusing into the compound through different pathways
2.3 MoSi2 上硼硅酸盐层的扩散性能
在初始氧化阶段之后,持续的氧化过程主要受氧穿过氧化膜能力的影响。氧化膜中氧的扩散系数在确定化合物的抗氧化性方面起着至关重要的作用,即氧的扩散系数越低,化合物的抗氧化性越高。根据实验结果[20,21],Mo-Si-B化合物上产生的氧化层的主要成分是硼硅酸盐。为了研究不同B含量的硼硅酸盐中不同元素的扩散系数,本文构建了MoSi2晶体被硼硅酸盐覆盖的超胞模型(硼硅酸盐模型为图1d~i所构建模型),其中B含量在0%到10%的范围内,并在1523 K下进行优化以符合实际氧化过程(图5)。原子波函数的开发涉及双数值加d函数基组的利用[22]。为了计算扩散系数(D),本文采用了间隙杂质随机游走模型的假设,并应用了
图5
图5
MoSi2被无定形SiO2 (0%B)及不同B含量的硼硅酸盐覆盖的模型
Fig.5
Models of MoSi2 covered with amorphous SiO2 (0%B) (a) and five borosilicates containing 2% (b), 4% (c), 6% (d), 8% (e) and 10% (f) B
其中Nα为系统中扩散原子的数量,ri (t)为时间t时第i个原子的位置。由表2知,不同B含量的硼硅酸盐中氧的扩散系数(DO)不同。B含量为0%、2%、4%、6%、8%和10%的硼硅酸盐中,氧的扩散系数DO分别为17.987 × 10-8、17.683 × 10-8、17.062 × 10-8、14.192 × 10-8、16.085 × 10-8和17.346 × 10-8 m2/s。由此可见,随着B含量的增加,硼硅酸盐层中氧的扩散系数先降低后增加,在B含量为6%的硼硅酸盐中表现出最低的DO (14.192 × 10-8 m2/s)。此外,本文还计算了B和Si的扩散系数,结果如表2所示。可以看出,Si的扩散系数(DSi)小于B的扩散系数(DB),相对来说B和O原子具有更强的扩散能力。
表2 O、Si和B在不同 B含量的硼硅酸盐中的扩散系数 (m2/s)
Table 2
Diffusivity coefficient | Amorphous SiO2 | 2%B- borosilicate | 4%B- borosilicate | 6%B- borosilicate | 8%B- borosilicate | 10%B- borosilicate |
|---|---|---|---|---|---|---|
| O | 17.987 × 10-8 | 17.683 × 10-8 | 17.062 × 10-8 | 14.192 × 10-8 | 16.085 × 10-8 | 17.346 × 10-8 |
| Si | 5.162 × 10-8 | 5.659 × 10-8 | 6.440 × 10-8 | 6.672 × 10-8 | 5.126 × 10-8 | 4.923 × 10-8 |
| B | - | 10.800 × 10-8 | 13.568 × 10-8 | 12.699 × 10-8 | 14.151 × 10-8 | 11.115 × 10-8 |
2.4 硼硅酸盐的结构稳定性
文献[15]报道高温下MoSi2化合物表面的氧化膜SiO2在热应力的作用下会发生开裂,导致MoSi2化合物的抗氧化性较差,这说明氧化膜的结构稳定性以及流动性都是影响氧化膜抗氧化性能好坏的关键因素。因而首先考虑了不同B含量的硼硅酸盐氧化膜的结构稳定性,通过计算不同B含量的硼硅酸盐的形成焓和结合能,用来表征硼硅酸盐的结构稳定性。硼硅酸盐氧化膜越稳定就越不容易开裂或分解,这对提高硼硅酸盐抗氧化性是有利的。内聚能Ecoadhesive代表晶体分解成原子的功,形成焓Hformation代表着晶体的形成能力,可以用来表征晶体的稳定性,其Ecoadhesive和Hformation的值越负,晶体就越稳定。计算模型如图1c~i所示,相关模型的Ecoadhesive和Hformation计算公式如公式(
表3 不同B含量的硼硅酸盐的形成焓Hformation和内聚能Ecohesive
Table 3
| Models | Ecohesive / eV | Hformation / eV |
|---|---|---|
| Amorphous SiO2 (0%B) | -6.339 | -2.436 |
| 2%B-content in borosilicate | -6.445 | -2.454 |
| 4%B-content in borosilicate | -6.512 | -2.471 |
| 6%B-content in borosilicate | -6.788 | -2.553 |
| 8%B-content in borosilicate | -6.366 | -2.281 |
| 10%B-content in borosilicate | -6.241 | -2.214 |
从计算结果中可以看出,对于不同B含量的硼硅酸盐来说,含量为6%B的硼硅酸盐具有最低的结合能(Ecoadhesive = -6.788 eV/atom)和形成焓(Hformation =-2.553 eV/atom),这说明6%B的硼硅酸盐的结构最为稳定。当硼硅酸盐中B的含量从0%增加到6%时,硼硅酸盐的结构稳定性逐渐增加,然而B的含量从6%增加到10%时,硼硅酸盐的结构稳定性逐渐降低,在6%含量时硼硅酸盐的结构稳定性达到最大值,这说明B含量在6%左右的硼硅酸盐具有最稳定的结构,在热应力下不容易开裂,能够很好的保护基体。
2.5 与实验结果对比分析
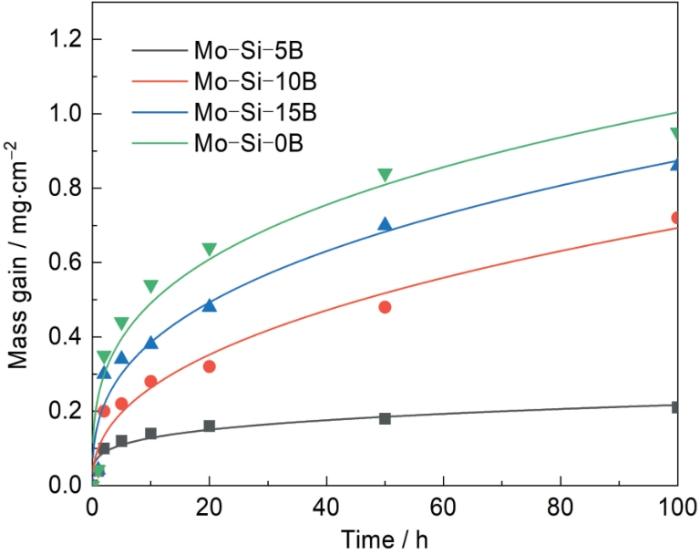
之前的研究表明MoSi2的氧化增重(0.95 mg/cm2)、Mo-60Si-10B (原子分数,%)的氧化增重(0.72 mg/cm2)和Mo-56Si-15B (原子分数,%)的氧化增重(0.86 mg/cm2)要高于掺杂Mo-62Si-5B (原子分数,%)的氧化增重(0.21 mg/cm2)。从结果中可以看出,掺杂B元素的MoSi2的抗氧化性能要优于不掺杂B元素的MoSi2,且B含量为5%时的Mo-Si-B化合物具有更好的抗氧化性能[14]。
从计算结果中可以看出掺杂B元素的MoSi2的优异的抗氧化性主要来源于:在初始氧化阶段,高B掺杂的MoSi2伴随着MoSi2/MoB界面的出现,该界面对氧的吸附能力(Ead③ = -8.306 eV)高于MoSi2(Ead① = -6.078 eV)和MoB (Ead② = -6.793 eV)相。通过对氧向化合物中扩散的扩散激活能的计算可以发现,氧通过MoSi2/MoB界面的扩散能垒最低(ΔE =-3.200 eV),这有利于氧化过程中氧在化合物表面的扩散。以上现象表明,高B掺杂的MoSi2在早期阶段更容易加速表面氧化膜的快速形成,从而提高化合物的抗氧化性。
在初始阶段之后,持续的氧化过程主要受氧通过覆盖化合物表面的硼硅酸盐层的扩散控制。通过对扩散系数的研究,发现含量为6%B的硼硅酸盐表现出最低的氧扩散系数(DO = 14.192 × 10-8 m2/s)。值得注意的是,由于技术限制,无法准确确定硼硅酸盐中的B含量。Yoshimi等[26]提出了一个假设,即硼硅酸盐中的B/Si比通常与Mo-Si-B化合物中的B/Si比一致,从表2的结果中可以看出B的扩散系数近似是Si的两倍,因而实际上Mo-Si-B化合物表面的硼硅酸盐中的B/Si比应该是Mo-Si-B化合物中的B/Si比的两倍左右,在这一假设的基础上,将硼硅酸盐中的B/Si比按照Mo-Si-B化合物中B/Si比的两倍做近似处理可以得出Mo-62Si-5B、Mo-60Si-10B和Mo-56Si-15B化合物表面的硼硅酸盐的B的含量分别为5%、9.4%和15.8%。Mo-62Si-5B化合物氧化后表面形成的硼硅酸中B含量(5%)与计算确定的最佳抗氧化性能的B含量(6%)相当,且与硼硅酸盐稳定性计算中的最稳定的硼硅酸盐的B含量(6%)相当,因而Mo-62Si-5B化合物比Mo-60Si-10B和Mo-56Si-15B化合物有着更好的高温抗氧化性,计算结果与实验结果相一致。
图6
图6
Mo-Si-B化合物1250 ℃静态氧化动力学曲线
Fig.6
Static oxidation kinetics of Mo-Si-B intermetallic compounds containing different contents of B at 1250 oC
3 结论
(1) MoSi2/MoB两化合物界面表现出最高的氧吸附能力和最低的氧扩散能垒。这表明MoSi2/MoB两化合物界面是氧吸附的有利位置,也为氧的扩散提供便利的途径。相应的MoB相对氧的吸附能力也要强于MoSi2相,因而,MoSi2/MoB两化合物界面(主要存在于高B掺杂的Mo-Si化合物中)和MoB相在早期阶段更容易导致化合物表面氧化膜的快速形成,提高化合物的抗氧化性。
(2) 高B掺杂的MoSi2氧化后形成的硼硅酸盐层中的氧扩散系数随着B含量的增加(0%增加到10%)先降低后增加,含量为6%B的硼硅酸盐表现出最低的氧扩散系数DO (14.192 × 10-8 m2/s)。
参考文献
High temperature strength, fracture toughness and oxidation resistance of Nb-Si-Al-Ti multiphase alloys
[J].
Advanced intermetallic alloys-beyond gamma titanium aluminides
[J].
Microstructure and mechanical properties of an advanced niobium based ultrahigh temperature alloy
[J].
The effects of uncommon silicides on the oxidation behavior of alloys from the Nb-Cr-Si system
[J].
A study of the microstructures and oxidation of Nb-Si-Cr-Al-Mo in situ composites alloyed with Ti, Hf and Sn
[J].
Effect of Al, Cr and Ta additions on the oxidation behaviour of Nb-Ti-Si in situ composites at 800 oC
[J].
Effects of B and Si on the fracture toughness of the Nb-Si alloys
[J].
An experimental study on synthesizing submicron MoSi2-based coatings using electrothermal explosion ultra-high speed spraying method
[J].
Formation of Cr-modified silicide coatings on a Ti-Nb-Si based ultrahigh-temperature alloy by pack cementation process
[J].
Hot corrosion behaviour of Mo-62Si-5B (at.%) alloy in different molten salts at 900 oC
[J].
Microstructure evolution and oxidation behavior of B modified MoSi2 coating on Nb-Si based alloys
[J].
Synthesis of oxidation resistant silicide coatings on Mo-Si-B alloys
[J].
Effect of minor B modification on the oxidation behavior of MoSi2 alloy at high temperature
[J].
Microstructural evolution and oxidation behaviour of Mo-Si-B coatings on an Nb-16Si-22Ti-7Cr-2Al-2Hf alloy at 1250 oC prepared by spark plasma sintering
[J].
Intrinsic embrittlement of MoSi2 and alloying effect on ductility: studied by first-principles
[J].
Microstructure, mechanical and tribological properties of in situ MoB reinforced Cu-Al matrix composites
[J].
First-principles simulation: ideas, illustrations and the CASTEP code
[J].
Isothermal oxidation behavior of cryomilled NiCrAlY bond coat: homogeneity and growth rate of TGO
[J].
General methods for geometry and wave function optimization
[J].
Mo-Si-B based coating for oxidation protection of SiC-C composites
[J].
Mo-Si-B alloys for ultrahigh-temperature structural applications
[J].
Analytic energy derivatives in the numerical local-density-functional approach
[J].
High-temperature corrosion mechanism of YSZ coatings subject to calcium-magnesium-aluminosilicate (CMAS) deposits: first-principles calculations
[J].
First-principles prediction of structure, energetics, formation enthalpy, elastic constants, polarization, and piezoelectric constants of AlN, GaN, and InN: comparison of local and gradient-corrected density-functional theory
[J].
A First-principles investigation of structural properties, electronic structures and optical properties of β- and γ-LiAl(SiO3)2
[J].
Oxidation behavior of Mo5SiB2-based alloy at elevated temperatures
[J].