工农业及生活污水的排放、不规范的海洋油气开采与海洋生物养殖活动等会引起海洋环境污染问题,无机氮是我国所辖海域主要污染因素之一[1]。据《2021年中国海洋生态环境状况公报》报道,我国无机氮含量未达到第四类海水水质标准的海域面积为2.1万平方千米,其中辽东湾、渤海湾、长江口、杭州湾、浙江沿岸和珠江口等近岸海域为无机氮污染较严重海域。海水无机氮污染物的存在形式有硝酸盐、亚硝酸盐和铵盐等,其中硝酸盐为主要的无机氮污染物。硝酸盐作为生物生长所必需的重要营养盐,其添加可影响生物活性,进而可能对金属材料的腐蚀产生影响。目前关于硝酸盐影响金属材料腐蚀的研究较多集中在油田采注水系统,少部分研究与近海环境相关。
石油工业常利用硝酸盐的生物竞争作用来抑制采注水系统中的硫酸盐还原菌 (SRB) 腐蚀[2]。大量油田采注水系统的现场实验结果显示,硝酸盐可作为电子受体选择性地刺激群落中具有硝酸盐还原、硫化物氧化功能的细菌 (如脱氮硫杆菌) 的生长,抑制H2S的生成,从而减轻腐蚀性细菌SRB的生物活性起到抑制腐蚀的作用 [3, 4]。但添加硝酸盐抑制腐蚀的有效性受到质疑 [5~7]。陈昊宇等[8]通过模拟胜利油田回注水系统的静态实验,研究了添加不同浓度硝酸盐对N80钢腐蚀的影响,认为当硝酸盐添加浓度为50 mg/L时,N80钢腐蚀速率降低30%;而当硝酸盐添加浓度为80 mg/L时,腐蚀速率增大。Nemati等[9]研究表明,向SRB混合群落中添加10 mmol/L硝酸盐使得碳钢腐蚀速率从1.4提高到2.9 g·m‒2·d‒1。Hubert等[10]研究表明,添加17.5 mmol/L的硝酸盐减少了硫化物的产生却促进了点蚀的发生,并将腐蚀区域从生物反应器出口转移到入口 (即从生产井转移到注入井)。这些争议可能与硝酸盐的添加浓度和环境中群落结构等的差别密切相关。
不同于油田采注水系统的贫氧条件,近海环境往往处于空气饱和状态,溶解O2状态的差异可能会引起硝酸盐对金属材料腐蚀影响的不同。然而,目前鲜有报道关注海水环境中硝酸盐对金属材料腐蚀的影响。Melchers和Jeffrey [11]通过调查认为钢桩发生低水位腐蚀加速的剧烈程度与海水中无机氮 (主要是硝酸盐) 的浓度呈正相关性,并将此归因于无机氮作为营养物质通过促进微生物的生长加剧由微生物活性引发的钢桩的低水位腐蚀加速,然而具体的影响机制还不明确。因此,本工作将研究天然海水环境中添加硝酸盐对EH40钢腐蚀的影响,通过设置多个硝酸盐的添加浓度,较全面地分析硝酸盐浓度对腐蚀的影响,并结合腐蚀产物层中微生物群落结构的变化,解析硝酸盐对腐蚀的作用机制。
1 实验方法
研究所用的EH40船板钢化学组成 (质量分数,%) 为:C 0.086、Si 0.240、Mn 1.490、P 0.011、S 0.001、Nb 0.034、Al 0.034、Mo 0.01、Cu 0.028、Ni 0.013、Cr 0.118、Ti 0.010、V 0.001、N 0.005、余量Fe。浸泡实验所用的EH40钢有两种规格:10 mm×20 mm×5 mm和10 mm×10 mm×5 mm,前者用于挂片实验,后者用于电化学测试,工作面尺寸为10 mm×10 mm。
选取汇泉湾海水作为实验介质,海水中硝酸盐的初始浓度约为1.75 μmol/L。向天然海水中添加不同质量的NaNO3,获得NaNO3的添加浓度分别为0、0.1、1、10和100 mmol/L的介质,采用全浸挂片的方式进行为期12周的浸泡实验。挂片期间,实验箱内的海水温度与室温保持一致 (10~17 ℃),实验体系处于静止、开放状态。为尽可能模拟真实的海水全浸区环境,每隔4~5 d更换补充实验箱内1/4的海水。采用失重法测量浸泡不同时间的EH40钢的腐蚀速率。利用电化学工作站 (Reference 3000) 对不同海水体系中浸泡12周后的EH40钢试样进行动电位极化曲线测试,并利用Tafel区阴极外推法计算腐蚀电流密度 (Icorr)。利用TM3030扫描电子显微镜 (SEM) 对浸泡不同时间EH40钢的腐蚀形貌进行观察。腐蚀产物形貌观察前,首先采用2.5%戊二醛固定,然后依次在30%、50%、70%、90%、100%的乙醇水溶液中梯度脱水,最后超临界干燥并喷金。利用RULTIMA4 X射线衍射仪 (XRD) 和MZ20-FC激光拉曼光谱 (Raman) 对EH40钢试样表面的腐蚀产物成分进行表征。采用OLS5000激光共聚焦显微镜 (CLSM) 对去除腐蚀产物后的EH40钢试样表面的蚀坑形态进行分析。
利用LSM 710激光共聚焦显微镜 (CLSM) 观察于不同体系中浸泡不同时间的EH40钢试样表面的生物膜,观察前使用荧光染料SYTO-11和PI于黑暗环境中进行染色。采用高通量测序法分析EH40钢试样表面腐蚀产物内微生物群落结构的差异。具体步骤包括:微生物组总DNA提取、目标片段 (细菌的16S rRNA基因V3-V4区) PCR扩增、扩增产物磁珠纯化回收、扩增产物荧光定量、测序文库制备 (采用TruSeq Nano DNA LT Library Prep Kit制备测序文库)、上机进行高通量测序和测序结果分析等。
2 结果与讨论
2.1 硝酸盐的添加对EH40钢腐蚀速率的影响
图1为EH40钢在添加0、0.1、1、10和100 mmol/L硝酸盐的海水中腐蚀失重与腐蚀速率随时间的变化曲线。失重曲线显示,随着浸泡时间的延长,不同海水环境中的EH40钢的腐蚀失重均呈现上升趋势。浸泡4周后,海水中不同的硝酸盐添加浓度对EH40钢腐蚀失重的影响逐渐明显,腐蚀失重大小顺序为:添加100 mmol/L≈添加10 mmol/L>添加1 mmol/L>添加0.1 mmol/L≈添加0 mmol/L硝酸盐。由图1b的平均腐蚀速率变化曲线可知,不同体系中试样的腐蚀速率均随着时间的延长而下降,这主要来自腐蚀产物积累带来的腐蚀阻碍作用 [12, 13]。同一浸泡时间下,不同海水环境中试样的平均腐蚀速率随硝酸盐添加浓度的变化规律与腐蚀失重的一致。
图1
图1
EH40钢在添加不同浓度硝酸盐海水中的腐蚀失重及平均腐蚀速率随时间的变化曲线
Fig.1
Variations of corrosion mass loss (a) and average corrosion rate (b) vs time of EH40 steel in seawater added with different concentrations of nitrate
EH40钢在添加有不同浓度硝酸盐的海水中浸泡12周后的动电位极化曲线如图2a所示。可以看出,随着硝酸盐添加浓度的增加阳极钝化区的宽度增加,这可能与硝酸盐使得腐蚀产物量增加有关。图2b为Icorr随硝酸盐添加浓度的变化。硝酸盐的添加浓度为0和0.1 mmol/L时,EH40钢试样的Icorr值接近,且均比较小;随硝酸盐的添加浓度增加至1和10 mmol/L时,EH40钢试样的Icorr值增加;当硝酸盐的添加浓度增大至100 mmol/L时,EH40钢试样的Icorr值增加幅度不大,接近添加10 mmol/L的Icorr值。Icorr值越大,表明腐蚀速率越大,即EH40钢在不同海水中的腐蚀速率大小关系为:添加100 mmol/L≈添加10 mmol/L>添加1 mmol/L>添加0.1 mmol/L≈添加0 mmol/L硝酸盐,与腐蚀失重结果一致。
图2
图2
EH40钢在添加不同浓度硝酸盐海水中浸泡12周后的动电位极化曲线及Icorr变化曲线
Fig.2
Potentiodynamic polarization curves (a) and Icorr (b) of EH40 steel immersed in seawater added with different concentrations of nitrate for 12 weeks
2.2 硝酸盐的添加对EH40钢腐蚀形貌的影响
图3展示了EH40钢在不同海水中浸泡12周后的宏观腐蚀形貌。不同海水环境中试样表面的腐蚀产物均呈黄褐色,添加0和0.1 mmol/L硝酸盐海水中试样的腐蚀产物表面较为疏松,而在添加1、10和100 mmol/L硝酸盐的海水中试样的腐蚀产物表面比较均匀平整。进一步采用SEM对腐蚀产物形貌进行表征,结果见图4。浸泡1周后,不同海水环境中的EH40钢试样表面局部区域出现簇状腐蚀产物,且添加10和100 mmol/L硝酸盐的海水中对应的簇状产物尺寸较大。随浸泡时间的延长,添加0和0.1 mmol/L硝酸盐的海水中试样的表面逐渐被较疏松的粗糙树枝状腐蚀产物完全覆盖,添加10和100 mmol/L硝酸盐的海水中试样的表面主要被堆积较密的团簇状腐蚀产物覆盖,表面较为均匀平整,而添加1 mmol/L硝酸盐的海水中试样的表面既有树枝状的腐蚀产物,也有团簇状的。
图3
图3
EH40钢在添加不同浓度硝酸盐的海水中浸泡12周后的表面腐蚀产物宏观形貌
Fig.3
Images of surface corrosion products of EH40 steel immersed in seawater added with 0 (a), 0.1 (b), 1 (c), 10 (d) and 100 (e) mmol/L nitrate for 12 weeks
图4
图4
EH40钢在添加不同浓度硝酸盐的海水中浸泡不同时间的表面腐蚀产物SEM形貌
Fig.4
SEM images of surface corrosion products of EH40 steel immersed in seawater added with 0 (a1-e1), 0.1 (a2-e2), 1 (a3-e3), 10 (a4-e4) and 100 (a5-e5) mmol/L nitrate for 1 (a1-a5), 2 (b1-b5), 4 (c1-c5), 8 (d1-d5) and 12 (e1-e5) weeks
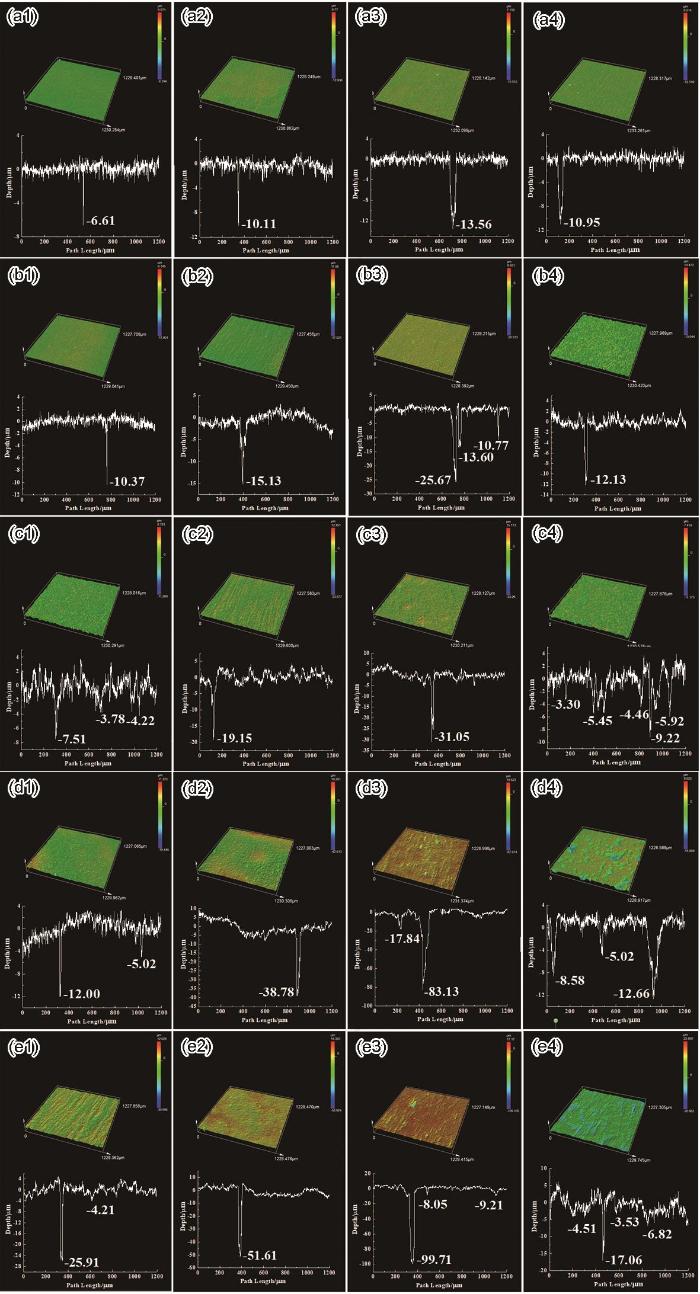
不同海水中浸泡不同时间的EH40钢试样去除腐蚀产物后,在CLSM下观察,结果如图5和6所示。图5为未添加硝酸盐海水中的EH40钢去除腐蚀产物后的CLSM图,在此海水体系中,试样表面未出现较深的蚀坑,整体上表现为均匀腐蚀形貌。图6展示了添加0.1、1、10和100 mmol/L硝酸盐海水中的EH40钢去除腐蚀产物的表面形貌及对应最大蚀坑深度截面轮廓。浸泡初期,在添加0.1 mmol/L硝酸盐的海水中的试样表面蚀坑不明显,最大蚀坑深度变化不大,直至浸泡12周时,表面出现最大深度为25.9 μm的蚀坑。在添加1 mmol/L的硝酸盐海水中的试样浸泡4周时,可在表面观察到最大蚀坑深度为19.2 μm的蚀坑,且表面最大蚀坑深度随着浸泡时间的延长而不断增加,在12周时达到51.6 μm。当硝酸盐的添加量为10 mmol/L时,EH40钢浸泡2周后,表面出现的蚀坑深度最大为25.7 μm,12周后可增至99.7 μm。进一步增加硝酸盐添加浓度至100 mmol/L,EH40钢表面蚀坑的最大深度随时间增加略微增大。此海水体系中的试样浸泡2周时表面比较粗糙;8周时表面蚀坑比较明显且分布范围广,展现出坑蚀形貌;随时间延长至12周,蚀坑进一步扩展并在表面形成明显的凹陷。因此,硝酸盐的添加加剧了EH40钢的局部腐蚀程度,且表面最大蚀坑深度随着硝酸盐添加浓度的增加先增大后减小,海水中添加10 mmol/L硝酸盐时,试样表面的最大蚀坑深度值最大。
图5
图5
EH40钢在未添加硝酸盐的海水中浸泡不同时间去除腐蚀产物后的表面CLSM像
Fig.5
Surface CLSM images of EH40 steel with removal of corrosion products after being immersed in seawater without nitrate addition for 1 (a), 2 (b), 4 (c), 8 (d) and 12 (e) weeks
图6
图6
EH40钢在添加不同浓度硝酸盐的海水中浸泡不同时间去除腐蚀产物后的表面CLSM图及对应最大蚀坑深度截面轮廓图
Fig.6
Surface CLSM images and corresponding maximum pit depth section profiles of EH40 steel with removal of corrosion products after being immersed in seawater added with 0.1 (a1-e1), 1 (a2-e2), 10 (a3-e3) and 100 (a4-e4) mmol/L nitrate for 1 (a1-a4), 2 (b1-b4), 4 (c1-c4), 8 (d1-d4) and 12 (e1-e4) weeks
2.3 硝酸盐的添加对EH40钢腐蚀产物成分的影响
图7
图7
EH40钢在添加不同浓度硝酸盐的海水中浸泡12周后表面腐蚀产物的Raman谱
Fig.7
Raman spectra of corrosion products formed on EH40 steel immersed in seawater added with different concentrations of nitrate for 12 weeks
2.4 硝酸盐的添加对灭菌海水中EH40钢腐蚀失重的影响
前文已经得出了硝酸盐的添加对EH40钢的海水腐蚀有促进作用,为探究硝酸盐促进EH40钢腐蚀的作用机制,进行了为期12周的添加0和10 mmol/L硝酸盐的无菌静态海水挂片实验,定期测定试样的腐蚀失重,结果见图8。实验前两周,添加10 mmol/L硝酸盐的无菌海水中试样的腐蚀失重略高于未添加硝酸盐的。如无菌体系中浸泡1周时,添加10 mmol/L硝酸盐的海水中试样的腐蚀失重约为未添加硝酸盐海水中试样的1.14倍。这种促进作用随着无菌海水浸泡实验进行到第4周时逐渐消失,此时添加10 mmol/L硝酸盐海水中试样的腐蚀失重与未添加硝酸盐海水中试样的几乎一致,而在含有微生物的天然海水中,10 mmol/L的硝酸盐添加使得腐蚀失重增加了0.29倍。随浸泡时间逐渐增加至8、12周时,未添加硝酸盐的无菌海水中试样的腐蚀失重甚至略高于添加10 mmol/L硝酸盐的无菌海水中的试样。因此,天然海水中添加硝酸盐主要增强了EH40钢的微生物腐蚀,即硝酸盐通过作用于海水中的微生物加重了试样的腐蚀程度。
图8
图8
EH40钢在添加不同浓度硝酸盐的灭菌海水中腐蚀失重随时间的变化
Fig.8
Time dependence of corrosion mass loss of EH40 steel in sterile seawater added with different concentrations of nitrate
2.5 硝酸盐的添加对EH40钢生物膜的影响
图9为EH40钢在不同海水中浸泡不同时间后经荧光染料染色后在CLSM下观察得到的图片。图中呈绿色荧光的为活细菌,呈红色荧光的为死细菌。可以看出,在12周的浸泡时间内,试样表面的生物膜主要由活细菌组成,死细菌则较少出现。浸泡1周时,海水中的微生物聚集在试样表面局部区域形成不均匀的生物膜。此时,虽然不同海水环境中试样表面的生物膜厚度较薄,但已呈现出差异,未添加和添加0.1 mmol/L硝酸盐的海水中试样表面的生物膜厚度接近,约为30 μm,添加1、10和100 mmol/L硝酸盐的海水中试样的生物膜厚度较大,分别约为45、53和60 μm。随着浸泡时间的延长,微生物在试样表面的聚集更加明显,不同海水环境中试样表面的生物膜厚度逐渐增加,生物膜厚度间的差异也逐渐明显。如4周时,添加0、0.1、1、10和100 mmol/L硝酸盐的海水中试样的生物膜厚度分别增加至约60、50、88、96和103 μm。浸泡后期,添加不同浓度硝酸盐的海水中试样表面生物膜厚度逐渐稳定,但不同海水环境中试样的生物膜厚度差异依旧明显。因此,硝酸盐的添加促进了EH40钢表面生物膜的生长,且10和100 mmol/L硝酸盐添加的促进作用最强。
图9
图9
EH40钢在添加不同浓度硝酸盐的海水中浸泡不同时间的表面生物膜CLSM像
Fig.9
CLSM images of biofilms formed on EH40 steel immersed in seawater added with 0 (a1-e1), 0.1 (a2-e2), 1 (a3-e3), 10 (a4-e4) and 100 (a5-e5) mmol/L nitrate for 1 (a1-a5), 2 (b1-b5), 4 (c1-c5), 8 (d1-d5) and 12 (e1-e5) weeks
2.6 硝酸盐的添加对EH40钢表面微生物群落结构的影响
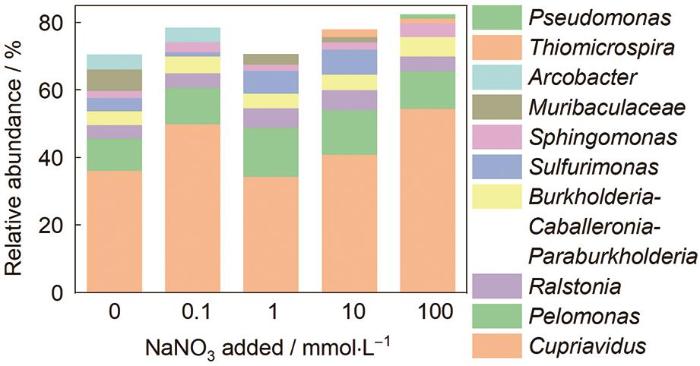
图10展示了在添加不同浓度硝酸盐的海水中浸泡12周后EH40钢表面微生物群落在属分类水平上的组成柱状图 (只显示丰度最高的10个菌属)。可以看出,在所有的海水体系中,EH40钢表面微生物群落丰度最高的菌属皆为Cupriavidus,其次为Pelomonas,隶属于这两个菌属的细菌可进行有氧呼吸 [16, 17]。Ralstonia、Sulfurimonas、Thiomicrospira和Pseudomonas菌属的细菌,既可在有氧环境下以溶解O2为电子受体进行呼吸,又可以在无氧环境下以硝酸盐作为电子受体进行呼吸 [18~23]。海水中未添加硝酸盐时,试样表面微生物群落结构中的硝酸盐还原菌属主要为Ralstonia和Sulfurimonas,其丰度分别为4.0%和3.9%。添加0.1和1 mmol/L硝酸盐时,硝酸盐还原菌属未发生变化,但Ralstonia的丰度分别变为4.2%和5.8%,Sulfurimonas的变为1.3%和6.7%。当硝酸盐的添加量为10 mmol/L时,除Ralstonia (5.8%) 和Sulfurimonas (7.4%) 外,出现了Thiomicrospira菌属,且其丰度为2.2%。进一步增加硝酸盐添加量至100 mmol/L,硝酸盐还原菌属主要为Ralstonia (4.3%)、Thiomicrospira (1.4%) 和Pseudomonas (1.2%)。硝酸盐的添加不仅引起了硝酸盐还原菌属类别的不同,还使得硝酸盐还原菌属的丰度发生变化,添加0、0.1、1、10和100 mmol/L硝酸盐时,其丰度分别为7.9%、5.5%、12.5%、15.4%和6.9%。
图10
图10
EH40钢在添加不同浓度硝酸盐的海水中浸泡12周后表面微生物群落在属分类水平上的比较
Fig.10
Histogram of microbial communities on EH40 steel after being immersed in seawater added with different concentration of nitrate for 12 weeks
浸没于海水中的钢铁材料随着有氧腐蚀的进行与好氧微生物的附着,会使得腐蚀产物的底层处于贫氧环境,进而利于硫酸盐还原菌、硝酸盐还原菌等细菌的生长。而在本研究中,未检测到Desulfovibrio和Desulfuromusa等典型硫酸盐还原菌属,这与实海挂样的结果存在差异 [24],这可能与实验室模拟条件下低的腐蚀速率不利于腐蚀产物的积累有关。Pseudomonas等菌属的硝酸盐还原菌与硫酸盐还原菌相似,均可通过胞外电子传递机制促进钢铁材料的腐蚀,且相较于SO
3 结论
天然海水中硝酸盐的添加能够促进EH40钢的腐蚀过程,且促进作用具有浓度依赖性,腐蚀速率大小关系为:添加100 mmol/L≈添加10 mmol/L>添加1 mmol/L>添加0.1 mmol/L≈添加0 mmol/L硝酸盐。硝酸盐的添加加剧了EH40钢的局部腐蚀程度,且表面最大蚀坑深度随着硝酸盐添加浓度的增加先增大后减小,海水中添加10 mmol/L硝酸盐时,试样表面的最大蚀坑深度值最大。天然海水中硝酸盐添加对EH40钢的腐蚀促进经由微生物起作用,其会改变表面的微生物群落结构,使得表面微生物群落中硝酸盐还原菌属 (Ralstonia、Sulfurimonas、Thiomicrospira和Pseudomonas)的丰度增加、种类分布发生变化,或可形成腐蚀性更强的生物膜。
参考文献
Corrosion of B10 Cu-Ni alloy in seawater polluted by high concentration of NH4 +
[J].
B10铜镍合金在高浓度NH4 +污染海水中腐蚀研究
[J].通过比较B10铜镍合金在天然海水和含10 mg/L NH<sub>4</sub><sup>+</sup>海水中的腐蚀行为,研究NH<sub>4</sub><sup>+</sup>对B10铜镍合金的腐蚀影响机制。采用失重法测量平均腐蚀速率;采用动电位极化分析、电化学阻抗谱 (EIS) 研究界面腐蚀电化学特征;采用扫描电子显微镜 (SEM) 表征腐蚀产物形貌;采用能量色散光谱 (EDS) 和X射线光电子能谱 (XPS) 分析腐蚀产物成分。结果表明,NH<sub>4</sub><sup>+</sup>的添加降低了腐蚀产物中具有保护作用的Cu<sub>2</sub>O成分的含量,提高了B10铜镍合金在海水中的腐蚀速率,促进了点蚀的发生。
Research progress on sulfate-reducing bacteria induced corrosion of steels
[J].
硫酸盐还原菌对钢材腐蚀行为的研究进展
[J].
The influence of nitrate on microbial processes in oil industry production waters
[J].
The effect of long-term nitrate treatment on SRB activity, corrosion rate and bacterial community composition in offshore water injection systems
[J].
The contribution of nitrate-reducing bacterium Marinobacter YB03 to biological souring and microbiologically influenced corrosion of carbon steel
[J].
Influence of nitrate concentrations on EH40 steel corrosion affected by coexistence of Desulfovibrio desulfuricans and Pseudomonas aeruginosa bacteria
[J].
Investigation of carbon steel corrosion by oilfield nitrate- and sulfate-reducing prokaryotes consortia in a hypersaline environment
[J].
Study on the microbiological corrosion in oilfield reinjection water system inhibited by biological competition technology
[J].
生物竞争抑制油田回注水系统微生物腐蚀研究
[J].
Impact of nitrate-mediated microbial control of souring in oil reservoirs on the extent of corrosion
[J].
Corrosion risk associated with microbial souring control using nitrate or nitrite
[J].Souring, the production of hydrogen sulfide by sulfate-reducing bacteria (SRB) in oil reservoirs, can be controlled through nitrate or nitrite addition. To assess the effects of this containment approach on corrosion, metal coupons were installed in up-flow packed-bed bioreactors fed with medium containing 8 mM sulfate and 25 mM lactate. Following inoculation with produced water to establish biogenic H(2)S production, some bioreactors were treated with 17.5 mM nitrate or up to 20 mM nitrite, eliminating souring. Corrosion rates were highest near the outlet of untreated bioreactors (up to 0.4 mm year(-1)). Nitrate (17.5 mM) eliminated sulfide but gave pitting corrosion near the inlet of the bioreactor, whereas a high nitrite dose (20 mM) completely eliminated microbial activity and associated corrosion. More gradual, step-wise addition of nitrite up to 20 mM resulted in the retention of microbial activity and localized pitting corrosion, especially near the bioreactor inlet. We conclude that: (1) SRB control by nitrate or nitrite reduction shifts the corrosion risk from the bioreactor outlet to the inlet (i.e. from production to injection wells) and (2) souring treatment by continuous addition of a high inhibitory nitrite dose is preferable from a corrosion-prevention point of view.
Accelerated low water corrosion of steel piling in harbours
[J].
Corrosion of carbon steel influenced by anaerobic biofilm in natural seawater
[J].
Effect of residual dissolved oxygen on the corrosion behavior of low carbon steel in 0.1 M NaHCO3 solution
[J].
Corrosion behavior of P110S oil casing steel in sulfur containing environment
[J].
P110S油套管在微含硫环境中的腐蚀行为研究
[J].采用不同含量的Na<sub>2</sub>S来模拟不同的含硫环境,利用挂片浸泡实验研究P110S钢级油套管在含硫体系中的腐蚀行为;利用电化学测试研究了其在不同含硫浓度中电化学特征;利用扫描电镜、激光共聚焦、XRD以及拉曼光谱对样品表面的腐蚀产物和形貌进行了表征。结果表明,P110S钢级油套管钢在含硫体系中发生严重的腐蚀,腐蚀速率和腐蚀电流密度均随含硫浓度增大而增大,腐蚀类型由均匀腐蚀转变为点蚀,腐蚀产物疏松。
Raman identification of natural red to yellow pigments: ochre and iron-containing ores
[J].
Cupriavidus necator gen. nov., sp. nov.; a nonobligate bacterial predator of bacteria in Soil
[J].
Augmentation of stimulated Pelomonas aquatica dispersible granules enhances remediation of hexahydro-1, 3, 5-trinitro-1, 3, 5-triazine (RDX) contaminated soil
[J].
Isolation and characterization of strains CVO and FWKO B, two novel nitrate-reducing, sulfide-oxidizing bacteria isolated from oil field brine
[J].\n Bacterial strains CVO and FWKO B were isolated from produced brine at the Coleville oil field in Saskatchewan, Canada. Both strains are obligate chemolithotrophs, with hydrogen, formate, and sulfide serving as the only known energy sources for FWKO B, whereas sulfide and elemental sulfur are the only known electron donors for CVO. Neither strain uses thiosulfate as an energy source. Both strains are microaerophiles (1% O\n 2\n ). In addition, CVO grows by denitrification of nitrate or nitrite whereas FWKO B reduces nitrate only to nitrite. Elemental sulfur is the sole product of sulfide oxidation by FWKO B, while CVO produces either elemental sulfur or sulfate, depending on the initial concentration of sulfide. Both strains are capable of growth under strictly autotrophic conditions, but CVO uses acetate as well as CO\n 2\n as its sole carbon source. Neither strain reduces sulfate; however, FWKO B reduces sulfur and displays chemolithoautotrophic growth in the presence of elemental sulfur, hydrogen, and CO\n 2\n. Both strains grow at temperatures between 5 and 40°C. CVO is capable of growth at NaCl concentrations as high as 7%. The present 16s rRNA analysis suggests that both strains are members of the epsilon subdivision of the division\n Proteobacteria\n, with CVO most closely related to\n Thiomicrospira denitrifcans\n and FWKO B most closely related to members of the genus\n Arcobacter\n. The isolation of these two novel chemolithotrophic sulfur bacteria from oil field brine suggests the presence of a subterranean sulfur cycle driven entirely by hydrogen, carbon dioxide, and nitrate.\n
Complete nucleotide sequence of pHG1: a Ralstonia eutropha H16 megaplasmid encoding key enzymes of H2-based lithoautotrophy and anaerobiosis
[J].The self-transmissible megaplasmid pHG1 carries essential genetic information for the facultatively lithoautotrophic and facultatively anaerobic lifestyles of its host, the Gram-negative soil bacterium Ralstonia eutropha H16. We have determined the complete nucleotide sequence of pHG1. This megaplasmid is 452,156 bp in size and carries 429 potential genes. Groups of functionally related genes form loose clusters flanked by mobile elements. The largest functional group consists of lithoautotrophy-related genes. These include a set of 41 genes for the biosynthesis of the three previously identified hydrogenases and of a fourth, novel hydrogenase. Another large cluster carries the genetic information for denitrification. In addition to a dissimilatory nitrate reductase, both specific and global regulators were identified. Also located in the denitrification region is a set of genes for cytochrome c biosynthesis. Determinants for several enzymes involved in the mineralization of aromatic compounds were found. The genes for conjugative plasmid transfer predict that R.eutropha forms two types of pili. One of them is related to the type IV pili of pathogenic enterobacteria. pHG1 also carries an extensive "junkyard" region encompassing 17 remnants of mobile elements and 22 partial or intact genes for phage-type integrase. Among the mobile elements is a novel member of the IS5 family, in which the transposase gene is interrupted by a group II intron.
Mechanisms of high salinity tolerance in plants
[J].
The effect of Ralstonia pickettii on environmental fatigue crack growth of 7xxx series aluminum alloys
[J].
Microbiologically influenced corrosion of C1018 carbon steel by nitrate reducing Pseudomonas aeruginosa biofilm under organic carbon starvation
[J].
Microbiologically influenced corrosion of welded AISI 304 stainless steel pipe in well water
[J].