关于pH值等因素对B30铜镍合金的成膜,国内外进行了一定的研究,Ekerenam等[21]和迟长云[22]等认为铜镍合金在pH<3的溶液中,由于pH值过低,材料表面无法形成Cu2O表面膜,随着pH值提高,腐蚀反应速度有所减小。李海舰等[23]和徐群杰等[24]认为腐蚀产物膜在较低温度下形成较好,随着温度的增加,B30铜镍合金的耐蚀性会有一定程度的降低。朱小龙等[25]在90Cu-10Ni合金腐蚀产物分析表明,随氯量降低,点蚀速度减小,在一定范围内随着盐度提高,Cl-的存在会影响形成的腐蚀产物,不易形成稳定的钝化膜。Ismail等[26]研究表明当盐度增大到一定数值时,反而利于Cu2O的生成,表面膜层致密性有所提升。
国内外对B30铜镍合金在不同海水环境中的腐蚀机制已有广泛研究,但针对实际海域中海水的pH、温度以及盐度的变化对B30铜镍合金表面成膜的研究较少,对不同海水环境中B30铜镍合金表面的成膜质量缺乏明确评价标准。本文以B30铜镍合金作为研究对象,针对实际海域中海水的pH、温度以及盐度所处的范围,通过改变海水中的pH值、温度和盐度,研究B30铜镍合金在不同海水中的腐蚀状况以及成膜机理,分析这3种因素对于成膜的影响,对实际工况中成膜工艺进行指导,帮助解决船用冷凝器存在的孔蚀问题。
1 实验方法
本文研究对象为B30铜镍合金,其主要成分 (质量分数,%) 为:Ni+Co 29~33,C 0.05,Fe 0.9,Mn 1.2,Pb 0.05,Si 0.15,P 0.006,S 0.01,Cu余量。电化学试样规格:10 mm×10 mm×3 mm,保留1 cm2工作面,其他面用环氧树脂进行密封处理。表面观察试样规格:50 mm×10 mm×3 mm。试样表面依次用800#、1000#、2000#的砂纸进行打磨。打磨完成的试样依次用蒸馏水和无水乙醇中冲洗,结束后吹干备用。
实验介质为青岛沙子口海域天然海水,海水的初始pH为7.8,温度为25 ℃,盐度为30,改变其中一个因素时其他因素保持不变。pH通过添加HCl和NaOH来调整,分别为6.6±0.1、8.4±0.1、9.8±0.1;温度通过水浴锅及低温冷水浴的方式控制,分别为2±2 ℃、13±2 ℃、25±2 ℃、36±2 ℃;盐度通过添加蒸馏水和蒸发的方式改变,分别为20±1、28±1、36±1。
采用Gamry reference 600+电化学工作站进行电化学测试,采用三电极体系,工作电极为在不同海水体系中预处理后的B30铜镍合金,参比电极为饱和甘汞电极 (SCE),辅助电极为混合金属氧化物电极 (MMO)。电化学阻抗 (EIS) 的测试在开路电位 (OCP) 下进行,施加幅值为10 mV的正弦波电位,扫描频率范围为105~10-2 Hz。动电位极化曲线扫描范围为-800~1200 mV (vs. OCP),扫描速率为0.334 mV/s,从阴极向阳极方向扫描。采用ESCALAB 250Xi X射线光电子能谱 (XPS) 对保护膜成分进行分析。采用Keyence-VK-X200的激光共聚焦显微镜进行表面观察。
2 结果与分析
2.1 pH对B30铜镍合金成膜的影响
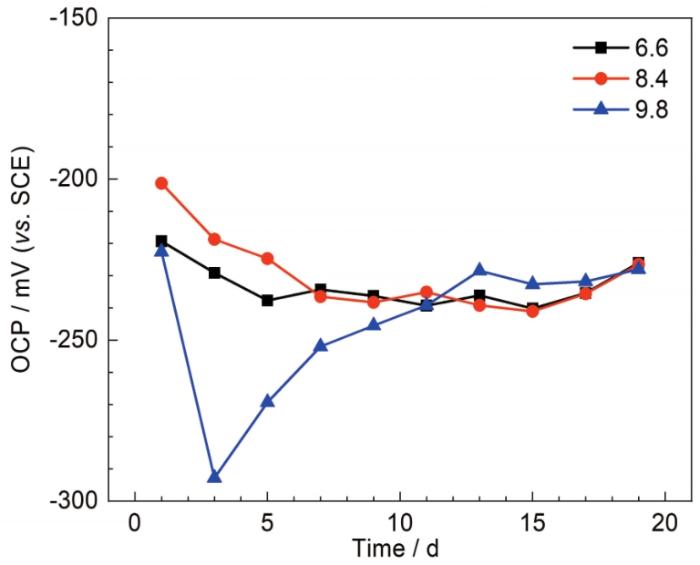
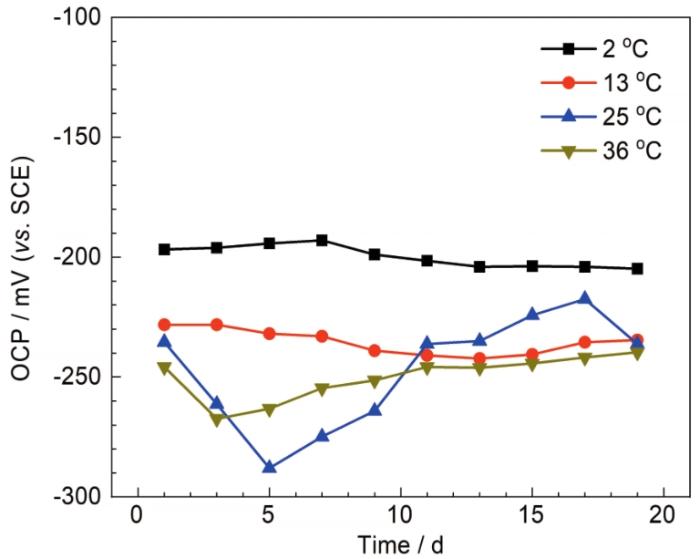
pH的变化会影响试样表面膜层的形成,图1为B30铜镍合金在不同pH海水中的OCP图。由OCP可以看出,在pH为6.6和8.4的海水中,OCP在1~5 d时,OCP发生负移,腐蚀倾向增大,两者相较而言,pH为6.6时腐蚀倾向更大;7~15 d时,OCP趋于平稳,15 d后腐蚀倾向有一定的上升,此时形成了较为致密的保护膜,腐蚀倾向减小。pH为9.8时,1~3 d,OCP急剧下降,这是由于B30铜镍合金放入海水中,由于合金中的镍的标准电极电位较铜负,和Cu有较大的电位差,容易发生腐蚀,但是在强碱性介质溶液中,镍的钝化能力增强,导致铜的溶解,发生十分严重的脱Cu腐蚀,3~13 d,OCP正移,表面缓慢成膜,腐蚀倾向较小,由OCP的变化趋势可以看出,pH为9.8时,试样表面初期腐蚀严重且成膜缓慢。
图1
图1
B30铜镍合金在不同pH海水中的OCP图
Fig.1
Open circuit potentials of B30 copper-nickel alloy in seawater with different pH
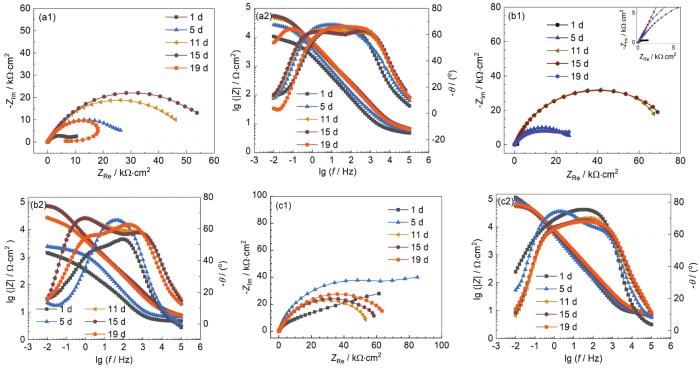
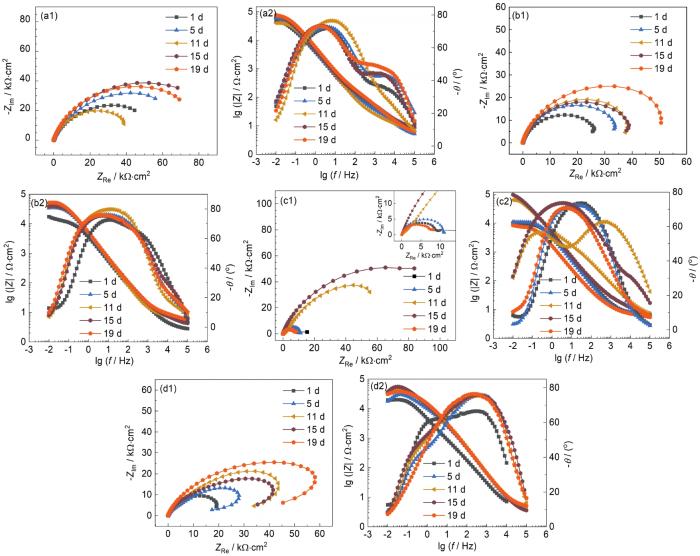
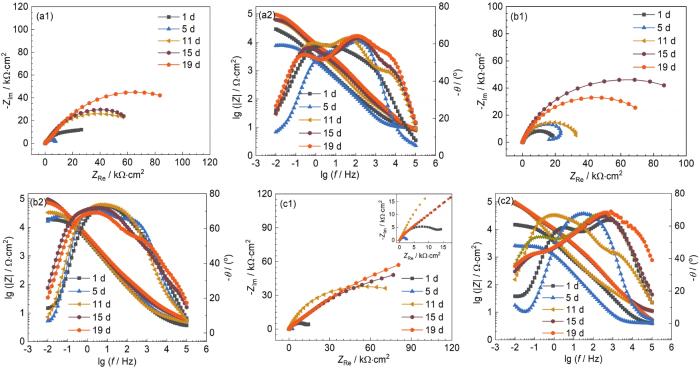
由图2 Nyquist图可以看出,在不同pH海水中,1~15 d容抗弧半径均处于波动增大的状态;19 d时,在pH为6.6和8.4的海水环境中,容抗弧出现下降的趋势,此时膜层不稳定,膜层保护性下降,随着pH的提高,当pH到达9.8时,前期虽然出现波动溶解状态,5~11 d出现下降的趋势,但后期形成的膜层保护效果更佳且膜层更为稳定不易溶解。
图2
图2
B30铜镍合金在不同pH值海水中的EIS图
Fig.2
Nyquist (a1-c1) and Bode (a2-c2) diagrams of B30 copper-nickel alloy in seawater with the pH 6.6 (a1, a2), 8.4 (b1, b2) and 9.8 (c1, c2)
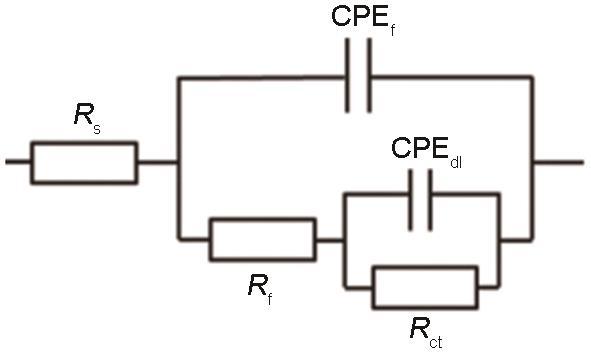
图3为B30铜镍合金在海水中交流阻抗拟合等效电路图。Rs是溶液电阻,Rct是电极反应的电荷转移电阻,Rct值可以反映试样表面发生反应的难易程度;Rf为膜电阻;CPEf由膜电容Cf和弥散指数nf组成,nf的值代表常相位角原件 (CPE) 偏离理想电容器的程度,也就是偏离一个完美光滑电极的程度,对于电化学分析时用来表征表面膜层的不均一性,当nf趋近于1时,均一性越高。CPEdl由双电层电容Cdl和弥散指数ndl组成。
图3
图3
B30铜镍合金在海水中电化学阻抗拟合等效电路图
Fig.3
Equivalent circuit diagram for fitting EIS of B30 copper-nickel alloy in seawater
表1 B30铜镍合金在不同pH的海水中浸泡不同时间的EIS的拟合数据
Table 1
| pH | t / d | Rct / Ω·cm2 | nd | Rf / Ω·cm2 | nf |
|---|---|---|---|---|---|
| 6.6 | 1 | 9514 | 0.717 | 2.923 | 0.947 |
| 5 | 28750 | 0.781 | 53.72 | 0.776 | |
| 11 | 52025 | 0.850 | 2492 | 0.748 | |
| 15 | 61315 | 0.802 | 2613 | 0.753 | |
| 19 | 10630 | 0.947 | 1501 | 0.804 | |
| 8.4 | 1 | 1774 | 0.476 | 73.14 | 0.789 |
| 5 | 32165 | 0.406 | 1204 | 0.802 | |
| 11 | 91373 | 0.911 | 1341 | 0.737 | |
| 15 | 91055 | 0.893 | 1127 | 0.735 | |
| 19 | 27023 | 0.612 | 2668 | 0.742 | |
| 9.8 | 1 | 49130 | 0.891 | 161.6 | 0.869 |
| 5 | 107000 | 0.980 | 755.6 | 0.807 | |
| 11 | 62110 | 0.827 | 125.3 | 0.764 | |
| 15 | 71490 | 1.000 | 154.2 | 0.760 | |
| 19 | 47090 | 0.997 | 273.1 | 0.764 |
试样1~5 d发生腐蚀,试样表面覆盖疏松的CuCl盐膜 (
随着pH的提高,溶液中OH-浓度增大,试样表面成膜速度较快,在5 d时形成了具有保护性的保护膜,并且形成的膜层稳定 (
图4
图4
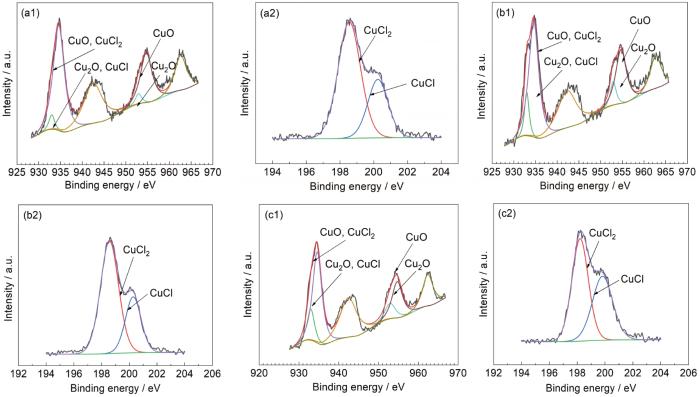
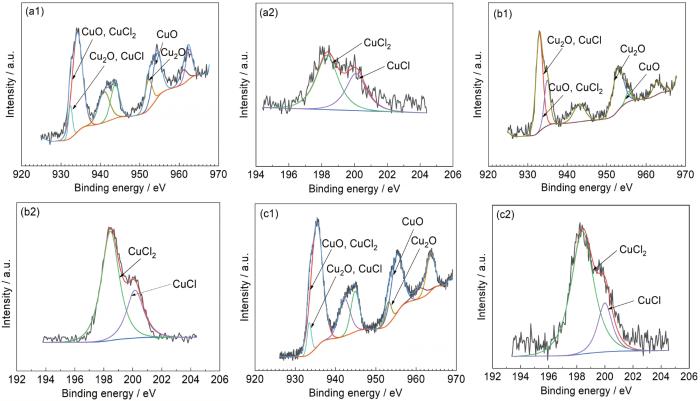
B30铜镍合金在不同pH值海水中浸泡20 d后表面的XPS分析结果
Fig.4
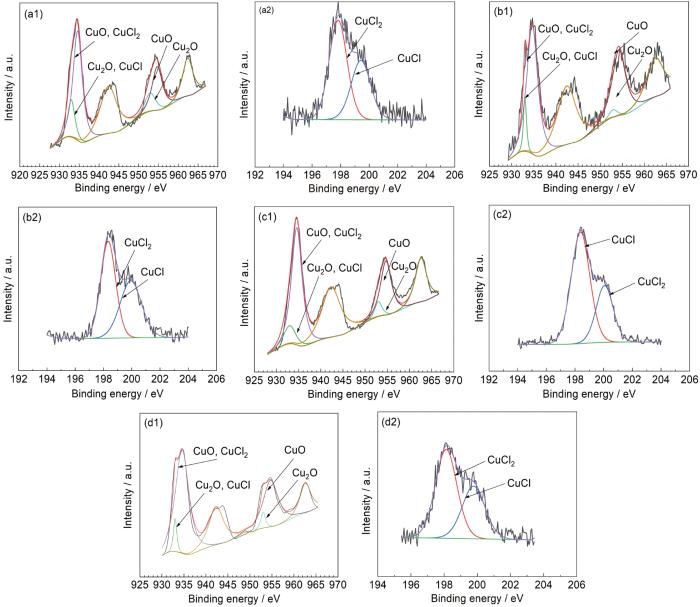
XPS diagrams of B30 copper-nickel alloy in seawater with the pH 6.6 (a1, a2), 8.4 (b1, b2) and 9.8 (c1, c2) for 20 d
表2 B30铜镍合金在不同pH海水中浸泡20 d后表面XPS的拟合结果
Table 2
| Element | Compound | pH | ||
|---|---|---|---|---|
| 6.6 | 8.4 | 9.8 | ||
| Cu | CuO, CuCl2 | 92.48 | 83.86 | 76.33 |
| Cu2O, CuCl | 7.52 | 16.14 | 23.67 | |
| Cl | CuCl2 | 68.91 | 66.77 | 61.53 |
| CuCl | 31.09 | 33.23 | 38.47 | |
表2为B30铜镍合金在不同pH值海水中浸泡20 d的XPS拟合数据。在实际工况中,海水的pH为6.6~9.8,由表中数据可以看出,在实际工况的范围内,随着pH的增大,Cu2O的比例有一定的提高,但并不明显,且并未出现pH过低或过高导致试样表面膜层无法形成的现象。由试样表面成膜发生的反应可知,当pH到达9.8时,试样初期腐蚀严重,后期试样表面较难持续形成CuO以及Cu2O的保护膜,因此即使XPS拟合数据显示其Cu2O和CuCl的含量高,但其表面膜层较薄,保护效果较差。相较而言,试样在pH为8.4的海水中,形成的膜层厚度以及致密性更佳。
图5为B30铜镍合金在不同pH海水中浸泡20 d后表面的激光共聚焦显微图像。由图可见,在成膜的过程中,pH为6.6的海水中,试样基体会发生点蚀,点蚀深度达到了12 nm;当pH升高至8.4和9.8时,基底发生均匀腐蚀;当pH到达9.8时,基底腐蚀程度有所减缓。
图5
图5
B30铜镍合金在不同pH海水中浸泡20 d后表面的激光共聚焦显微图像
Fig.5
CLSM images of B30 copper-nickel alloy after 20 d of immersion in seawater with the pH (a) 6.6, (b)8.4, (c) 9.8 and the depth of pit at the circles in Fig.5a (d)
2.2 温度对B30铜镍合金成膜的影响
由于所处地域的不同,各地海水的温度也不相同,主要范围处于2~36 ℃,在此范围内研究B30铜镍合金在不同温度的海水环境中的成膜,图6为B30铜镍合金在不同温度海水中的OCP图。由图6可以看出,2和13 ℃ OCP较为稳定,2 ℃时OCP最正,腐蚀倾向明显小于其他温度海水。温度为25 ℃时,相较2和13 ℃时,1~5 d OCP发生明显负移,这是由于随着温度的提高,离子转移速度加快,试样会产生较大的腐蚀倾向;5~11 d,OCP发生负移,试样表面逐渐成膜,但形成的膜层质量并不稳定,所以后期OCP会出现上下波动的情况,此时膜层处于形成与溶解的变化过程。温度为36 ℃时,1~3 d,OCP负移,腐蚀倾向变大,且较其他温度腐蚀倾向最大;3~19 d,OCP开始正移,腐蚀倾向变小且比较稳定,说明此温度下虽然前期腐蚀倾向较大,但后期成膜后还是较为稳定的。
图6
图6
B30铜镍合金在不同温度海水中的OCP图
Fig.6
Open circuit potentials of B30 copper-nickel alloy in seawater at different temperatures
图7
图7
B30铜镍合金在不同温度海水中的电化学阻抗图
Fig.7
Nyquist (a1-d1) and Bode (a2-d2) diagrams of B30 copper-nickel alloy in seawater at 2 ℃ (a1, a2), 13 ℃ (b1, b2), 25 ℃ (c1, c2) and 36 ℃ (d1, d2)
由Bode图可以看出,2 ℃时初期就形成了两个相位角峰,形成了两层膜,随着时间的增大,高频区的峰值有一定的提高,13 ℃时两个相位角峰并不明显,25 ℃在11~15 d时形成了两个较为明显的相位角峰,但高频区的相位角峰不稳定,11~19 d,高频区峰值逐渐降低,膜层致密性降低。36 ℃出现了两个峰,试样表面成膜,但可以看出高频区的峰位置不如2 ℃时频率高,此温度下形成的膜层不如低温下形成的膜层致密。
表3为图7 B30铜镍合金在不同温度海水中的EIS图经图3所示的拟合电路图拟合所得。由Rf值可以看出,在2~25 ℃时,随着温度的升高,溶解氧浓度的改变,成膜过程减缓,膜层质量降低,Rf值逐渐减小。当温度到达36 ℃时,由于温度过高,离子转移速度加快,从而导致腐蚀更加严重,表面形成的腐蚀产物膜加厚,从而使Rf值增大。由Rct的拟合结果可以看出,温度为2和13 ℃时,随着温度的降低,溶解氧浓度有一定的提高,更容易成膜,成膜造成的阻碍阳极溶解过程,Rct值变大。温度到达25 ℃时,随着温度的升高,饱和溶解氧浓度的改变也会减小,而由于温度的升高造成的电子转移速率增大,其产生的影响会增大,腐蚀加剧,此时试样表面成膜,但形成的膜层并不稳定。温度到达36 ℃时,由于温度的升高,海水中的生物活性增强,离子扩散速率加大,试样的极化电流密度增大。腐蚀加剧导致试样表面成膜更加快速,且能够持续稳定的成膜,膜层较厚。对比温度为2 ℃与36 ℃形成的两种膜层,2 ℃时Rct最大,这是由于虽然36 ℃形成的膜层Rf值较大,但只是因为试样腐蚀严重,表面形成膜层较厚,但其膜层致密性较差,对于阳极溶解过程阻碍小,Rct值小。此时试样仍然会发生腐蚀,膜层无法形成一个较好的保护作用。
表3 B30铜镍合金在不同温度海水中的电化学阻抗拟合数据
Table 3
| Temperature / ℃ | t / d | Rct / Ω·cm2 | ndl | Rf / Ω·cm2 | nf |
|---|---|---|---|---|---|
| 2 | 1 | 66730 | 0.878 | 82.16 | 0.705 |
| 5 | 88710 | 0.878 | 77.57 | 0.727 | |
| 11 | 47630 | 0.884 | 26.22 | 0.804 | |
| 15 | 107700 | 0.901 | 176.5 | 0.732 | |
| 19 | 98000 | 0.879 | 199.3 | 0.752 | |
| 13 | 1 | 15030 | 0.799 | 27.61 | 0.837 |
| 5 | 38870 | 0.857 | 11.53 | 0.867 | |
| 11 | 42350 | 0.897 | 5.653 | 0.897 | |
| 15 | 44100 | 0.842 | 13.11 | 0.859 | |
| 19 | 602 | 0.847 | 9.796 | 0.858 | |
| 25 | 1 | 9829 | 0.947 | 30.87 | 0.822 |
| 5 | 11796 | 0.838 | 7.337 | 0.849 | |
| 11 | 11244 | 0.727 | 9.441 | 0.738 | |
| 15 | 143610 | 0.824 | 19.42 | 0.758 | |
| 19 | 8783 | 0.815 | 6.688 | 0.783 | |
| 36 | 1 | 21040 | 0.806 | 1928 | 0.798 |
| 5 | 20080 | 0.815 | 6981 | 0.860 | |
| 11 | 41300 | 0.717 | 7997 | 0.863 | |
| 15 | 43620 | 0.786 | 11830 | 0.852 | |
| 19 | 26130 | 0.680 | 13760 | 0.860 |
图8为B30铜镍合金在不同温度海水中浸泡20 d后表面的XPS谱。表4为XPS拟合后的表面成膜物质及其含量。由表中数据可以看出,随着温度的降低,Cu2O和CuCl所占的比例有所提高。这是由于随着温度的降低,海水环境中的饱和溶解氧浓度会有所提升。温度低于13 ℃时,不同温度Cu2O和CuCl的占比差距较大;温度高于13 ℃时,不同温度的Cu2O和CuCl的占比差距并不大,原因是因为海水中的饱和溶解氧在低温区的差距较为明显,并且在13~36 ℃时,随着温度的提高,溶解氧的扩散也会有一定的提升,因此不同温度下饱和溶解氧的差距导致的材料表面的溶解氧的变化并不明显。由数据可以得出,温度的差距在一定程度上会影响形成膜层的质量,温度2 ℃形成的表面膜层成分致密性最好[19],温度超过一定数值时,温度对其成分组成的影响并不大。
图8
图8
B30铜镍合金在不同温度海水中浸泡20 d后表面的XPS图谱
Fig.8
XPS diagrams of B30 copper-nickel alloy after immersion in seawater at 2 ℃ (a1, a2), 13 ℃ (b1, b2), 25 ℃ (c1, c2) and 36 ℃ (d1, d2) for 20 d
表4 B30铜镍合金在不同温度海水中浸泡20 d后表面成膜物质及其含量
Table 4
| Element | Compound | Temperature / ℃ | |||
|---|---|---|---|---|---|
| 2 | 13 | 25 | 36 | ||
| Cu | CuO, CuCl2 | 85.25 | 91.14 | 91.44 | 91.96 |
| Cu2O, CuCl | 14.75 | 8.86 | 8.56 | 8.04 | |
| Cl | CuCl2 | 61.42 | 52.83 | 61.53 | 61.30 |
| CuCl | 38.58 | 47.17 | 38.47 | 38.70 | |
由图9可见,在2~25 ℃时,随着温度的升高,B30铜镍合金基底的腐蚀程度有所增大;当温度到达36 ℃时,由于表面形成了较厚的膜层,后期也对基体有一定的保护作用,腐蚀程度有一定的减轻,但基底的腐蚀程度还是比2 ℃时的严重。
图9
图9
B30铜镍合金在不同温度海水中浸泡20 d后表面的激光共聚焦显微镜图
Fig.9
CLSM diagrams of B30 copper-nickel alloy after immersion in seawater at 2 ℃ (a), 13 ℃ (b), 5 ℃ (c) and 36 ℃ (d) for 20 d
2.3 盐度对B30铜镍合金成膜的影响
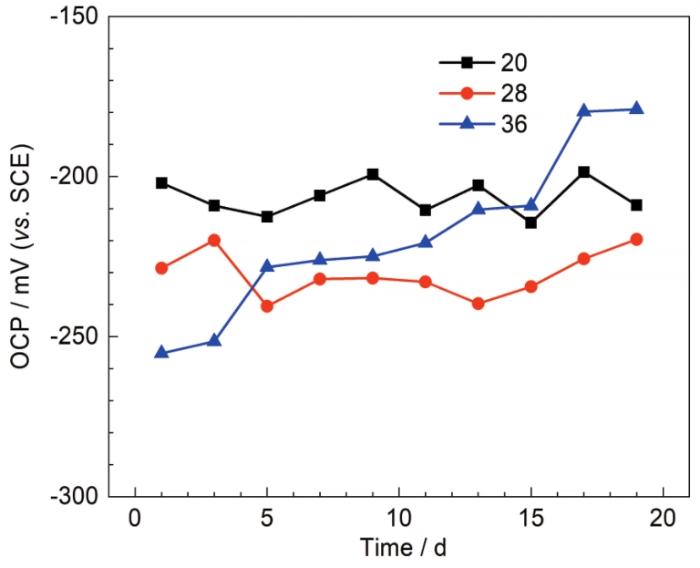
图10为B30铜镍合金在不同盐度海水中的OCP图。由图可见,盐度为20和28时,OCP变化较小且稳定,盐度为20时比28时OCP更正,腐蚀倾向更小。盐度为36时,1~3 d时,OCP相较其他盐度更负,腐蚀倾向更大,5~19 d,OCP逐渐正移,腐蚀倾向减小,在15 d时甚至比盐度20时更正,说明在高盐度的环境中,试样在成膜后期也能够形成具有保护性的膜层。
图10
图10
B30铜镍合金在不同盐度海水中的OCP
Fig.10
Open circuit potentials of B30 copper-nickel alloy in seawater with different salinities
图11为B30铜镍合金在不同盐度海水中的EIS图。由Nyquist图可见,盐度从20到28,随着盐度的增大,容抗弧半径逐渐减小,这是由于材料表面形成的CuCl盐膜在盐度提升的情况下更容易形成可溶性物质CuCl2- (
图11
图11
B30铜镍合金在不同盐度海水中的EIS图
Fig.11
Nyquist (a1-c1) and Bode (a2-c2) diagrams of B30 copper-nickel alloy in seawater with different salinities of 20 (a1, a2), 28 (b1, b2) and 36 (c1, c2)
表5为B30铜镍合金在不同盐度海水中的EIS图经图3所示的等效电路拟合所得数据。由Rf值可以看出,盐度为28时,膜层初期处于波动溶解阶段,5~11 d出现下降的趋势,15 d时已经趋于稳定;盐度为28时,1~5 d呈现波动溶解状态,随时间增长,膜层逐渐形成。盐度从20到28,随着盐度的增大,Rf值减小,一是由于随着盐度的增大,海水中的溶解氧含量降低,二是由于随着盐度的增大,Cl-的含量也会有一定程度的提高,从而会影响形成的腐蚀产物的种类,表面膜层的致密性、稳定性下降。当盐度为36时,由于Cl-浓度过高,表面容易形成了较厚的盐膜,并且高盐度下也更容易形成Cu2O,从而使得Rf值较大,抑制阳极溶解反应[39],由于初期盐膜属于疏松多孔的物质,并且也会生成可溶性的CuCl2-,因此在5~11 d时会出现Rf值下降的现象。
表5 B30铜镍合金在不同盐度的海水中的电化学阻抗拟合数据
Table 5
| Salinity | t / d | Rct / Ω·cm2 | nd | Rf / Ω·cm2 | nf |
|---|---|---|---|---|---|
| 20 | 1 | 37180 | 0.742 | 355.5 | 0.675 |
| 5 | 8250 | 0.650 | 789.3 | 0.791 | |
| 11 | 89239 | 0.676 | 151.1 | 0.792 | |
| 15 | 73720 | 0.912 | 15370 | 0.688 | |
| 19 | 122000 | 0.784 | 14360 | 0.718 | |
| 28 | 1 | 21020 | 0.826 | 24.9 | 0.819 |
| 5 | 29064 | 0.809 | 9.4 | 0.798 | |
| 11 | 37040 | 0.832 | 10.1 | 0.844 | |
| 15 | 131300 | 0.812 | 37.0 | 0.791 | |
| 19 | 96590 | 0.817 | 132 | 0.754 | |
| 36 | 1 | 15580 | 0.701 | 555 | 0.795 |
| 5 | 61710 | 0.812 | 2570 | 0.799 | |
| 11 | 118600 | 0.777 | 134 | 0.732 | |
| 15 | 203500 | 0.545 | 7860 | 0.754 | |
| 19 | 323700 | 0.513 | 7770 | 0.758 |
由Rct值可以看出,盐度为20时,Rct在11 d时达到稳定状态;盐度为28时,相对于盐度20,形成稳定的膜层较慢;盐度为36时,试样表面Rct值逐渐增大,比较稳定,这是由于高盐度形成的CuCl盐膜以及进一步生成的Cu2O导致膜层不断增厚,使得Rct值较大。
图12为B30铜镍合金在不同盐度海水中浸泡20 d后的XPS。表6为XPS拟合后的结果。由表中数据可以看出,盐度从20到28,随着盐度的提升,Cu2O和CuCl的所占的比例有所降低,而CuO和CuCl2所占的比例有所提高。这是由于随着海水中含盐量的提高,Cl-的浓度也会有一定的提高,从而使腐蚀产物发生变化,CuCl浓度的提高,有利于材料表面形成致密的Cu2O保护膜,而CuCl2浓度的提高,则代表材料表面更容易形成疏松且保护性差的CuO和Cu2(OH)3Cl。盐度从28到36,随着盐度的增加,Cu2O和CuCl的含量再次增大,但Cl-浓度增大到一定值时,CuCl含量的提高,进而促进表面膜层致密氧化物Cu2O的生成[40],这点与电化学交流阻抗数据相符。由数据可以看出随着盐度的提高,表面膜层形成的保护效果呈现先变差后变好的趋势。
图12
图12
B30铜镍合金在不同盐度海水中浸泡20 d后表面的XPS图
Fig.12
XPS diagrams of B30 copper-nickel alloy after immersion in seawater with different salinities of 20 (a1, a2), 28 (b1, b2) and 36 (c1, c2) for 20 d
表6 B30铜镍合金在不同盐度海水中浸泡20 d的XPS图拟合结果
Table 6
| Element | Compound | Salinity | ||
|---|---|---|---|---|
| 20 | 28 | 36 | ||
| Cu | CuO, CuCl2 | 75.86 | 89.14 | 82.64 |
| Cu2O, CuCl | 24.14 | 10.86 | 17.36 | |
| Cl | CuCl2 | 65.05 | 66.39 | 63.94 |
| CuCl | 34.94 | 33.61 | 36.06 | |
图13为B30铜镍合金在不同盐度海水中的基底图,由图可以看出在盐度为20的海水中,试样基底仍然可以看出清晰的试样抛光划痕,基底几乎没有发生腐蚀,在盐度为28的海水中,试样发生大片区域的腐蚀,腐蚀加剧,当盐度到达36时,试样基底大片区域的腐蚀连接成片,基底几乎被腐蚀掉一层。
图13
图13
B30铜镍合金在不同盐度海水中浸泡20 d后表面的激光共聚焦显微镜图
Fig.13
CLSM diagrams of B30 copper-nickel alloy after immersion in seawater with the salinities of 20 (a), 28 (b) and 36 (c) for 20 d
2.4 B30铜镍合金在不同海水中的膜层评测
图14
图14
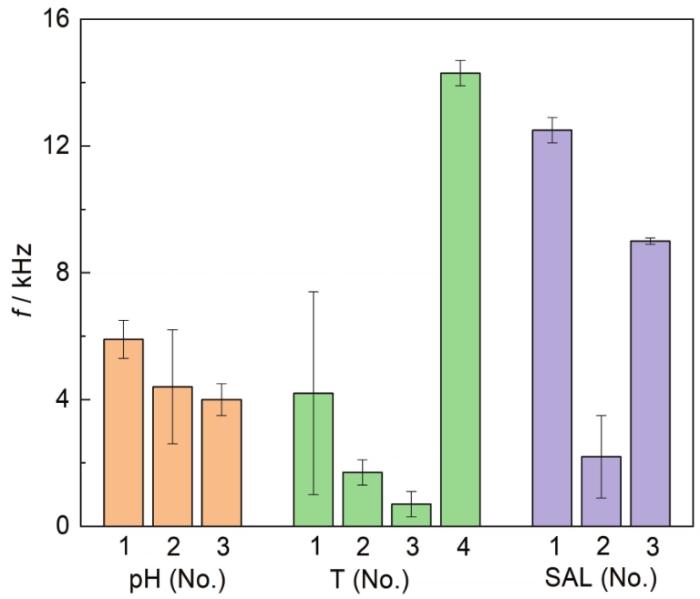
B30铜镍合金在不同海水中的相位角-45°所对应的频率值
Fig.14
Diagram of frequency values corresponding to the phase angle -45° for B30 copper-nickel alloy in seawater under different conditions
表7 B30铜镍合金在不同条件的海水中的相位角-45°所对应的频率值
Table 7
| f / kHz | pH (No.) | Temperature / ℃ (No.) | Salinity (No.) | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 6.6 (1) | 8.4 (2) | 9.8 (3) | 2 (1) | 13 (2) | 25 (3) | 36 (4) | 20 (1) | 28 (2) | 36 (3) | |||
| AVG | 5.9 | 4.4 | 4.0 | 4.2 | 1.7 | 0.7 | 14.3 | 12.5 | 2.2 | 9.0 | ||
| SD | 0.6 | 1.8 | 0.5 | 3.2 | 0.4 | 0.4 | 0.4 | 0.4 | 1.3 | 0.1 | ||
由表中数据可以看出,温度为36 ℃和盐度为20、36的环境中试样的频率值最高,形成的膜层致密性最佳。
动电位极化曲线能够表征试样表面的腐蚀反应过程,对在不同海水中浸泡20 d的B30铜镍合金试样进行动电位极化曲线的测试。对动电位极化曲线进行数据拟合,通过腐蚀电流密度对试样的腐蚀以及形成的膜层进行侧面评测,腐蚀电流越低,腐蚀越轻,耐蚀性越好。
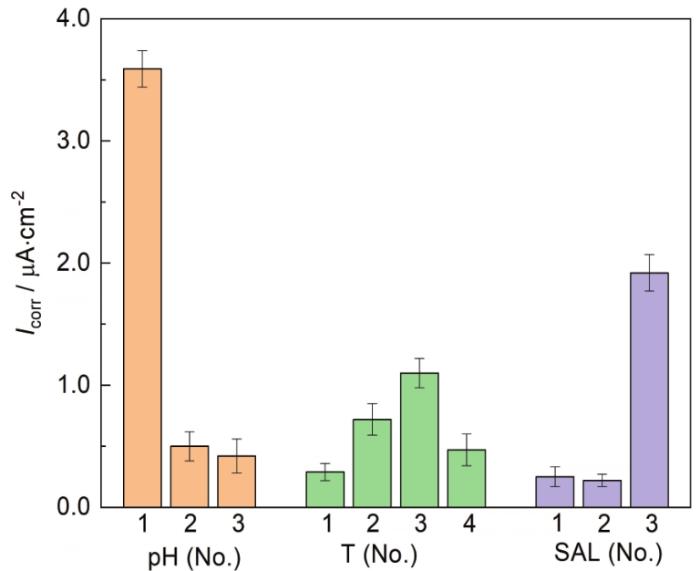
图15以及表8为B30铜镍合金在不同海水中腐蚀电流密度拟合数据,由拟合所有数据可以看出,pH为6.6以及盐度为36时,海水环境中侵蚀性离子较多,试样的腐蚀明显比其他海水环境严重。pH以及盐度对B30铜镍合金的腐蚀以及成膜的影响较大。B30铜镍合金在pH为6.6的海水中的腐蚀最为严重,pH为8.4~9.8腐蚀电流密度变化不大。温度对于B30铜镍合金的影响,腐蚀电流密度呈现先增大后减小的趋势,在2 ℃的海水中腐蚀电流密度最小,约为25 ℃时温度的五分之一,13~36 ℃时温度变化不大。在盐度为20~28的海水中,腐蚀电流密度较低且变化不大,盐度到达36,试样的腐蚀有明显提升。在温度为2 ℃以及盐度为20和28的海水中,表面成膜的试样腐蚀电流密度最低,腐蚀最轻。
图15
图15
B30铜镍合金在不同海水中的腐蚀电流密度图
Fig.15
Diagram of corrosion current densities of B30 copper-nickel alloy in seawater under different conditions
表8 B30铜镍合金在不同条件的海水中的腐蚀电流密度
Table 8
| Icorr / μA·cm-2 | pH (No.) | Temperature / ℃ (No.) | Salinity (No.) | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 6.6 (1) | 8.4 (2) | 9.8 (3) | 2 (1) | 13 (2) | 25 (3) | 36 (3) | 20 (1) | 28 (2) | 36 (3) | |||
| AVG | 3.59 | 0.50 | 0.42 | 0.29 | 0.72 | 1.10 | 0.47 | 0.25 | 0.22 | 1.92 | ||
| SD | 0.15 | 0.12 | 0.14 | 0.07 | 0.13 | 0.12 | 0.13 | 0.08 | 0.05 | 0.15 | ||
3 结论
由电化学阻抗数据和X射线光电子能谱数据分析可得,B30铜镍合金在pH为6.6~9.8的海水中膜层质量先变好再变差;在温度为2~36 ℃的海水中,膜层质量呈现先变差再变好的趋势;在盐度为20~36的海水中,膜层质量呈现先变差再变好的趋势。
综合电化学阻抗谱测试和动电位极化曲线测试可知,在盐度为20的海水中,B30铜镍合金表面形成的膜层质量最佳,保护效果最好。
参考文献
Effect of protein adsorption on the corrosion behavior of 70Cu-30Ni alloy in artificial seawater
[J].Copper alloys often used in cooling circuits of industrial plants can be affected by biocorrosion induced by biofilm formation. The objective of this work was to study the influence of protein adsorption, which is the first step in biofilm formation, on the electrochemical behavior of 70Cu-30Ni (wt.%) alloy in static artificial seawater and on the chemical composition of oxide layers. For that purpose, electrochemical measurements performed after 1h of immersion were combined to surface analyses. A model is proposed to analyze impedance data. In the presence of bovine serum albumin (BSA, model protein), the anodic charge transfer resistance deduced from EIS data at Ecorr is slightly higher, corresponding to lower corrosion current. Without BSA, two oxidized layers are shown by XPS and ToF-SIMS: an outer layer mainly composed of copper oxide (Cu2O redeposited layer) and an inner layer mainly composed of oxidized nickel, with a global thickness of ~30nm. The presence of BSA leads to a mixed oxide layer (CuO, Cu2O, Ni(OH)2) with a lower thickness (~10nm). Thus, the protein induces a decrease of the dissolution rate at Ecorr and hence a decrease of the amount of redeposited Cu2O and of the oxide layer thickness. © 2013.
Corrosion product film formed on the 90/10 copper-nickel tube in natural seawater: composition/structure and formation mechanism
[J].
The effect of temperature on the corrosion behaviour of a 70/30 Cu-Ni commercial alloy in seawater
[J].
Studies on corrosion and protection of heat exchange tubes of B30 copper-nickel alloy
[J].
B30铜镍合金换热管腐蚀与防护研究进展
[J].
Corrosion of nickel-containing stainless steel in concentrated sulphuric acid
[J].
Copper-Nickel alloy for the construction of ship and boat hulls
[J].
Corrosion behavior of copper alloys in chloride media
[J].
The corrosion behavior of copper alloys, stainless steels and titanium in seawater
[J].
Seawater-corrosion-induced intergranular precipitation in Cu-Ni alloy
[J].
海水腐蚀导致铜镍合金的沿晶析出
[J].半硬态B_(Fe30-1-1)铜镍合金管材在实海暴露过程中随着表面氧化膜的腐蚀脱落,在晶界上出现沿晶析出物,形成较大的沿晶腐蚀倾向。TEM观察表明,这种析出物是调幅分解(Spinodaldecomposition)的产物,其衍衬象为明暗相间的条纹,调幅波长小于50nm。该析出物使材料在拉伸时出现脆性沿晶断口,强度略有上升,但大大恶化了材料的耐海水腐蚀性能。文中根据试验结果阐明了析出物的生成动力,认为是海水腐蚀导致材料的应力状态改变(即应变诱生)及合金元素沿晶界向表层的扩散促使已形核的析出物粗化所致。
Failure investigation of brass heat exchanger tube
[J].
Effect of residual stress on corrosion resistance of copper tube BFe30-1-1 in 3.5%NaCl
[J].
残余应力对BFe30-1-1铜管耐蚀性能的影响
[J].采用电化学测试,X射线衍射和俄歇深度分析研究了残余应力对BFe3O-1-1铜镍合金管在3.5%NaCl溶液内浸泡过程中形成的表面膜及其稳定性的影响.结果表明,一种管材压缩、拉伸残余应力沿层深交替出现,起伏变化较大;另一种管材残余应力较小,且分布平稳.前者形成的表面膜易脱落,无镍的富集;后者的表面膜中富镍,且与基体粘附力较强.
Influence of temperature on corrosion product film formation on CuNi10Fe in the low temperature range: Part 2: studies on corrosion product film formation and properties in relation to microstructure and iron content
[J].
Role of the corrosion product film in the corrosion protection Cu-Ni alloys in saltwater
[D].
The effect of surface film on electrochemical behavior of Cu-Ni-Alloy
[J].
铜镍合金表面膜对其电化学行为的影响
[J].
Corrosion behavior of H62 brass alloy/TC4 titanium alloy welded specimens
[J].
H62黄铜/TC4钛合金焊接件腐蚀行为研究
[J].采用真空扩散焊接进行H62黄铜与TC4钛合金的焊接,并使用3.5% (质量分数) NaCl溶液对焊接件进行全浸实验。利用SEM及EDS对焊缝两侧的微观形貌及元素分布进行分析,并分析距离焊缝不同距离的区域内,H62黄铜的微观腐蚀形貌的差异;利用扫描Kelvin探针测试焊缝区及其两侧基底合金的表面电位随浸泡时间的变化,分析焊接件的电偶腐蚀规律;利用XPS分析焊接后的H62黄铜与TC4钛合金区域的化学成分,并分析其腐蚀机理。结果表明,由真空扩散焊连接的H62黄铜及TC4钛合金焊缝间距约为25~30 μm;浸泡实验初期H62黄铜电位略高于TC4钛合金的,但是随着浸泡实验时间延长,H62黄铜的表面电位开始逐渐下降,后期 (4 h) 表面电位开始低于钛合金的;同时,距离TC4钛合金较近区域的H62黄铜腐蚀较焊缝远处的更严重;H62黄铜浸泡实验后的腐蚀产物主要包括CuO,Cu<sub>2</sub>O,CuCl,CuCl<sub>2</sub>和Cu(OH)<sub>2</sub>,而TC4钛合金表面主要为含有TiO<sub>2</sub>和Ti<sub>2</sub>O<sub>3 </sub>的氧化膜。说明浸泡在3.5%NaCl溶液中的H62黄铜/TC4钛合金焊接试样存在电偶腐蚀倾向,H62黄铜作为阳极被加速腐蚀,TC4钛合金作为阴极被保护,阴极和阳极区域间的电偶对距离作用越长,腐蚀程度越轻。
Potential-pH diagrams for 90-10 and 70-30 Cu-Ni in sea water
[J].
Corrosion of copper-nickel alloys in sea water polluted with sulfide and sulfide oxidation products
[J].The corrosion rates of copper alloys 706 (90:10 Cu:Ni) and 715 (70:30 Cu:Ni) were measured, using rotating cylinder specimens in sea water that contained oxygen, sulfide, sulfur, and polysulfide, either singly or in combination. In addition a control test was performed using unpolluted deaerated sea water. Corrosion rates were monitored for over 24 hours, using linear polarization and potential step techniques. The work has shown that copper-nickel alloys can corrode quite rapidly in deaerated sea water if these normally “passive” alloys are made active by the presence of sulfide, or if sulfur is available as an oxidant.
Influence of pH on electrochemical behavior of 70/30 Cu-Ni alloy
[J].
pH值变化对B30铜镍合金腐蚀电化学行为的影响
[J].
Effect of temperature on electrochemical behavior of B30 Cu-Ni alloy in seawater
[J].
温度对B30铜镍合金在海水中电化学行为的影响
[J].
Review of corrosion product films of Cu-Ni alloys in seawater
[J].
Cu-Ni合金海水蚀产物膜研究进展
[J].
Evolution of the corrosion product film and its effect on the erosion-corrosion behavior of two commercial 90Cu-10Ni tubes in seawater
[J].
Electrochemical behavior of B30 Cu-Ni alloy in seawater
[J].
B30铜镍合金在海水中的电化学行为
[J].
Analysis of factors affecting the corrosion of copper alloys
[J].
影响铜合金腐蚀的因素分析
[J].
Electrochemical studies of inhibition effects for B30 Cu-Ni alloy corrosion in simulated water
[J].
模拟水中B30铜镍合金耐蚀性的电化学研究
[J].
Review on corrosion behaviors of Cu Ni alloys in seawater
[J].
Cu-Ni合金海水腐蚀行为研究进展
[J].
Electrochemical behavior of copper-nickel alloys in acidic chloride solutions
[J].
EIS characteristics of Cu-based alloy in seawater
[J].
铜合金在海水中电化学阻抗谱特征研究
[J].
Electrochemical behavior of Cu-Ni alloy in sodium chloride solution
[J].
铜镍合金B-30在氯化钠介质中的电化学行为
[J].
Galvanic corrosion performance of high-strength copper-nickel alloys in seawater
[J].
Stress corrosion cracking of a copper elbow fitting
[J].
The roles of mercapto, benzene and methyl groups in the corrosion inhibition of imidazoles on copper: I. Experimental characterization
[J].
Anodic polarization behavior of copper in aqueous bromide and bromide/benzotriazole solutions
[J].
Congress on marine corrosion and fouling
[C].
Corrosion of B10 Cu-Ni alloy in seawater polluted by high concentration of NH4 +
[J].
B10铜镍合金在高浓度NH4 +污染海水中腐蚀研究
[J].通过比较B10铜镍合金在天然海水和含10 mg/L NH<sub>4</sub><sup>+</sup>海水中的腐蚀行为,研究NH<sub>4</sub><sup>+</sup>对B10铜镍合金的腐蚀影响机制。采用失重法测量平均腐蚀速率;采用动电位极化分析、电化学阻抗谱 (EIS) 研究界面腐蚀电化学特征;采用扫描电子显微镜 (SEM) 表征腐蚀产物形貌;采用能量色散光谱 (EDS) 和X射线光电子能谱 (XPS) 分析腐蚀产物成分。结果表明,NH<sub>4</sub><sup>+</sup>的添加降低了腐蚀产物中具有保护作用的Cu<sub>2</sub>O成分的含量,提高了B10铜镍合金在海水中的腐蚀速率,促进了点蚀的发生。
Research progress on the formation and rupture mechanism of seawater corrosion product film of Cu-Ni alloy
[J].
Cu-Ni合金海水腐蚀产物膜的形成与破裂机制研究进展
[J].
Surface characterization and corrosion behavior of 70/30 Cu-Ni alloy in pristine and sulfide-containing simulated seawater
[J].
The effect of Fe on the corrosion rate of copper rich Cu-Ni alloys
[J].
Combined effect of chloride and pH on corrosion resistance of Cu-10Ni alloy
[J].