镀锌钢板广泛应用于民用和国防建设的各个领域,能够对钢基体起到有效的保护作用[1,2],镀锌钢在大气[3-10]和含Cl-的盐溶液[11-14]等不同环境下服役时,腐蚀影响因素不同,腐蚀环境会改变表面腐蚀产物的组成和形态,进而影响其耐腐蚀性能。刘栓等[15]报道了镀锌钢在大气环境、海水环境和钢筋混凝土中的腐蚀行为的研究进展。大气中的Cl-、CO2及腐蚀性的SO2、NO2等是影响镀锌层防护性能的重要因素,同时会引发氢析出、氢渗透和腐蚀开裂等严重的问题。海水环境中Cl-对镀锌层的腐蚀破坏最为严重,同时镀锌层在海洋大气区、潮差区、浪花飞溅区、全浸区、海泥区等不同的腐蚀带,腐蚀规律和耐蚀性能有较大差异。钢筋混凝土是建筑工程的主要结构材料,镀锌处理已成为钢筋防锈的重要技术手段,在服役的过程中pH和Cl-是影响其寿命的重要因素。
当前镀锌钢腐蚀行为的研究主要集中在大气环境、海水环境或者其他含有Cl-的环境,对于镀锌钢在淡水环境中的腐蚀鲜有报道。海水淡化是保障舰船淡水供应的重要技术手段,不同海域的海水具有不同的pH、盐度、离子浓度等,海水淡化处理后所获得的水质环境也不尽相同,对于镀锌钢在海水淡化处理后的淡水环境中的腐蚀行为仍然是未知的。本文选取3种利用海水淡化装置处理后不同种类的二级反渗透水作为腐蚀介质,研究镀锌钢在不同反渗透水中的腐蚀行为,同时为了调整水质达到适合饮用的目的,在反渗透水的基础上添加不同含量的Mg2+、Ca2+和HCO3-,研究其在调质水中的腐蚀特征。
1 实验方法
本工作选取国产热浸镀锌钢板,共选用了6种淡水水样,其中1#~3#水样为不同盐度的海水经淡化处理后所得的反渗透二级水,在海水淡化处理前的盐度分别为25000、35000和45000 mg/L。4#~6#是在2#反渗透水的基础上通过加入MgCl2、CaCl2和NaHCO3所得的调质水,具体的含义为4#水为2#水+(20 mg/L MgCl2、15 mg/L CaCl2、90 mg/L NaHCO3),5#水为2#水+(50 mg/L MgCl2、35 mg/L CaCl2、90 mg/L NaHCO3),6#水为2#水+(50 mg/L MgCl2、35 mg/L CaCl2、70 mg/L NaHCO3)。所选不同淡水的性质如表1所示。
表1 不同淡水的性质
Table 1
| No. | pH | TDS / mg·L-1 | Turbidity / NTU | Cl- / mg·L-1 | Bicarbonate / mg·L-1 | Hardness (CaCO3) / mg·L-1 | Ca2+ / mg·L-1 | Mg2+ / mg·L-1 |
|---|---|---|---|---|---|---|---|---|
| 1# | 8.27 | 3.86 | 0.15 | <0.02 | --- | --- | --- | --- |
| 2# | 7.72 | 5.65 | 0.15 | <0.02 | --- | --- | --- | --- |
| 3# | 7.13 | 120.4 | 0.20 | <0.02 | --- | --- | --- | --- |
| 4# | 6.86 | 71.1 | 0.27 | <0.02 | 88.45 | 27.75 | 7.70 | 2.04 |
| 5# | 6.62 | 103.2 | 0.25 | <0.02 | 87.84 | 85.70 | 21.80 | 7.49 |
| 6# | 6.54 | 89.0 | 0.26 | <0.02 | 73.20 | 55.97 | 13.47 | 5.35 |
利用VersaSTAT V3F电化学工作站对浸泡不同时间的镀锌钢板进行了开路电位 (OCP) 和电化学阻抗谱 (EIS) 测试,整个测试周期为720 h,其中待测样品为工作电极,铂片为对电极,饱和甘汞电极为参比电极。电化学阻抗谱测试前先进行10 min的开路电位扫描,待电位稳定后进行测试,频率测试范围105~10-2 Hz,正弦波扰动振幅为10 mV。采用Zsim Demo对EIS数据进行了拟合。利用MIRA 3扫描电镜 (SEM) 及自带的能量色散X射线光谱 (EDS) 对在不同水环境中浸泡720 h后镀锌钢板的显微形貌进行了观察。
2 结果与讨论
2.1 镀锌钢在不同反渗透水中的电化学特征
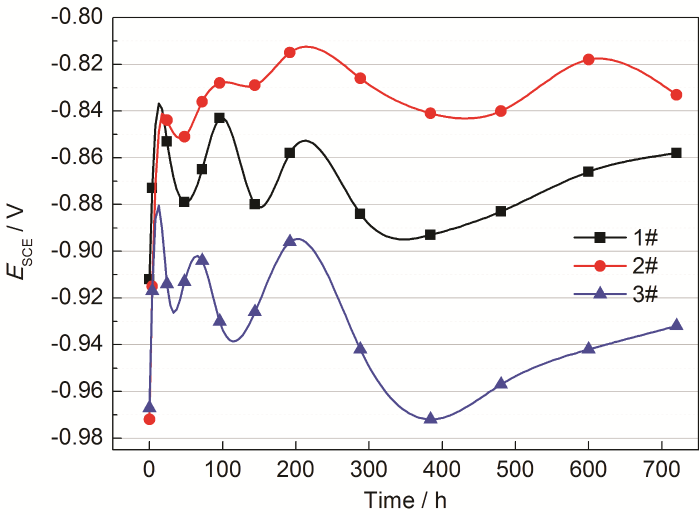
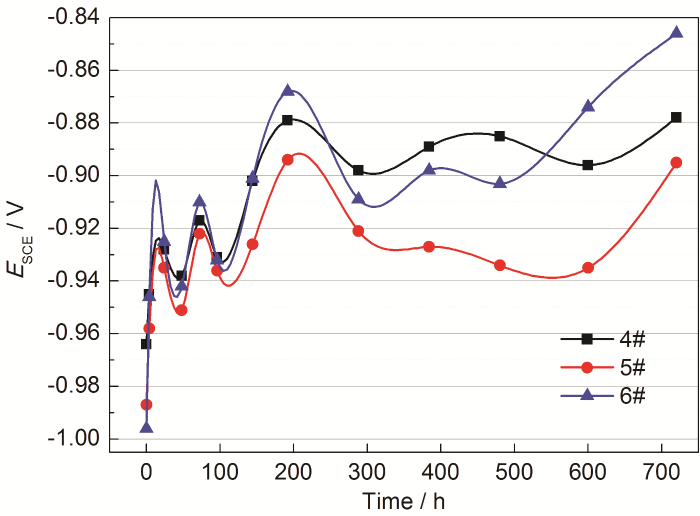
镀锌钢在1#~3#反渗透水中浸泡720 h的开路电位如图1所示。可以看出,镀锌钢在3种反渗透水中的开路电位变化主要分为快速上升阶段、波动式变化阶段和后期反弹上升阶段。从整体上看,镀锌钢在3种反渗透中开路电位的高低为:2#>1#>3#,即镀锌钢在进水盐度为35000 mg/L的海水淡化处理后所得的反渗透二级水中的开路电位最高。
图1
图1
镀锌钢在不同反渗透水中开路电位随时间的变化
Fig.1
OCP vs time of the galvanized steel in different reverse osmosis water
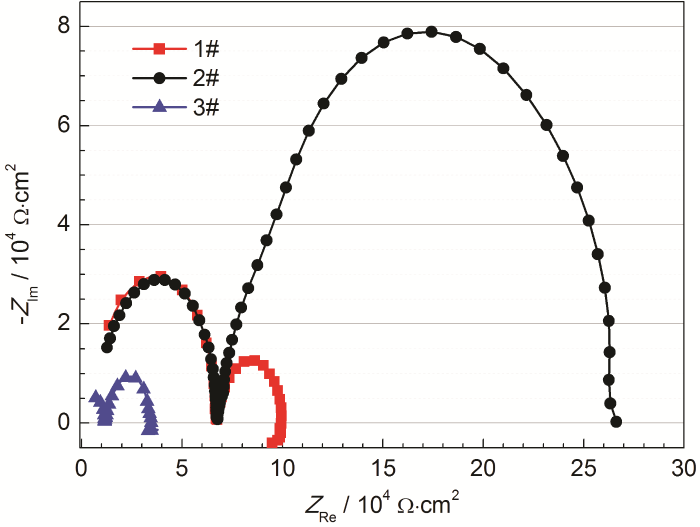
为了更进一步揭示镀锌钢在整个720 h浸泡时间内的失效机制,对镀锌钢在3种水环境中浸泡不同时间的电化学阻抗谱进行了测试,浸泡开始时的Nyquist图如图2所示。由图可见,镀锌钢在3种反渗透中的阻抗谱均由两个容抗弧组成,第一个容抗弧与X轴的交点即为该溶液体系下的溶液电阻,由于3种反渗透水中的离子浓度不尽相同,所测的溶液电阻不同,且溶液电阻随浸泡时间的变化而变化。第二个容抗弧代表了镀锌钢腐蚀过程中的信息,可以看出镀锌钢在2#水样中的容抗弧半径较大,其次是1#水样和3#水样,这与图1中开路电位的测试结果相符,预示着镀锌钢在2#水样中可能具有最低的腐蚀速率。考虑到第一个容抗弧没有实际的物理意义,只是反映了溶液电阻的信息,为了便于比较,对镀锌钢在所有反渗透中的电化学阻抗谱进行了归一化处理,将所得的实部阻抗均减去测试时的溶液电阻。
图2
图2
镀锌钢在不同反渗透水中浸泡0 h时的电化学阻抗谱
Fig.2
Nyquist plot of galvanized steel in different reverse osmosis water at the beginning immersion
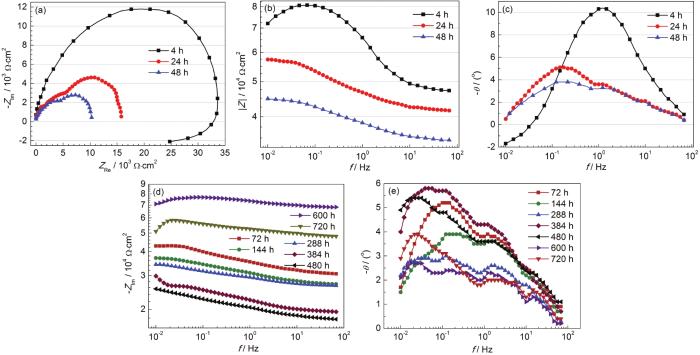
从图1镀锌钢板在3种反渗透水中开路电位的变化,可以将其腐蚀历程分成3个阶段:第一阶段,开路电位快速上升期,时间节点约为0~48 h;第二阶段开路电位波动期,时间节点约为48~480 h;第三阶段开路电位反弹上升期,时间节点约为480~720 h。镀锌钢在1#反渗透水中浸泡4~48 h的电化学阻抗谱如图3a~c所示,从Nyquist图中 (图3a) 可以看出,浸泡初期4 h时,镀锌板阻抗表现出单一容抗弧和低频感抗的特征,随着浸泡时间的增加,24和48 h时都表现出双容抗弧的特征,且容抗弧的半径随浸泡时间的增加快速降低。从Bode图的阻抗模值变化来看 (图3b),镀锌板的低频阻抗模值由4 h时的7.19×104 Ω·cm2逐渐下降至48 h时4.48×104 Ω·cm2,从Bode图的相位角变化判断,镀锌钢在1#反渗透水中的相位角整体偏低,多在10o以下,且随浸泡时间的增加,相位角进一步降低,由一个宽化的时间常数特征峰向两个峰转变。镀锌钢浸泡72~720 h的电化学阻抗谱如图3d和e所示,从阻抗模值的变化来看 (图3d),镀锌钢在浸泡72~480 h的过程中,阻抗模值持续降低,在600~720 h范围内,出现了明显的上升,从相位角的变化判断,镀锌钢在72~720 h整个浸泡过程中,相位角均表现出两个时间常数特征峰。
图3
图3
镀锌钢在1#反渗透水中浸泡不同时间的电化学阻抗谱
Fig.3
Nyquist (a), modules (b, d) and phase angle (c, e) plots of the galvanized steel in 1# reverse osmosis water during the immersion 4~48 h (a~c) and 72~720 h (d, e)
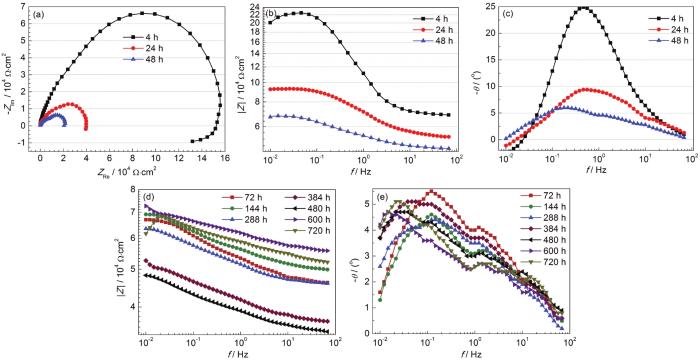
镀锌钢在2#反渗透水中浸泡4~48 h和72~720 h的电化学阻抗谱如图4所示。可以看出,随着浸泡时间由4 h增加至48 h,镀锌钢阻抗由单一容抗弧+低频感抗向双容抗弧转变,容抗弧的半径明显减小 (图4a),低频阻抗模值由4 h时的2.0×105 Ω·cm2逐渐下降至48 h时6.7×104 Ω·cm2 (图4b),时间常数特征峰由一个宽化的峰向两个峰转变。镀锌钢在浸泡72~480 h的过程中,阻抗模值持续降低,在600~720 h范围内,出现了明显的上升 (图4d),相位角在72~720 h的浸泡时间内均表现出两个时间常数特征峰 (图4e),这与在1#反渗透水中的变化趋势完全一样。镀锌钢在3#反渗透水中浸泡4~48 h和72~720 h的电化学阻抗谱如图5所示,阻抗变化特征和趋势与其在1#、2#反渗透水中基本一致,这里不再赘述。
图4
图4
镀锌钢在2#反渗透水中浸泡不同时间的电化学阻抗谱
Fig.4
Nyquist (a), modules (b, d) and phase angle (c, e) plots of the galvanized steel in 2# reverse osmosis water during the immersion 4~48 h (a~c) and 72~720 h (d, e)
图5
图5
镀锌钢在3#反渗透水中浸泡不同时间的电化学阻抗谱
Fig.5
Nyquist (a), modules (b, d) and phase angle (c, e) plots of the galvanized steel in 3# reverse osmosis water during the immersion 4~48 h (a~c) and 72~720 h (d, e)
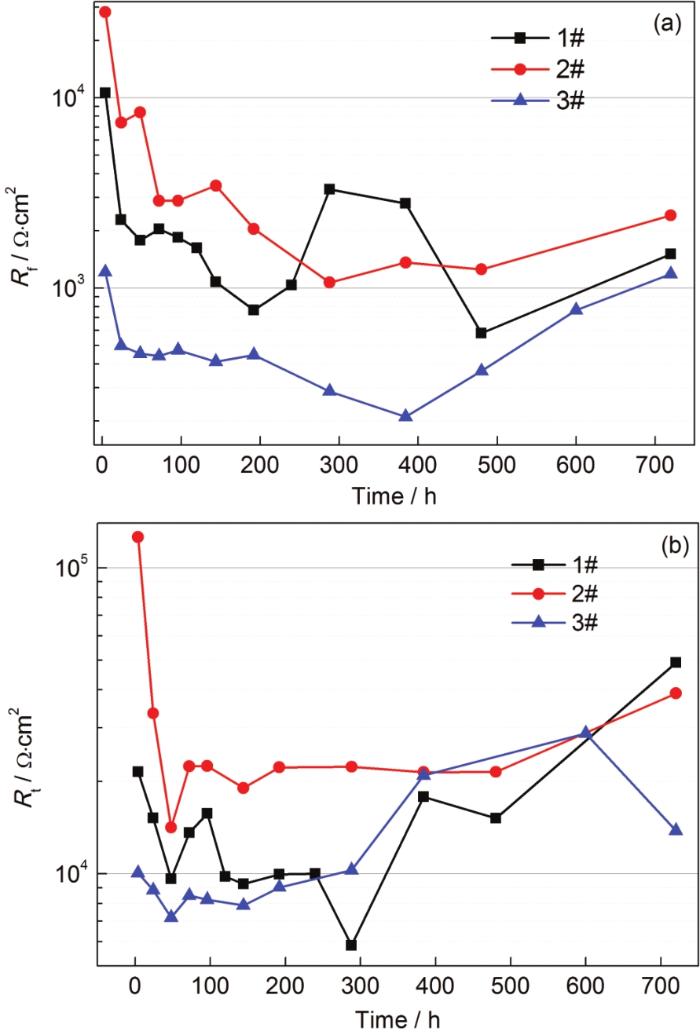
镀锌钢在1#~3#反渗透水中电化学阻抗谱低频模值随时间的变化如图6a所示,低频模值的高低在一定程度上可以反映出体系腐蚀速率的变化,可以看出镀锌钢在2#反渗透水中表现出最低的腐蚀速率,其次是1#水样和3#水样。进一步分析每一种反渗透水中低频模值的变化可以发现,镀锌钢低频模值随时间的变化同样可分为3个阶段:0~48 h,低频模值的快速下降;48~384 h,低频模值缓慢下降;384~720 h,低频模值表现出一定程度的上升。根据图3~5镀锌钢在3种反渗透水中电化学阻抗谱的特征,选用如图6b所示的等效电路对数据进行拟合,其中Rs为溶液电阻,CPEdl为双电层电容,Rt为电荷转移电阻,CPEf为表面膜电容,Rf为表面膜电阻,镀锌钢在不同反渗透水中电化学阻抗谱的拟合结果见表2~4。
图6
图6
镀锌钢在不同反渗透水中电化学阻抗谱低频模值随时间的变化及其等效电路
Fig.6
Low-frequency modules vs time (a) and equivalent circuit (b) of the galvanized steel in different reverse osmosis water
表2 镀锌钢在1#反渗透水中电化学阻抗谱拟合结果
Table 2
| Time / h | CPEf / Ω-1·cm-2·sn | Rf / Ω.cm2 | CPEdl / Ω-1·cm-2·sn | Rt / Ω·cm2 |
|---|---|---|---|---|
| 4 | 2.5×10-6 | 10576.7 | 7.8×10-6 | 21525.2 |
| 24 | 5.2×10-6 | 2280.6 | 6.1×10-5 | 15234.2 |
| 48 | 7.0×10-6 | 1785.3 | 8.2×10-5 | 9629.1 |
| 72 | 4.7×10-6 | 2040.3 | 8.4×10-5 | 13602.0 |
| 96 | 5.2×10-6 | 1847.6 | 9.8×10-5 | 15721.6 |
| 120 | 6.4×10-6 | 1622.0 | 9.8×10-5 | 9795.7 |
| 144 | 5.1×10-6 | 1075.7 | 1.1×10-4 | 9261.8 |
| 192 | 4.9×10-6 | 764.9 | 1.1×10-4 | 9972.5 |
| 240 | 1.0×10-5 | 1038.2 | 1.8×10-4 | 10006.5 |
| 288 | 2.9×10-5 | 3303.0 | 3.7×10-4 | 5831.9 |
| 384 | 3.1×10-5 | 2783.9 | 2.4×10-4 | 17830.0 |
| 480 | 6.6×10-6 | 578.7 | 1.8×10-4 | 15188.9 |
| 600 | --- | --- | --- | --- |
| 720 | 4.3×10-6 | 1509.8 | 1.6×10-4 | 48933.2 |
表3 镀锌钢在2#反渗透水中电化学阻抗谱拟合结果
Table 3
Time h | CPEf Ω-1·cm-2·sn | Rf Ω·cm2 | CPEdl Ω-1·cm-2·sn | Rt Ω·cm2 |
|---|---|---|---|---|
| 4 | 1.6×10-6 | 28201.5 | 2.8×10-6 | 125931.9 |
| 24 | 1.7×10-6 | 7418.8 | 1.1×10-5 | 33472.3 |
| 48 | 1.0×10-5 | 8385.6 | 5.7×10-5 | 14180.1 |
| 72 | 3.8×10-6 | 2878.0 | 5.3×10-5 | 22454.6 |
| 96 | 3.7×10-6 | 2879.1 | 5.8×10-5 | 22500.0 |
| 120 | 4.1×10-6 | 3456.0 | 7.2×10-5 | 19076.8 |
| 144 | 4.0×10-6 | 2049.4 | 7.7×10-5 | 22284.6 |
| 192 | 5.1×10-6 | 1069.0 | 6.2×10-5 | 22364.0 |
| 240 | 4.8×10-6 | 1362.5 | 8.5×10-5 | 21502.5 |
| 288 | 3.9×10-6 | 1252.5 | 1.0×10-4 | 21513.8 |
| 384 | --- | --- | --- | --- |
| 480 | 2.5×10-6 | 2411.0 | 9.5×10-5 | 38901.7 |
| 600 | 1.6×10-6 | 28201.5 | 2.8×10-6 | 125931.9 |
| 720 | 1.7×10-6 | 7418.8 | 1.1×10-5 | 33472.3 |
表4 镀锌钢在3#反渗透水中电化学阻抗谱拟合结果
Table 4
Time h | CPEf Ω-1·cm-2·sn | Rf Ω·cm2 | CPEdl Ω-1·cm-2·sn | Rt Ω·cm2 |
|---|---|---|---|---|
| 4 | 1.0×10-6 | 1212.8 | 1.1×10-5 | 10070.0 |
| 24 | 1.5×10-6 | 498.3 | 5.0×10-5 | 8845.8 |
| 48 | 1.7×10-6 | 451.6 | 7.8×10-5 | 7196.6 |
| 72 | 1.6×10-6 | 439.5 | 9.2×10-5 | 8496.7 |
| 96 | 1.6×10-6 | 472.7 | 1.1×10-4 | 8229.2 |
| 120 | 1.9×10-6 | 411.0 | 1.8×10-4 | 7875.6 |
| 144 | 1.3×10-6 | 445.6 | 2.0×10-4 | 9024.9 |
| 192 | 2.3×10-6 | 286.7 | 2.5×10-4 | 10280.8 |
| 240 | 2.4×10-6 | 211.1 | 3.8×10-4 | 20958.4 |
| 288 | 1.8×10-6 | 366.5 | 4.9×10-4 | 105075.5 |
| 384 | 2.8×10-6 | 765.3 | 4.9×10-4 | 28722.9 |
| 480 | 5.0×10-6 | 1185.6 | 6.3×10-4 | 13817.4 |
| 600 | 1.0×10-6 | 1212.8 | 1.1×10-5 | 10070.0 |
| 720 | 1.5×10-6 | 498.3 | 5.0×10-5 | 8845.8 |
图7
图7
镀锌钢在不同反渗透水中腐蚀产物膜电阻和电荷转移电阻随时间的变化
Fig.7
Rf (a) and Rt (b) vs time of the galvanized steel in different reverse osmosis water
2.2 镀锌钢在不同反渗透水中的显微形貌特征
从以上镀锌钢在不同反渗透水中的电化学特征可以总结出,其在反渗透水中的腐蚀失效可以分成3个阶段,第一个阶段由于表面锌的快速溶解,体系的阻抗模值迅速降低;第二阶段,随着腐蚀产物的生成,阻抗模值的下降速度明显减小;第三阶段,镀锌钢表面腐蚀产物膜不断增厚,对基体起到了一定的保护作用,体系的阻抗模值略有上升。镀锌钢在3种反渗透水中浸泡720 h后的微观形貌如图8所示,可以看出,镀锌钢在不同的反渗透水中浸泡后呈现出不同的形貌特征,1#反渗透水中的形貌特征主要以球状产物为主,2#反渗透水中的形貌特征主要以块状腐蚀产物为主,3#反渗透水中的形貌特征主要以尺寸较小的球状产物形成的大的团簇为主。镀锌钢在以上3种反渗透水中腐蚀产物膜的化学成分如表5所示,可见3种溶液中腐蚀产物膜的主要成分是C、O、Na、Zn,其中以2#反渗透水中生成腐蚀产物膜的O含量最高,3#反渗透水中生成腐蚀产物膜的Zn含量最高,可以推测其产物主要是锌的氧化物、氢氧化物和碱式碳酸锌等,主要的化学反应机理如下:
图8
图8
镀锌钢在不同反渗透水中浸泡720 h后的微观形貌
Fig.8
Morphologies of the domestic galvanized steel after 720 h immersion: (a) 1#, (b) 2#, (c) 3#
表5 镀锌钢在3种反渗透水中腐蚀产物膜的化学成分
Table 5
| Reverse osmosis water | C | O | Zn | Na |
|---|---|---|---|---|
| 1# | 11.9 | 37.4 | 41.9 | 8.8 |
| 2# | 8.1 | 43.8 | 38.9 | 9.2 |
| 3# | 11.7 | 31.9 | 51.4 | 5.0 |
阳极反应:
阴极反应:
Zn的氢氧化物和氧化物的生成反应:
碱式碳酸锌的生成反应:
2.3 镀锌钢在不同调质水中的电化学特征
在2#反渗透水中通过加入不同浓度的MgCl2、CaCl2和NaHCO3,得到了4#~6#不同的调质水,4#调质水和5#调质水比较可以得出MgCl2和CaCl2浓度对镀锌钢腐蚀的影响,5#调质水和6#调质水对比可以得出碳酸氢钠含量对镀锌钢腐蚀的影响。镀锌钢在此3种调质水中开路电位随时间的变化如图9所示。从中可以看出,随着浸泡时间的增加,镀锌钢在3种水溶液中的开路电位呈现相似的变化特征,主要可以分成两个阶段:第一阶段0~192 h,开路电位呈波浪式上升后在192 h处达到一个顶点;第二阶段192~720 h,开路电位先下降后上升。
图9
图9
镀锌钢在不同调质水中开路电位随时间的变化
Fig.9
OCP vs time of the galvanized steel in different conditioned water
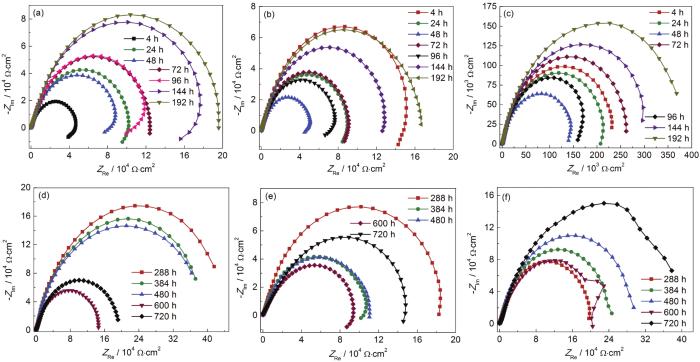
镀锌钢在4#~6#调质水中浸泡720 h的电化学阻抗谱如图10所示,可以看出镀锌钢在3种调质水中的阻抗谱具有相似的特征,均表现出高频容抗和低频感抗的特征,根据开路电位和阻抗谱的变化特征,将镀锌钢在3种调质水中的腐蚀历程分成两个阶段:第一阶段0~192 h和第二阶段192~720 h。图10显示,镀锌钢在4#调质水中浸泡的第一阶段0~192 h,容抗弧的半径呈现不断增加的趋势 (图10a);在第二阶段192~720 h,容抗弧的半径先降低而后增加,在600 h时降至最低 (图10b)。图10c和d显示,镀锌钢在5#调质水中浸泡的第一阶段0~192 h,容抗弧的半径由0~48 h逐渐减小,在48 h时降至最低,随着浸泡时间的进一步增加,72~96 h出现短暂的波动后,容抗弧的半径不断增大,在192 h时增至最大 (图10c);第二阶段192~720 h,容抗弧的半径变化趋势与4#调质水中相似,表现出先减小后增大的特征,在600 h降至最低 (图10d)。图10e和f显示,镀锌钢在6#调质水中浸泡第一阶段0~192 h阻抗谱的变化特征与其在5#调质水中的行为完全一致,容抗弧的半径由0~48 h逐渐减小,在48 h时降至最低,随着浸泡时间的进一步增加,72~96 h出现短暂的波动后,容抗弧的半径不断增大,在192 h时增至最大 (图10e);浸泡第二阶段192~720 h阻抗谱的变化特征与其在4#、5#调质水中的特征一致,容抗弧表现出先减小后增大的特征,在600 h降至最低 (图10f)。
图10
图10
镀锌钢在4#~6#调质水中浸泡720 h的电化学阻抗谱
Fig.10
Nyquist plots of the galvanized steel in 4# (a, d), 5# (b, e) and 6# (c, f) conditioned water during 720 h immersion of I stage (a~c) and II stage (d~f)
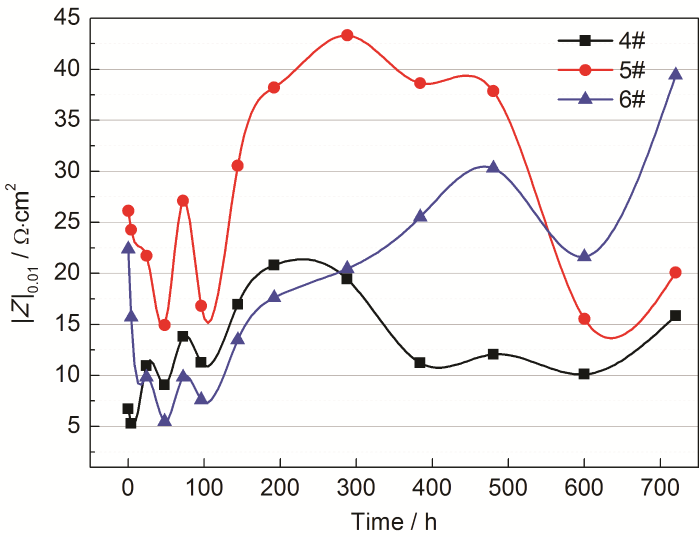
镀锌钢在4#~6#溶液中电化学阻抗谱低频模值随时间的变化如图11所示。镀锌钢低频阻抗模值在3种调质水中表现出不同的变化规律,在4#和5#溶液中表现出先波浪式上升而后下降的趋势,而在6#溶液中则表现为先降低后上升的特征,尤其是镀锌钢低频阻抗模值在6#调质水中后期的升高,已明显超过其在4#和5#调质水中的表现,但从整体上看,镀锌钢在5#调质水中表现出最高的阻抗模值,预示着最低的腐蚀速率,其次是6#和4#调质水。也就是说,增加反渗透水中氯化镁和氯化钙的浓度,镀锌钢的腐蚀速率降低,进一步降低水溶液中碳酸氢钠的浓度,镀锌钢的腐蚀速率有所增加。
图11
图11
镀锌钢在4#~6#调质水中电化学阻抗谱低频模值随时间的变化
Fig.11
Low-frequency modules of the galvanized steel in different conditioned water
2.4 镀锌钢在不同调质水中的显微形貌特征
总结镀锌钢在4#~6#调质水中的电化学阻抗谱规律可以得出以下共性特征:第一,在腐蚀历程的第一阶段0~192 h,镀锌钢在4#溶液中的阻抗谱呈现不断增大的趋势,而在5#和6#调质水中则表现出先降低后增加的趋势,均在48 h时表现出最差的耐蚀性能,其中的原因可能是相比于4#调质水,5#调质水中有更高的Cl-浓度,6#溶液不仅具有高的Cl-浓度,pH稍低于4#调质水,腐蚀的初期,高的Cl-浓度和低的pH更容易造成镀锌层的溶解,造成体系阻抗的降低,随着浸泡时间的增加,表面Zn的腐蚀产物不断生成,对表面起到了明显的保护作用,造成了体系阻抗的升高;第二,在腐蚀历程的第二阶段192~720 h,镀锌钢在3种溶液中均表现为先减小后增大的趋势,在600 h降至最低,体系阻抗的减小可能是由于表面疏松腐蚀产物膜的脱落造成的,待新的腐蚀产物不断生成在表面沉积,体系的阻抗再次升高。
镀锌钢在4#~6# 3种溶液中浸泡720 h的显微形貌如图12所示。可以看出,镀锌钢在3种溶液中的显微形貌并无本质上的差别,均是由球状腐蚀产物堆垛而成,球与球之间会相互合并形成大的团簇,增强腐蚀产物膜的致密性。镀锌钢在以上3种溶液中腐蚀产物膜的化学成分如表6所示,与1#~3#溶液中腐蚀产物膜的成分相似,4#~6#溶液中腐蚀产物膜的主要成分依然是C、O、Na、Zn,其中以5#溶液中生成腐蚀产物膜的O含量最高,6#溶液中生成腐蚀产物膜的Zn含量最高,可以推测其产物主要是Zn的氧化物、氢氧化物和碱式碳酸锌等,主要的化学反应机理与1#~3#溶液中的反应机理相似,这里不再赘述,所不同的是由于溶液中添加了碳酸氢钠,碱式碳酸锌的反应路径除了上述反应式外,还可能通过以下路径,促进了腐蚀产物膜的生成:
图12
图12
镀锌钢在4#~6# 3种调质水中浸泡720 h的显微形貌
Fig.12
Morphologies of the galvanized steel after 720 h immersion in 4# (a), 5# (b) and 6# (c) conditioned water
表6 镀锌钢在3种调质水中腐蚀产物膜的化学成分
Table 6
| Conditioned water | C | O | Zn | Na |
|---|---|---|---|---|
| 4# | 11.8 | 27.7 | 50.3 | 10.2 |
| 5# | 9.8 | 35.4 | 47.2 | 7.6 |
| 6# | 6.9 | 29.9 | 54.8 | 8.4 |
3 结论
(1) 镀锌钢在不同盐度海水获得的反渗透水中表现出了相似的电化学特征,第一阶段,阻抗模值迅速下降,对应着表面锌的快速溶解;第二阶段,阻抗模值缓慢降低,预示着表面腐蚀产物对腐蚀的抑制作用;第三阶段,阻抗模值略有升高,腐蚀产物的不断生成对基体起到了一定的保护作用。相对于进水盐度为25000和45000 mg/L,当进水盐度为35000 mg/L时,镀锌钢在对应的反渗透水中表现出最低的腐蚀速率。
(2) 在反渗透水中增加CaCl2、MgCl2和NaHCO3改变了镀锌钢的腐蚀失效历程和表面形貌特征,其中增加反渗透水中MgCl2和CaCl2的浓度,镀锌钢的腐蚀速率降低,进一步降低水溶液中碳酸氢钠的浓度,镀锌钢的腐蚀速率有所增加,镀锌钢表面不同电化学性质的表现与其表面腐蚀产物膜的附着和脱落密切相关。
参考文献
Investigation on interfacial microstructures and properties of hot-dip galvanizing coating
[D].
热浸镀锌镀层界面结构与性能研究
[D].
Corrosion behavior of field-exposed zinc in a tropical marine atmosphere
[J].
Long-term atmospheric corrosion of zinc
[J].
EXAFS study of atmospheric corrosion products on zinc at the initial stage
[J].
Corrosion behavior of galvanized steels in different atmospheric environments
[J].
镀锌钢在不同大气环境中的腐蚀行为
[J].
Corrosion behavior of galvanized steel in simulated ocean atmosphere
[J]. J
镀锌钢在模拟海洋大气环境下的腐蚀行为
[J].
Corrosion resistance of domestic galvanized steel sheet
[J].
国产镀锌钢板的耐蚀性研究
[J].
Behavior of Zn in atmospheres containing sulfur dioxide and chloride ions
[A].
A Laboratory study of the initial stages of the atmospheric corrosion of zinc in the presence of NaCl; Influence of SO2 and NO2
[J].
Initial formation of corrosion products on pure zinc in saline solution
[J].
Effect of Fe-Zn alloy layer on the corrosion resistance of galvanized steel in chloride containing environments
[J].
Corrosion behavior of galvanized steel in NaCl solution
[J].
镀锌层在NaCl溶液中的腐蚀行为研究
[J].
Effect of Zn(OH)2 on corrosion behavior of galvanized steel in seawater
[J].
海水中Zn(OH)2对镀锌钢腐蚀行为的影响
[J].