CO2腐蚀是油气集输管线和井下管柱面临的普遍问题。实验室研究碳钢的CO2腐蚀通常在烧瓶、高压反应釜等密闭容器中进行。由于这些密闭容器的容积有限,碳钢的腐蚀会导致离子浓度显著改变,即溶液的pH值显著升高、Fe2+浓度大幅增加。然而,对于油气管道中的某一具体位置而言,其pH值和Fe2+浓度并不会随着腐蚀的进行而产生显著变化,这是因为生产过程中,在这一具体位置上不断有新鲜的流体流过[1]。众所周知,pH值和Fe2+浓度的改变会影响碳钢表面腐蚀产物膜的形成,例如,腐蚀产物中FeCO3膜的形成速率,进而影响腐蚀速率[2,3,4,5,6]。因此,实验室评价所获得的腐蚀速率往往与现场管道的腐蚀速率存在较大差异。要减小二者的差异,就必须控制实验过程中溶液的pH值和Fe2+。目前,控制腐蚀过程中的pH值和Fe2+浓度有以下几种方法。第一种方法是尽量增大溶液体积和腐蚀样品表面积之比,减小腐蚀过程中pH值和Fe2+浓度的变化幅度[7,8]。然而,密闭容器的容积毕竟有限,样品面积通常为1~10 cm2,在长周期实验中,这种方法很难保证较为恒定的pH值和Fe2+浓度。第二种方法是建立大型的管道环路,使腐蚀溶液在环路中循环流动,并对管道的某一部分加热,使得Fe2+转化为沉淀,以降低溶液中的Fe2+浓度,同时采用注射泵向管道中注入酸液,以降低pH值[9,10]。这种方法不仅需要复杂的实验装置,还可能向体系中引入新的杂质。第三种方法:建立一种单向流动的装置,使得新鲜溶液不断流经样品表面[11]。这种方法不仅需要大量的测试溶液,且不适用于高温、高压的实验环境。因此,建立一种简单、实用的pH值和Fe2+浓度控制方法,具有重要应用价值。
1 实验方法
1.1 电极及测试溶液
本研究以API 5L X65钢作为研究对象,其化学成分 (质量分数,%) 为:C 13,Cr 14,S 0.009,P 0.009,Mo 0.16,Si 0.26,V 0.047,Ni 0.36,Mn 1.16,Fe余量。将X65钢加工成直径为12 mm,长14 mm的圆柱形电极。实验前用1200#砂纸打磨电极,之后用丙酮在超声水浴中清洗10 min,氮气吹干,放入干燥器中备用。测试采用1%NaCl溶液,将2 L测试溶液倒入烧瓶中,加热至80 ℃,并向溶液中通入CO2,以除去溶液中的O2。除氧2 h后,用注射器向溶液中滴加0.1 mol/L的NaOH溶液,将溶液pH值调至5.80。继续除氧2 h后,用注射器加入FeCl2溶液,使得溶液中的Fe2+浓度为20 mg/L。将研究电极放入测试溶液中,持续通入CO2,实验过程中将CO2进气导管 (见图1) 移至液面以上,避免气泡对电化学测试的影响,以保证实验过程中CO2分压不变 (0.537×105Pa),总压为1.01325×105Pa。
图1
图1
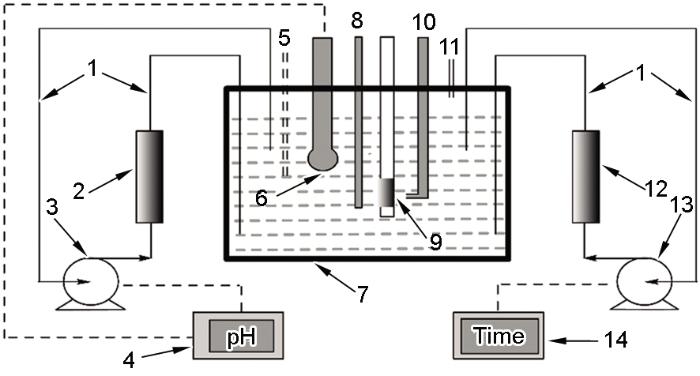
pH值和Fe2+浓度控制装置示意图
Fig.1
Schematic setup for pH and ferrous ion concen-tration control system: (1) stainless steel tubing, (2) column for ion exchange, (3) pump, (4) pH controller, (5) gas inlet, (6) pH probe, (7) flask, (8) counter electrode, (9) X65 steel sample, (10) refer-ence electrode, (11) gas outlet, (12) column for ion exchange, (13) pump, (14) timer
1.2 实验装置及使用方法
实验装置示意图如图1所示,装置由pH值控制、Fe2+浓度控制和电解池3个部分组成。pH值控制部分包括离子交换柱、pH值探头、pH值控制器、恒流泵等几个关键部分。实验前将H型离子交换树脂装入离子交换柱中,实验时打开恒流泵,使溶液流经离子交换柱。H型离子交换树脂能与溶液中的阳离子 (Na+和Fe2+) 发生离子交换,置换出H+并被输送回烧瓶中,使得烧瓶中溶液的pH值降低。恒流泵的通/断由pH值控制器控制,当烧瓶中的pH值高于设定值时,恒流泵运行;当烧瓶中溶液的pH值降至设定值时,恒流泵停止运行。Fe2+浓度控制部分包括离子交换柱、恒流泵、计时控制器。实验前将Na型离子交换树脂放入离子交换柱中,实验中打开恒流泵,使溶液流经离子交换柱,Na型离子交换树脂与溶液中的Fe2+发生交换,释放出Na+,Fe2+被离子交换树脂吸收,实现降低Fe2+浓度的目的。实验中采用计时控制器来控制恒流泵的通/断,采用紫外可见分光光度计运用邻二氮菲法每隔一定时间测定一次溶液中的Fe2+浓度,以调整恒流泵的通断时间比。
1.3 电化学测试及表面表征
电化学测试采用三电极体系,Ag/AgCl电极为参比电极,Pt片为辅助电极,X65碳钢为工作电极。采用Gamry Reference 600电化学工作站连续监测腐蚀过程中的开路电位,并用线性极化技术监测腐蚀速率。线性极化测试中,扫描速率为0.125 mV/s,扫描电位范围为相对开路电位±5 mV。根据下式计算腐蚀速率:
式中,CR代表腐蚀速率,Rp表示极化电阻,B为一个取决于阴、阳极Tafel斜率的常数,M为Fe的摩尔质量,n为Fe原子腐蚀过程中转移电子的个数,F为Faraday常数,ρ为Fe的密度。其中,根据相关文献,本腐蚀体系的B取值26 mV[4]。用Phillips Quanta 200型扫描电子显微镜 (SEM) 观察样品的腐蚀产物膜横截面形貌。
2 结果与讨论
2.1 pH值的控制
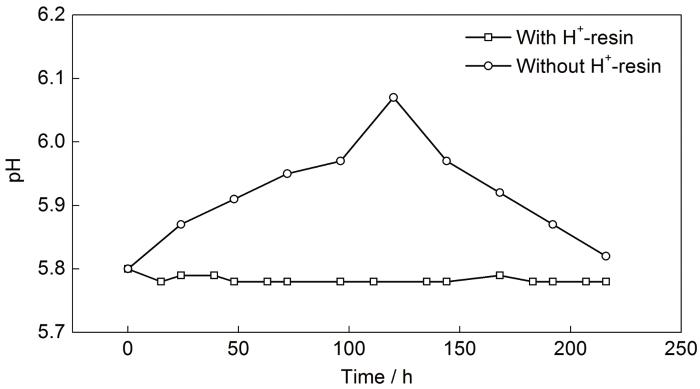
在碳钢的CO2腐蚀过程中,溶液的pH值会发生显著变化,如图2所示。当未使用H型离子交换树脂调节pH值时,pH值随腐蚀时间呈现先升高后降低的趋势。在220 h内,溶液pH值始终高于初始时的5.80。
图2
图2
加入和不加入H型离子交换树脂时X65碳钢腐蚀过程中pH值随时间的变化曲线
Fig.2
pH values as a function of time during the corrosion of X65 in 1%NaCl solution with and without hydro-gen form resin at 80 ℃ (the initial sulution: 20 mg/L Fe2+, pH=5.80 and
当加入H型离子交换树脂后,树脂与溶液中的Na+或Fe2+发生离子交换:
式中,R代表H型离子交换树脂的官能团。发生离子交换后,Na+或Fe2+被吸附在离子交换树脂的官能团上,H+进入溶液并沿着导管进入烧瓶中,使得烧瓶中的pH值降低。在pH值控制器的控制下,实现pH值的自动调节。如图2所示,加入H型离子交换树脂后,溶液的pH值可以控制在5.78~5.80之间。
2.2 Fe2+浓度的控制
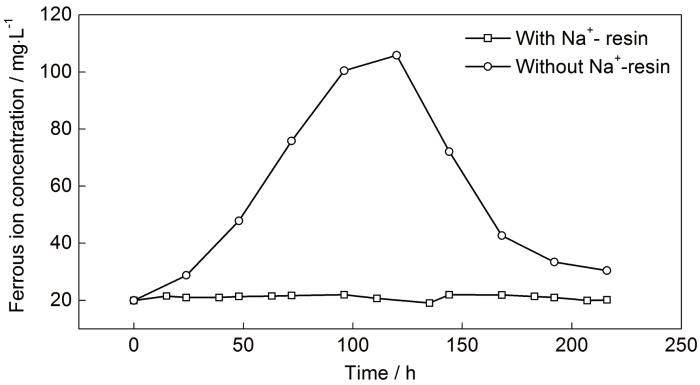
X65钢腐蚀过程中,阳极溶解产生大量的Fe2+,使得溶液中的Fe2+浓度发生显著变化,如图3所示。Fe2+浓度随时间呈先升高后降低的趋势,220 h内Fe2+浓度始终高于初始Fe2+浓度20 mg/L。
图3
图3
加入和不加入Na型离子交换树脂时X65碳钢腐蚀过程中Fe2+浓度随时间的变化曲线
Fig.3
Fe2+concentration as a function of time during the corrosion of X65 in 1%NaCl solution with and with-out sodium form resin at 80 ℃ (the initial solution: 20 mg/L Fe2+, pH=5.80,
当加入Na型离子交换树脂后,树脂与溶液中的Fe2+发生离子交换:
式中,X代表Na型离子交换树脂的官能团。发生离子交换后,溶液中的Fe2+被树脂吸收,Na+被释放出来并随溶液进入烧瓶,使得溶液中的Fe2+浓度降低。在220 h内,溶液中的Fe2+浓度可以控制在19~22 mg/L。与初始Fe2+浓度20 mg/L相比,浓度变化量不超过2 mg/L,基本实现了恒定Fe2+浓度的实验环境,见图3。尽管H型离子交换树脂也可以和Fe2+发生离子交换,见式 (3),但由于要控制溶液的pH值,不能使过量的H+进入溶液,所以Fe2+浓度控制部分选用Na型离子交换树脂。
2.3 恒定pH值和Fe2+浓度下X65钢的腐蚀行为
FeCO3膜是影响碳钢CO2腐蚀速率的关键因素。FeCO3膜越致密、完整,碳钢的腐蚀速率越低。Li等[4]认为,FeCO3膜的形成取决于FeCO3的饱和值S,见下式:
当S>1时,FeCO3即可形成。经计算,当pH值为5.80,CO2分压为0.537×105Pa,在1%NaCl溶液中Fe2+浓度为6.32 mg/L时,S值即为1。本研究中Fe2+浓度初始浓度为20 mg/L,远高于6.32 mg/L,因此,FeCO3可以在实验环境中形成。特别是随着腐蚀的进行,样品表面的Fe2+浓度远高于溶液中Fe2+浓度。同时,样品表面的pH值也比溶液pH值高,更有利于FeCO3膜的形成。从理论计算和Fe2+浓度的测定结果来看,无论是在恒定的pH值和Fe2+浓度条件下,还是在非恒定条件下,FeCO3膜都可以在电极表面形成,其致密程度和完整程度将决定样品的腐蚀速率。
图4为X65碳钢在1%NaCl溶液中腐蚀220 h后,样品表面腐蚀产物的横截面形貌。根据文献[1,4]可知,此种条件下,腐蚀产物膜的成分为FeCO3。在恒定的pH值和Fe2+浓度条件下,样品表面的FeCO3膜不致密,膜层中裂纹较多。同时,FeCO3膜与基体金属之间存在部分间隙,见图4a。然而,在非恒定的pH值和Fe2+浓度条件下,样品表面的FeCO3膜更厚、更致密,与基体金属之间无间隙,见图4b。这是因为在非恒定的pH值和Fe2+浓度条件下,随着腐蚀的进行,溶液的pH值和Fe2+浓度总高于初始pH值和Fe2+浓度 (见图2和3),使得FeCO3膜的生长速率高于恒定条件下FeCO3膜的生长速率。在相同的时间内,非恒定条件下FeCO3的生长速率越高,膜层越厚且越致密。这也预示着非恒定的pH值和Fe2+浓度条件下样品的腐蚀速率会比恒定条件下的低。
图4
图4
恒定和非恒定pH值和Fe2+浓度条件下X65碳钢在1%NaCl溶液中腐蚀220 h后的表面腐蚀产物横截面SEM像
Fig.4
SEM section images of the corrosion products formed on X65 steel in 1%NaCl solution at 80 ℃for 220 h under two different conditions of constant (a) and non-constant (b) pH and ferrous ion concentration (the initial solution: 20 mg/L Fe2+, pH=5.80,
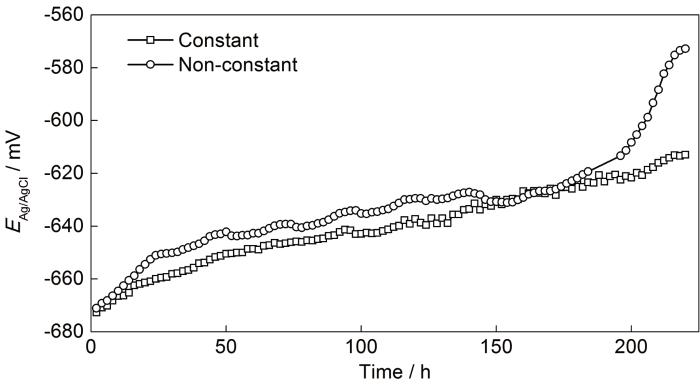
图5为在恒定和非恒定的pH值和Fe2+浓度条件下,X65钢样品的开路电位随时间的变化曲线。可知,在非恒定条件下,X65钢的开路电位在0~196 h内从-672 mV (vsAg/AgCl) 缓慢升至-613 mV。196 h后,开路电位迅速上升,并在220 h后稳定在-572 mV。然而,在恒定的pH值和Fe2+浓度条件下,X65钢的开路电位从初始值-673 mV随时间缓慢上升,220 h时的开路电位仅为-613 mV。结合pH值和Fe2+浓度测定结果可知,非恒定条件下的pH值和Fe2+浓度显著高于恒定条件下的。由前面的讨论可知,pH值和Fe2+浓度越高,越有利于在X65碳钢表面形成FeCO3膜。因此,可以认为,在恒定的pH值和Fe2+浓度下,在220 h内X65钢表面形成的FeCO3膜还不够完整,因此开路电位并没有迅速升高。在非恒定的条件下,X65钢表面的FeCO3膜在196 h后就已经比较完整,因此,开路电位迅速升高并维持相对稳定。样品表面的FeCO3膜的横截面形貌特征也佐证了这一推论。
图5
图5
X65碳钢在恒定和非恒定的pH值和Fe2+浓度条件下腐蚀电位随时间的变化曲线
Fig.5
Corrosion potential as a function of corrosion time for X65 steel in 1%NaCl solution with constant and non-constant pH and ferrous ion concentration at 80 ℃ (the initial solution: 20 mg/L Fe2+, pH=5.80,
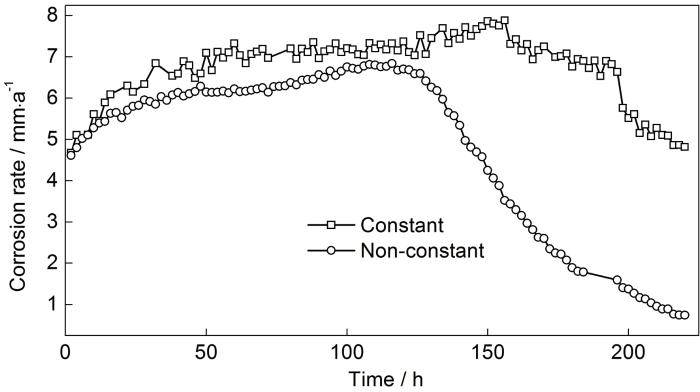
图6为恒定和非恒定的pH值和Fe2+浓度下,X65钢的腐蚀速率随时间的变化曲线。可知,在非恒定条件下,腐蚀速率随时间先缓慢增加,至120 h后又迅速下降,220 h时腐蚀速率约为0.5 mm/a。然而,在恒定条件下,X65钢的腐蚀速率先增加后趋于平稳,在160 h后腐蚀速率才开始缓慢下降,220 h后腐蚀速率仍然高达4.5 mm/a,显著高于非恒定条件下的腐蚀速率。
图6
图6
X65钢在恒定和非恒定的pH值和Fe2+浓度条件下的腐蚀速率随时间变化曲线
Fig.6
Corrosion ratevstime curves of X65 steel during the corrosion in 1%NaCl solution with constant and non-constant pH and ferrous ion concentration at 80 ℃ (the initial solution: 20 mg/L Fe2+, pH=5.80,
根据样品的横截面形貌特征、腐蚀电位和腐蚀速率随时间的变化情况来看,X65钢在恒定的pH值和Fe2+浓度条件下腐蚀行为与非恒定条件下的腐蚀行为存在明显差异。对比可知,220 h后,非恒定条件下,FeCO3膜的致密度更高,腐蚀电位更高,腐蚀速率更低。其本质原因是在非恒定条件下,溶液的pH值和Fe2+浓度总是高于恒定条件下的,导致FeCO3膜的生长速率高于恒定条件下的。由此可见,当温度和CO2分压一定时,pH值和Fe2+浓度是腐蚀速率的决定因素,也是造成样品在密闭容器中的腐蚀速率与油气田现场的腐蚀速率差异的根本原因。
3 结论
(1) 在非恒定的pH值和Fe2+浓度的1%NaCl溶液中,X65钢的腐蚀速率在120 h后迅速下降,220 h后为0.5 mm/a。X65钢表面形成了致密的、与钢基体结合紧密的FeCO3膜。
(2) 在恒定的pH值 (5.80) 和Fe2+浓度 (20 mg/L) 的1%NaCl溶液中,X65钢的腐蚀速率在160 h后才开始缓慢下降,220 h后仍然高达4.5 mm/a。样品表面的FeCO3膜不致密,存在裂纹,在与基体的界面处明显存在间隙。
(3) 相同的温度和CO2分压下,pH值和Fe2+浓度是腐蚀速率的决定因素,也是造成密闭容器中测定的腐蚀速率与油气田现场的腐蚀速率之间差异的根本原因。